Natriumbisulfiitti (NAHSO3) rakenne, ominaisuudet, käyttö, hankkiminen
- 2238
- 205
- Edgar VonRueden
Hän natriumbisulfiitti Se on epäorgaaninen kiinteä kiinteä aine, jonka on muodostettu ioni -natrium -na+ ja HSO -bisulfiitti -ioni3-. Sen kemiallinen kaava on Nahso3. Se on kiteinen valkoinen kiinteä aine, ja sen antioksidanttiominaisuuksia käytetään laajasti elintarvikkeiden säilöntäaineena (esimerkiksi joissakin hilloissa).
Nahso3 Se on pelkistävä kemiallinen yhdiste, joka on päinvastainen hapettumiselle, ja tästä syystä se toimii antioksidanttina monissa sen sovelluksissa, kuten syötävissä tuotteissa, koska se estää sen huonontumista.
 Jotkut kaupalliset hillot sisältävät Nahso -natriumbisulfiittiä3. Kirjoittaja: OpenClipart-Vektorit. Lähde: Pixabay.
Jotkut kaupalliset hillot sisältävät Nahso -natriumbisulfiittiä3. Kirjoittaja: OpenClipart-Vektorit. Lähde: Pixabay. Tätä käyttöä on kuitenkin kyseenalaistettu, koska ihmisillä on ilmoitettu astmatapauksia sen jälkeen, kun he ovat syöneet natriumbisulfiittia sisältäviä ruokia. Sen sanotaan jopa tuhoavan B1 -vitamiini.
Kansainväliset terveysjärjestöt ovat rajoittaneet niiden käyttöä mikrokonteksteihin elintarvikkeissa.
Natriumbisulfiitissa on kuitenkin monia muita käyttötarkoituksia, kuten jodin saamisessa, anti -infektiona, valkaisuaineisiin kudoksiin, puun sulamiseen paperimassan valmistuksen aikana oluen ja viinitynnyreiden desinfiointiaineena jne.
[TOC]
Kemiallinen rakenne
Natriumbisulfiitti muodostuu natrium -kationilla+ ja HSO -bisulfiitti -anionin3-.
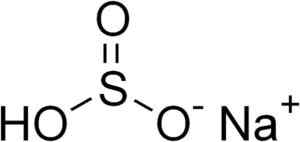 Natriumbisulfiitin kemiallinen rakenne3. Edgar181 [julkinen alue]. Lähde: Wikimedia Commons.
Natriumbisulfiitin kemiallinen rakenne3. Edgar181 [julkinen alue]. Lähde: Wikimedia Commons. Vesipitoisissa liuoksissa bisulfiitti muodostaa 4 lajia. Laimennetussa liuoksessa alla esitettyjen rakenteiden välillä on tasapaino:
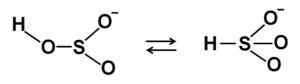 HSO -bisulfiitti -ionirakenteet3- Laimennetussa vesiliuoksessa. Kirjoittaja: Marilú Stea.
HSO -bisulfiitti -ionirakenteet3- Laimennetussa vesiliuoksessa. Kirjoittaja: Marilú Stea. Kun konsentraatio lisää kahta bisulfiittimolekyyliä vuorovaikutuksessa toistensa kanssa muodostaen pyrosulfiitti -ionin S2JOMPIKUMPI52--
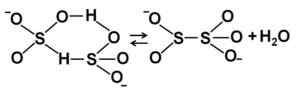 Bisulfiitti -ionirakenteet konsentroituneessa vesiliuoksessa. Kirjoittaja: Marilú Stea.
Bisulfiitti -ionirakenteet konsentroituneessa vesiliuoksessa. Kirjoittaja: Marilú Stea. Nimikkeistö
-Natriumbisulfiitti
-Natriumvetyosulfiitti
-Natriumvesulfiitti.
Ominaisuudet
Fyysinen tila
Kiteinen valkoinen kiinteä aine.
Molekyylipaino
104,06 g/mol
Sulamispiste
Se hajoaa.
Tiheys
1,48 g/cm3 20 ºC.
Liukoisuus
Vesiliukoinen: 29 g/100 g vettä.
PHE
Sen liuokset ovat happamia, pH: n välillä 2,5 - 5,5.
Kemialliset ominaisuudet
Vesiliuoksessa natriumbisulfiitti3 on erotettu ioneihinsa: natriumkationi na+ ja HSO -bisulfiitti -anionin3-.
Jos natriumbisulfiitti altistetaan ilmalle, häviää niin2 ja hapettaa hitaasti sulfaatin2Sw4.
Se voi palvella sinua: galliinihappo: rakenne, ominaisuudet, hankkiminen, käyttöJos hänen hajoamisensa lämmitetään, rikkioksidit ja natrium monoksid.
Se on pelkistävä aine, joka on vastakohta hapettimelle. Ja tästä syystä se voi käyttäytyä antioksidanttina.
Sillä on pieni rikin haju. Se ei ole syttyvä.
Riskejä
Nahso Natrium bisulfiitti3 Se on vahva nahka ja kudos ärsyttävä. Pöly ärsyttää silmiä, nenää ja kurkkua. Nauttimisella ärsyttää vatsaa. Suuret annokset voivat aiheuttaa väkivaltaisia kouristuksia, ripulia, masennusta ja kuolemaa.
Se ei ole polttoainetta, mutta se lämmitetään ärsyttäviä ja myrkyllisiä kaasuja.
Saada
Se valmistetaan kyllästymällä natriumkarbonaattiliuos NA2Yhteistyö3 Rikkidioksidilla niin2 ja kiteytyy liuoksessa.
Sovellukset
Sellu- ja paperiteollisuudessa
Nahso3 Sitä käytetään puun ruuansulatuksessa, niin että siitä voi tulla paperia. Se toimii myös massan valkoisempana.
Sitä käytetään myös kloorin poistamiseen, kun paperimassa on valkaistu tällä.
Elintarviketeollisuudessa
Natriumbisulfiitti sen pelkistävälle omaisuudelle toimii antioksidanttina.
Sitä käytetään säilöntäaineena suuressa määrässä ruokaa ja juomia, mukaan lukien viini ja olut, sen heikkenemisen estämiseksi ja maun parantamiseksi.
Se valkaisee ruokaa, kuten tietyt syötävät tärkkelykset.
Se vähentää tai estää ruoan heikkenemistä, mahdollistaa leivotuissa ruokia käytetyn taikinan ja tarjoilee maissijyvien pehmentämiseksi märän jauhamisen aikana, muun muassa.
Viinin ja oluen käymisen hallitsemisen lisäksi se toimii antiseptisenä kehityksessään, koska se toimii sterilointina ja sienitautien torjunta -aineena tynnyreissä ja piikissä.
 Viini- tai olut tynnyrit desinfioidaan joskus natriumbisulfiittillä3. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay.
Viini- tai olut tynnyrit desinfioidaan joskus natriumbisulfiittillä3. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay. Kuivattuissa hedelmissä se on pitoisuuksina yli 100 ppm (ppm tarkoittaa "osaa miljoonaa"), monissa muissa elintarvikkeissa se on pitoisuutena välillä 10–100 ppm, kuten jäädytettyjä ja kuivia perunoita, suolakurkkuja, kastikkeita ja hilloja.
 Kaupalliset suolakurkku3. Kirjoittaja: Photo Mix. Lähde: Pixabay.
Kaupalliset suolakurkku3. Kirjoittaja: Photo Mix. Lähde: Pixabay. Kiista sen käytöstä ruoassa
Ruoassa on ollut huolestuneita sekä natriumbisulfiitin myrkyllisistä vaikutuksista sekä. On olemassa erilaisia mielipiteitä.
Voi palvella sinua: kaliumferrosyanidiOn ilmoituksia astmapotilaiden haittavaikutuksista, jotka ovat hengityselinsairauksia, NAHO: n nauttimisen jälkeen3. Muut lähteet osoittavat, että bisulfiitti -ioni voi tuhota B1 -vitamiinin tai tiamiinin.
 Tyttö pyrki lääkettä astman lievittämiseen. Kirjoittaja: OpenClipart-Vektorit. Lähde: Pixabay.
Tyttö pyrki lääkettä astman lievittämiseen. Kirjoittaja: OpenClipart-Vektorit. Lähde: Pixabay. Tietyt tutkijat kuitenkin vuonna 1985 havaitsivat, että natriumbisulfiitti suojaa kemiallisilta aineilta ja estää tai estää solujen muutoksen syöpään. Pienet annokset ovat parhaat.
Tämä suojaava vaikutus on selitetty sen pelkistävien tai antioksidanttiominaisuuksien perusteella ja se voi tällä tavalla hyökätä vapaita radikaaleja.
Toisaalta Maailman terveysjärjestö tai WHO (lyhenne englanniksi Maailman terveysjärjestö), suosittelee päivittäisen saannin hyväksyttäväksi tasolle noin 0,7 mg/kg henkilöä.
Tämä tarkoittaa, että on suositeltavaa olla ylittämättä kyseistä määrää.
Yhdysvaltojen elintarvike- ja lääketieteen hallinto tai USFDA (englanninkielinen lyhenne Yhdysvaltain elintarvike- ja lääkehallinto), Hän luokitteli natriumbisulfiittia "yleisesti tunnustettuksi vakuutukseksi".
Maatalouden sovelluksissa
Käytetään alhaisissa pitoisuuksissa Nahso3 Se toimii kasvien kasvun säätelijänä, parantaa fotosynteesiä ja edistää sadon suorituskykyä.
Tämä tavoite on testattu erityyppisissä kasveissa, kuten mansikka- ja teekasvissa.
 Mansikkakasvit parantavat suorituskykyään pienillä määrillä Nahso3 Kasteluvedessä. Kirjailija: alyssapia. Lähde: Pixabay.
Mansikkakasvit parantavat suorituskykyään pienillä määrillä Nahso3 Kasteluvedessä. Kirjailija: alyssapia. Lähde: Pixabay. Se on monien torjunta -aineiden ja biosidien aktiivinen aineosa.
Vesiympäristöissä se voi myös nopeuttaa tiettyjen rikkakasvien torjunta -aineiden muutosta vähemmän myrkyllisiksi tuotteiksi eliminoimalla kloori.
Jodin saamisessa
Nahso3 Se on pelkistävä yhdiste, jota käytetään natrium naion jodin vapauttamiseen3. Tämä on yksi tapa saada jodia lähteistä, kuten Chilen nitro tai jotkut suolat.
Kun brutto chilen nitraattiliuoksen natriumnitraatti kiteytyi, on Naio -liuos3 joka on käsitelty natriumbisulfiittillä3, tuottaa ilmaista jodia.
2 Naio3 + 5 Nahso3 → 3 Nahso4 + Naa2Sw4 + Yllyttää2
Huonekalu- ja puuteollisuudessa
Nahso3 Sitä on testattu soijaproteiinien modifioimiseksi ja sen tarttuvuusominaisuuksien parantamiseksi puulla tavoitteena pakkauskappaleista toisiltaan valmistaa esimerkiksi agglomeraatit, puun pahvi tai kivihävi, vastahakoinen jne. Kaikki huonekaluille tai laudoille, useiden sovellusten joukosta.
Se voi palvella sinua: litiumhydroksidi (LIOH) Sirpaleiden tai puisten jäännösten agglomeraatti. Kirjoittaja: Titus Tschardke [julkinen alue]. Lähde: Wikimedia Commons.
Sirpaleiden tai puisten jäännösten agglomeraatti. Kirjoittaja: Titus Tschardke [julkinen alue]. Lähde: Wikimedia Commons. Tämä tehdään formaldehydiin perustuvien perinteisten liimojen korvaamiseksi, koska sekä niiden valmistusprosessissa että käytön aikana taipumus muokata ilmakehän, joka on myrkyllinen yhdiste.
Natriumbisulfiitti parantaa soijaproteiiniliiman kiinteää pitoisuutta ja vähentää tämän juoksevuuden parantamisen viskositeettia niin, että se tunkeutuu puun huokosiin, lisäämällä sen koheesiota tämän ja kappaleiden välillä.
Soijaproteiiniliima modifioitu NAHSO: lla3 Sillä on hyvä vedenkestävyys ja erinomainen säilytysvakaus johtuen natriumbisulfiitin antioksidanttisesta vaikutuksesta.
Tämä vahvistaa, että modifioidut soijaproteiiniliimat Nahsolla3 Ne ovat verrattavissa formaldehydiin perustuviin liimoihin ja niitä voidaan käyttää huonekalu- ja puuteollisuudessa, mikä on vähemmän saastuttavaa.
Erilaisissa sovelluksissa
Sillä on useita käyttötarkoituksia, yleensä sen pelkistävien ominaisuuksien perusteella (mikä on vastakohta hapettimelle). Tässä on joitain sovelluksia.
-Valokuvauksessa.
-Nahkaparkitsissa hiusten poistamiseksi nahoista.
-Terapeuttinen käyttö:. Sitä käytetään antioksidanttina muutamassa tipassa -ojoosille.
-Maakaasun uuttaminen hydraulisella murtumalla.
-Kuituvärissä sitä käytetään kuumien tai kylmien kylpyammeiden valmistukseen tiettyjen väriaineiden liuottamiseksi.
-Pesulan tai valkaisun pelkistyksenä valkaisuainetta, silkki- ja kasvikuituja.
-Kemian laboratorioissa ihon ja vaatteiden tahrojen poistamiseksi. Biokemian laboratorioissa nestemäisenä säilöntäaineena tai ratkaisuina, jotka voivat heikentyä ajan myötä. Kemiallisena reagenssina.
-Kumilateksin hyytymiselle.
-Kosmetiikkateollisuudessa antioksidanttina.
-Desinfiointiaine ja valkaisu.
-Jäteveden käsittelyssä kloorin eliminoimiseksi desinfioinnin viimeisessä vaiheessa ja kyetä ladata ympäristölle hoidetut vedet.
 Natriumbisulfiittiankki jätevedenkäsittelylaitoksessa Kaliforniassa, missä sitä käytetään ylimääräisen kloorin eliminoimiseen ennen puhdistetut vedet ladataan ympäristöön. Grendelkhan [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons.
Natriumbisulfiittiankki jätevedenkäsittelylaitoksessa Kaliforniassa, missä sitä käytetään ylimääräisen kloorin eliminoimiseen ennen puhdistetut vedet ladataan ympäristöön. Grendelkhan [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)]. Lähde: Wikimedia Commons. Viitteet
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Natriumbisulfiitti. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Qi, G. et al. (2013). Natriumbisulfiittillä modifioitujen Ser -proteiinien tarttuvuus ja fysikaalis -kemialliset ominaisuudet. J Am Oil Chem SOC (2013) 90: 1917-1926. Toipunut AOCS: stä.Verkkokirjasto.Viiva.com.
- Borek, c. et al. (1985). Natriumbisulfiitti suojaa radiogogeenisiltä ja kemiallisesti indusoiduilta muunnoksilta hamsterin alkioissa ja hiiren C3H/10T-1/2 -soluissa. Toxicol Ind Health 1985SEP; 1 (1): 69-74. Palautettu lehdistä.Sagepub.com.
- Friedler, E. et al. (2015). Jatkuva aktiivinen valvontamenetelmä juomaveden ja jätevesien jakautumisjärjestelmien välisten ristikkoyhteyksien tunnistamiseksi. Ympäristö Monit Assess (2015) 187: 131. Linkki palautettu.Jousto.com.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Sunnyvale Cleanwater -ohjelma. (2019). Veden pilaantumisen hallintalaitoksen pääsuunnitelma. Toipunut SunnyvalEclean -vedestä.com.
- Barros Santos, C. (2008). Lisäaineet espanjalaisten ruokinnassa ja heidän valtuutuksensa ja käyttöä säätelevän lainsäädännön. Kirjojen visio. Palautettu kirjoista.Google.yhteistyö.mennä.

