Calcogens tai Amphumos
- 778
- 95
- Eddie Hackett
 Kalkkogeeniset elementit. Lähde: Gabriel Bolívar
Kalkkogeeniset elementit. Lähde: Gabriel Bolívar Mitkä ovat kaltegeenit tai amfumit?
Se Kalteppurit jompikumpi Ankali Ne ovat kemiallisia elementtejä, jotka kuuluvat jaksollisen taulukon ryhmään tai happiperheeseen. Niitä löytyy ryhmästä kautta tai 16, joka sijaitsee oikealla puolella tai lohko P.
Ryhmän pää, kuten nimestä päätetään. Sana 'calcogen' johtuu kreikkalaisesta sanasta Chalcos, Mitä kupari tarkoittaa.
Monet kemikaalit ovat nimenneet nämä elementit tuhkan, liidun, pronssien ja ketjujen kouluttajiksi. Menestynein tulkinta vastaa kuitenkin 'mineraalimuotoilijoiden' tulkintaa.
Siten kalteppeihin on ominaista olla läsnä lukemattomissa mineraaleissa, kuten silikaatteja, fosfaatteja, oksideja, sulfideja, seleniuroja jne.
Toisaalta sana 'ampigeeni' tarkoittaa 'kykenevä muodostamaan happoa tai emäksisiä yhdisteitä ". Yksinkertainen esimerkki tästä on se, että on happoja ja emäksisiä oksideja.
Happea ei löydy vain hengitetystä ilmasta, vaan se on myös osa 49% maankuoresta. Siksi ei riitä katsomaan pilviä saadaksesi sen päähän ja pohtimaan kalsogeenien maksimaalista fyysistä ilmenemistä, on tarpeen käydä vuorella tai malmilla.
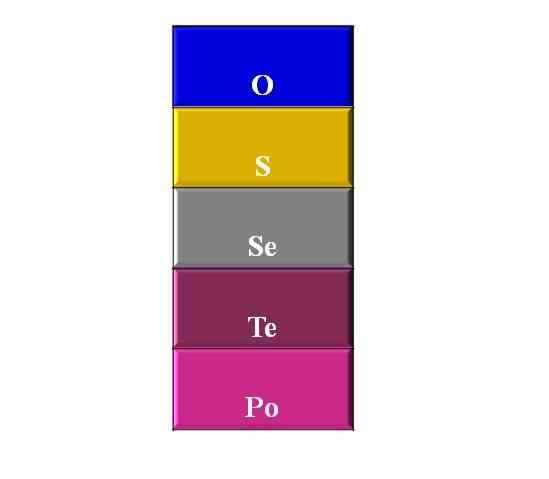
Yläkuva näyttää sarakkeen tai ryhmän, jossa on kaikki sen elementit, joita johtaa happi. Niiden nimeäminen jälkeläisjärjestyksessä on: happi, rikki, seleeni, telurio ja polonium.
Vaikka sitä ei ole esitetty, synteettinen, radioaktiivinen elementti sijaitsee poloniumin alla ja toinen raskain Oganeseon: Light (LV).
Happi
Happea löytyy luonnosta pääasiassa kahtena alotrooppina: o2, molekyyli- tai diatominen happi ja o3, otsoni. Se on kaasua maanpäällisissä olosuhteissa ja se saadaan ilma -nesteytyksestä. Nestemäisessä tilassa se esittelee vaaleita sinertäviä sävyjä, ja otsonin muodossa voi muodostaa punertavan ruskeaa suolaa, nimeltään Orzónidos.
Voi palvella sinua: ammoniumhydroksidiRikki
Luonnollisesti esittelee kaksikymmentä erilaista alotroopea, jotka ovat yleisin kaikista, s8, "Rikki kruunu". Rikki kykenee muodostamaan itsensä syklisten molekyylien tai kierteisten ketjujen kanssa kovalenttisella sidoksella s-s-s ... tämä tunnetaan nimellä Catenation.
Normaaliolosuhteissa se on keltainen kiinteä aine, jonka punertavan ja vihertävän värit riippuvat molekyylin muodostavien rikkiatomien lukumäärästä. Vain kaasufaasissa sitä löytyy diatomisena molekyylinä s = s, s2, samanlainen kuin molekyylin happi.
Seleeni
Seleeni muodostaa lyhyitä ketjuja kuin rikkiä, mutta riittävästi rakenteellisella monimuotoisuudella löytääkseen punaiset, kiteiset ja mustat amorfiset alotroopit.
Jotkut pitävät sitä metalloidina, ja toiset ei -metallielementtiä. Yllättäen se on välttämätöntä eläville organismeille, mutta erittäin alhaisina pitoisuuksilla.
Telurio puolestaan kiteytyy harmahtavana kiinteänä aineena ja sillä on metalloidin ominaisuudet ja ominaisuudet. Se on erittäin niukka elementti maan aivokuoressa, löytää pieninä pitoisuuksina harvinaisissa mineraaleissa.
Poloni
Kaikista kalsogeeneistä se on ainoa metallielementti, mutta kuten 29 isotooppiaan (ja muita), se on epävakaa, erittäin myrkyllinen ja radioaktiivinen. Sitä löytyy jäljempänä joissakin uraanimineraaleissa ja tupakansavussa.
Ominaisuudet
Elektroninen kokoonpano ja Valencia -tilat
Kaikilla kalteppeilla on sama elektroninen kokoonpano: NS2NP4. Heillä on, Valenciaa on kuusi elektronia. Lohteessa P, jaksollisen taulukon oikealla puolella, heillä on taipumus saada enemmän elektroneja kuin menettää ne, joten kaksi elektronia ansaitsee Valencian oktettinsa loppuunsaattamiseksi ja hankkia seurauksena Valencia -2 -2.
Voi palvella sinua: litiumkloridi (LICL): Ominaisuudet, riskit ja käytötHe voivat myös menettää kuusi Valencian elektronia, jotka ovat +6: n tilassa.
Valencian mahdolliset kalsogeenien tilat vaihtelevat -2 -+6, nämä kaksi ovat yleisimpiä. Ryhmän laskeutuessa (hapesta poloniumiin), positiivisen valenssitilojen elementtien taipumus kasvaa, mikä on yhtä suuri kuin metallisen luonteen lisääntyminen.
Esimerkiksi happi hankkii melkein kaikissa yhdisteissään Valencia --2 -tilan, paitsi silloin, kun se muodostaa yhteyksiä fluoriin, pakottaen sen menettämään elektronit suuremman elektronegatiivisuuden vuoksi, ottaen käyttöön Valencia -tilaa +2 (of of of of 42-A. Peroksidit ovat myös esimerkki yhdisteistä, joissa hapella on Valencia -1 ja ei -2.
Metallinen ja ei -metallinen merkki
Kun ryhmä laskeutuu, atomiradiot kasvavat ja niiden kanssa elementtien kemialliset ominaisuudet muokataan. Esimerkiksi happi on kaasua ja termodynaamisesti on stabiilia diatomisina molekyylinä O = O, kuin "hapetettu ketju" O-o-o-o ..
Se on ryhmän suurempi ei -metallisesta luonteesta, ja siksi se muodostaa kovalenttisia yhdisteitä kaikkien P -lohkon elementtien kanssa ja joidenkin siirtymämetallien kanssa.
Ei -metallinen merkki vähenee metallisen luonteen kasvaessa. Tämä heijastuu fysikaalisissa ominaisuuksissa, kuten kiehumis- ja fuusiopisteissä, jotka kasvavat rikkiä poloniumiksi.
Toinen ominaisuus metallisen luonteen lisääntymiselle on Telurion ja poloniumin muodostamien yhdisteiden kiteisten kokoonpanojen lisääntyminen.
Yhdisteet
Jotkut kalsogeenien muodostamat yhdisteet mainitaan yleensä alla.
Voi palvella sinua: isopentano: rakenne, ominaisuudet, käyttötarkoitukset, hankkiminenHydrorit
-H₂o
-H2S
IUPAC -nimikkeistön mukaan sitä kutsutaan rikkivetyksi eikä rikkihydridiksi, koska H: stä puuttuu Valencia -1 -1.
-H2HÄN
Samoin se on nimetty vety Seleniuroksi, samoin kuin muu hydros.
-H2Teetä
-H2Poikki
Happihydridi on vettä. Muut ovat haisevia ja myrkyllisiä, koska he ovat H -olo2S tunnetuin kaikista, jopa populaarikulttuurissa.
Sulfidit
Kaikilla on yhteistä anionia s2- (Yksinkertaisin). Heidän joukossaan ovat:
-Mgs
-Fes
-Kufes2
-Naa2S
-Bassi
Samalla tavalla on selenuroja, tiedän2-, Telenuros, TE2-, ja Polonuros, PO2-.
Halogeeniros
Kalsogeenit voivat muodostaa yhdisteitä halogeenien kanssa (F, Cl, BR, I). Jotkut niistä ovat:
-Tei2
-S2F2
--2
-SCL2
-SF6
-Sebr4
Oksidit
Lopuksi on oksideja. Niissä hapen valenssi on -2, ja se voi olla ioninen tai kovalenttinen (tai molempien ominaisuudet). Heillä on esimerkiksi seuraavat oksidit:
-Sw2
-Teo2
-Ag2JOMPIKUMPI
-Usko2JOMPIKUMPI3
-H₂O (vetyoksidi)
-SEO3
On muitakin satoja tuhansia yhdisteitä, joihin liittyy mielenkiintoisia kiinteitä rakenteita. Lisäksi ne voivat esiintyä polykisktejä tai polisyaatioita, etenkin rikki- ja seleenitapauksissa, joiden ketjut voivat hankkia positiivisia tai negatiivisia kuormituksia ja olla vuorovaikutuksessa muiden kemiallisten lajien kanssa.
Viitteet
- Chalcogens. Kannattaa. Kemia.com.

