Orgaaniset yhdisteet

- 4891
- 285
- Shawn Stanton II
Selitämme, mitkä orgaaniset yhdisteet ovat, niiden ominaisuudet, tyypit, jotka ovat, erot epäorgaanisten yhdisteiden kanssa ja annamme useita esimerkkejä
 Orgaaniset yhdisteet tulevat elävistä olennoista
Orgaaniset yhdisteet tulevat elävistä olennoista Mitkä ovat orgaanisia yhdisteitä?
Se Orgaaniset yhdisteet Ne ovat niitä, jotka tulevat elävistä olennoista ja sisältävät toisiinsa kytkettyjä hiili- ja vetyatomeja avoimien ketjujen tai suljettujen syklien muodossa.
Hiilen ja vedyn lisäksi orgaaniset yhdisteet voivat sisältää myös muita elementtejä, kuten happea (O), typpeä (N), rikkiä (S), fosforia (P), fluoria (F), klooria (CL), Bromi (BR) tai jodi (i). Kaikkia näitä kutsutaan heteroátomosiksi.
Elämä ei olisi mahdollista ilman orgaanisia yhdisteitä, joten kaikki elävät olennot sisältävät niitä. Näitä aineita on tuhansia ja löydämme ne kaikkialta, alkaen omasta ruumiistamme.
Orgaanisten yhdisteiden ominaisuudet
Ne perustuvat hiilikemiaan
Hiili muodostaa kaikkien orgaanisten yhdisteiden perustan. Näissä yhdisteissä hiiliatomit voidaan kytkeä toisiinsa tai muiden elementtien kanssa. Jokainen hiiliatomi muodostaa aina 4 sidosta yhteensä yksinkertaisten, kaksinkertaisten ja kolminkertaisten sidosten välillä.
Heillä on kovalenttisia linkkejä
Pääkemiallisia linkkejä on kolme tyyppiä, jotka ovat kovalenttisia, ionisia ja metallisia sidoksia. Orgaanisille yhdisteille on ominaista, että heillä on vain kovalenttiset sidokset kaikkien atomiensa joukossa.
Ne ovat polttoaineita
 Hiili on polttoaine, joka saadaan puussa olevista orgaanisista yhdisteistä
Hiili on polttoaine, joka saadaan puussa olevista orgaanisista yhdisteistä Sisällyttämällä niin monta hiiliatomia, orgaaniset yhdisteet ovat palavia. Tämä tarkoittaa, että he voivat palata palamisreaktion avulla ilman hapen kanssa.
Orgaanisten yhdisteiden palamisreaktiot ovat eksotermisiä reaktioita, jotka vapautuvat hyvin lämpöä. Kaikki elävät olennot hyödyntävät kaikkea tätä energiaa suorittaakseen kaikki reaktiot, jotka pitävät meidät hengissä.
Heillä on isomeria
Monilla orgaanisilla yhdisteillä on sama molekyylin kaava, mutta ne ovat täysin erilaisia yhdisteitä. Tätä ominaisuutta kutsutaan isomeíaksi, ja se on ominaista orgaanisille yhdisteille.
Esimerkiksi molemmilla metallisella etanolin etanolilla on molekyylinen kaava C2H6Tai, mutta ensimmäinen on kaasu, kun taas toinen on neste.
Ne voivat muodostaa polymeerejä
Toinen orgaanisten yhdisteiden ominaisuus on, että ne voivat muodostaa jättiläisiä molekyylejä, jotka toistavat atomiryhmän uudestaan ja uudestaan pitkässä ketjussa. Näitä yhdisteitä kutsutaan polymeereiksi ja tyypillinen esimerkki niistä on muoveja.
Liukoisuus
Toinen ominaisuus, joka kuvaa orgaanisia yhdisteitä, on niiden liukoisuus. Monet heistä, erityisesti polaariset orgaaniset yhdisteet, liukenevat veteen. Muut yhdisteet eivät liukene veteen, vaan orgaanisissa liuottimissa, kuten sykloheksanissa.
Voi palvella sinua: sucniinihappo: rakenne, ominaisuudet, hankkiminen, käyttöOrgaanisten yhdisteiden tyypit
Orgaanisilla yhdisteillä on ominaisuuksia ja ominaisuuksia, jotka tekevät niistä hyvin erilaisia kuin epäorgaaniset yhdisteet (ne, jotka eivät tule elävistä olennoista, kuten mineraaleista).
Monet näistä ominaisuuksista antavat heille luokitella ne eri tavoin, mikä aiheuttaa erityyppisiä orgaanisia yhdisteitä. Tärkeimmät luokituskriteerit ovat:
- Sen alkuperän mukaan.
- Sen rakenteen ja koostumuksen mukaan.
- Funktionaalisen ryhmän mukaan.
- Hänen napaisuudensa mukaan.
Seuraavaksi kuvataan kunkin näiden kriteerien mukaan luokiteltujen orgaanisten yhdisteiden tyypit:
Orgaanisten yhdisteiden tyypit niiden alkuperän mukaan
Jos ne ovat peräisin, orgaaniset yhdisteet voivat olla:
- Luonnolliset orgaaniset yhdisteet: Ne ovat luonnosta ja ne tulevat suoraan elävistä olennoista. Selluloosa on hyvä esimerkki, koska se on maan runsain luonnollinen orgaaninen yhdiste.
- Synteettiset orgaaniset yhdisteet: Ne viittaavat orgaanisiin yhdisteisiin, jotka kemikaalit syntetisoivat laboratoriossa tai kemiallisessa kasvissa. Kaikki päivittäin käyttämämme muovit ovat synteettisiä ja myös monia lääkkeitä.
Orgaanisten yhdisteiden tyypit niiden rakenteen ja koostumuksen mukaan
Niiden atomien mukaan ja tapa, jolla nämä atomit yhdistyvät yhteen, orgaaniset yhdisteet voivat olla:
- Alifaattiset hiilivedyt: muodostettu vain hiili ja vety ja missä hiilet muodostavat avoimia ketjuja joko lineaarisesti tai haarautuneita. Ne sisältävät alquenos ja alkines.
- Aromaattiset hiilivedyt: Tähän perheeseen kuuluvat yhdisteet, joita kutsutaan myös hiekkaksi, sisältävät tyydyttymättömiä syklejä (joilla voi silti olla enemmän vetyä), joilla on suuri molekyylin stabiilisuus. Tätä ominaisuutta kutsutaan aromaattisuudeksi ja se on ominaista bentseenille ja kaikille sen johdannaisille.
- Heterosykliset yhdisteet: Ne ovat syklisiä yhdisteitä, joissa yksi tai useampi hiiliatomi korvataan heteroátomolla, joka voi olla happea, typpeä, rikkiä tai fosforia. Esimerkkejä heterosykleistä ovat pyridiini ja furano.
- Organometalli yhdisteet: Ne ovat erityinen yhdisteiden luokka, joka on puolivälissä orgaanisen ja epäorgaanisen välillä. Niille on ominaista, että se sisältää orgaanisen osan heteroátomilla.
Orgaanisten yhdisteiden tyypit funktionaalisen ryhmän mukaan
Orgaanisen molekyylin osa, jossa kemiallisia reaktioita yleensä esiintyy, on pieni atomien ryhmä, jota kutsutaan funktionaaliseksi ryhmäksi. On olemassa useita erilaisia funktionaalisia ryhmiä, jotka mahdollistavat orgaanisten yhdisteiden luokittelun:
- Sulkeutuu: Ne sisältävät vain hiiltä ja vetyä, joka on kytketty vain yksinkertaisilla sidoksilla. Esimerkiksi butaani.
- Alkeenia: Ne ovat hiilivetyjä, jotka sisältävät kaksoishiilihiilisidoksen. Esimerkiksi buuteni.
- Alkynit: Ne ovat hiilivetyjä, jotka sisältävät kolminkertaisen hiilihiilisidoksen. Esimerkiksi Etino, joka tunnetaan myös nimellä asetyleeni.
- Alkyylihalogenurot: Orgaaniset yhdisteet, jotka sisältävät halogeenin (F, Cl, BR tai I), joka on kytketty alifaattiseen hiileen. Esimerkiksi klorometaani.
- Alkoholit: Alkoholit ovat polaarisia orgaanisia yhdisteitä, jotka sisältävät hydroksyyliryhmän (-OH) yhdessä alifaattisen hiilen kanssa.
- Fenolit: Nämä yhdisteet sisältävät myös hydroksyyliryhmän (-OH), mutta tässä tapauksessa yhdessä aromaattisen hiilen kanssa.
- Eetterit: Ne tunnistetaan helposti, koska ne ovat kaksi hiiliketjua yhdessä toistensa kanssa happiatomilla. Esimerkiksi metyylieetteri.
- Amiini: Ne ovat orgaanisia yhdisteitä, jotka ovat peräisin ammoniakista (NH3-A. Ne sisältävät yhden tai useamman alifaattisen hiilen (alkyyliryhmät), jotka on kytketty typpiatomiin yksinkertaisten sidosten avulla.
- Aldehydit: Hapetetut orgaaniset yhdisteet, jotka sisältävät karbonyyliryhmän (C = O) yhdessä vedyn kanssa yhdessä sen terminaalista hiilistä. Yleensä heillä on ominaisia hajuja, kuten Cinamaldehydi, joka antaa kanelin hajun.
- Ketonit: Ne ovat happea orgaanisia yhdisteitä, jotka sisältävät karbonyyliryhmän (C = O) yhdessä kahden hiiliketjun kanssa.
- Karboksyylihapot-.
- Esterit: Ne tulevat alkoholin karboksyylihapon liitosta. Tässä tapauksessa karboksyyliryhmän vety korvataan vuokraryhmällä.
- Amidas: Ne tulevat karboksyylihapon liitosta amiinilla. Tässä tapauksessa karboksyyliryhmän OH korvataan typellä, joka on kiinnitetty kahteen vetyyn, vetyyn ja alkyyliin tai kahteen alakkaan.
Orgaanisten yhdisteiden tyypit niiden napaisuuden mukaan
Voimme myös luokitella orgaaniset yhdisteet polaariin ja apolaariin:
- Polaariset orgaaniset yhdisteet: Näillä yhdisteillä on polaariset kovalenttiset sidokset atomien kanssa, kuten typpi ja happi, jotka tekevät koko molekyylistä polaaria. Suurin osa näistä yhdisteistä on liukoinen veteen.
- Apolaariset orgaaniset yhdisteet: He ovat niitä, joilla ei ole polaarisia linkkejä tai linkkien napaisuuksia peruutetaan toisiinsa. Nämä yhdisteet eivät liukene veteen.
Erot orgaanisten yhdisteiden ja epäorgaanisten yhdisteiden välillä
Seuraava taulukko on yhteenveto orgaanisten ja epäorgaanisten yhdisteiden välisistä eroista:
Orgaaniset yhdisteet | Epäorgaaniset yhdisteet | |
Alkuperä: | Tulevat elävistä olennoista tai heidän jäännöksistä. | He eivät tule elävistä olennoista. |
Sävellys: | Muodostuneet melkein yksinomaan C, N, O, S, P, F, Cl, Br ja I. | Ne voidaan muodostaa jaksollisen taulukon minkä tahansa elementin avulla. |
Linkkityypit: | Ne muodostavat kovalenttisia sidoksia sekä napaina että apolaarina. | Ne voivat muodostaa kaikentyyppisiä kemiallisia linkkejä, mukaan lukien polaariset, apolaariset, ioniset tai metalliset kovalenttiset sidokset. |
Isomery: | Suurin osa ISomeía. | Vain jotkut nykyiset isomeía. |
Polttoaineet: | Ne ovat polttoaineita. | Useimmat eivät ole palavia. |
Esimerkkejä orgaanisista yhdisteistä
1. Metaani (ch4-A
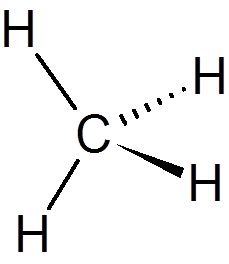
2. Etyyliasetaatti (C4H8JOMPIKUMPI2-A
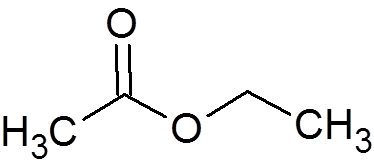
3. Bentseeni (c6H6-A
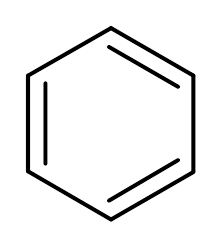
4. Etyylialkoholi (c2H6JOMPIKUMPI)
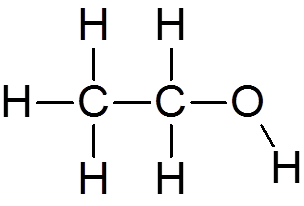
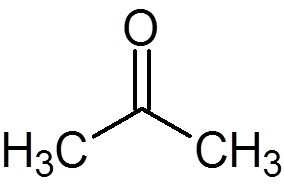
5. Asetoni (c3H6JOMPIKUMPI)
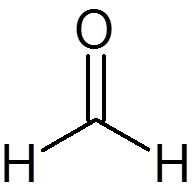
6. Formaldehydi (ch2JOMPIKUMPI)
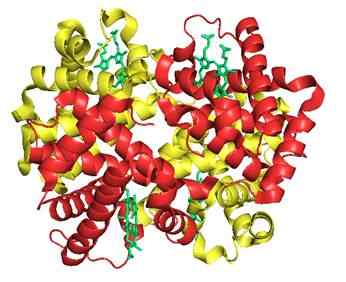
7. Hemoglobiini (proteiini)
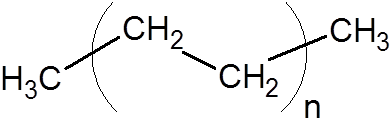
8. Polyeteeni (yksi yleisimmistä muoveista)
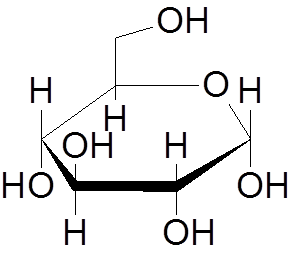
9. Glukoosi (c6H12JOMPIKUMPI6-A
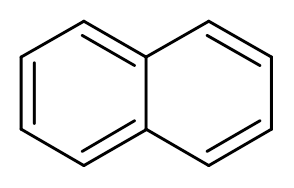
10. Naftaleeni (C10H8-A
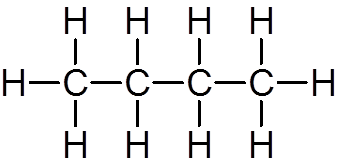
yksitoista. Butano (c4H10-A
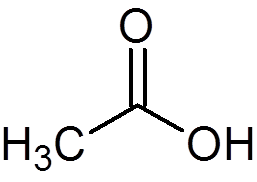
12. Etikkahappo tai etikka (C2H4JOMPIKUMPI2-A
13. Neopentano (C5H12-A
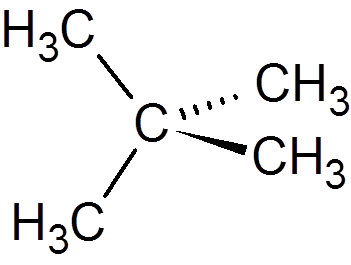
14. Sykloheksan (C6H12-A
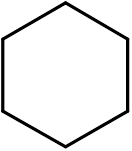
viisitoista. Pyridiini (C5H5N)
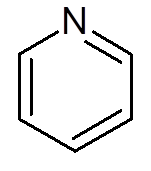
16. Guanina (c5H5N5JOMPIKUMPI)
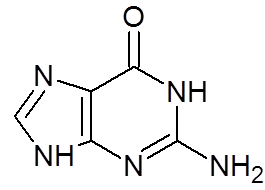
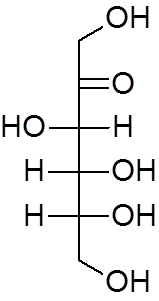
17. Fruktoosi (c6H12JOMPIKUMPI6-A
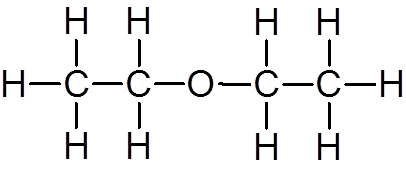
18. Etyylieetteri (C4H10JOMPIKUMPI)
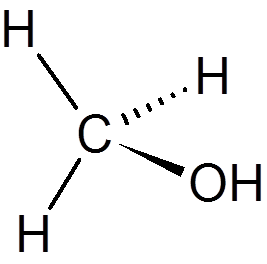
19. Metanoli (ch4JOMPIKUMPI)
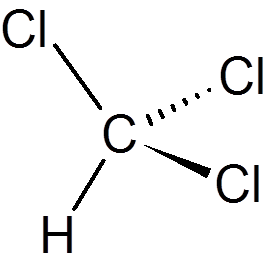
kaksikymmentä. Kloroformi (CHCL3-A
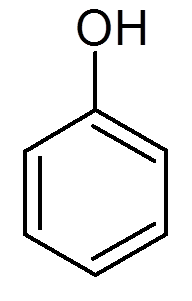
kaksikymmentäyksi. Fenoli (c6H6JOMPIKUMPI)
22. Asetyleeni (C2H2-A
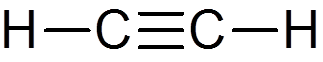
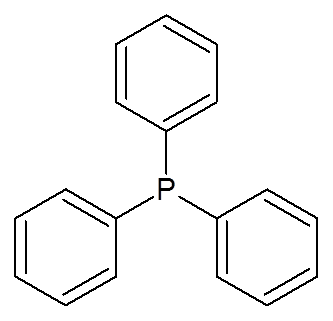
23. Trifenyylifosfiini ((C6H6-A3P)
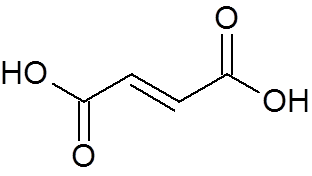
24. Trans-buteodioiinihappo (C4H4JOMPIKUMPI4-A
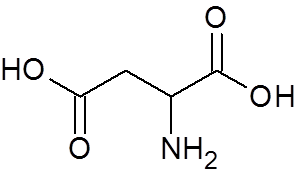
25. Asparagiinihappo (aminohappo) (C4H7EI4-A
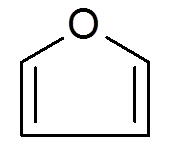
26. Furano (c4H4JOMPIKUMPI)
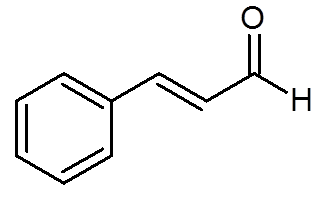
27. Cinamaldehydi (kanelin tuoksu) (C9H8JOMPIKUMPI)
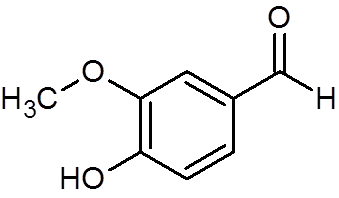
28. Vaniliini (c8H8JOMPIKUMPI3-A
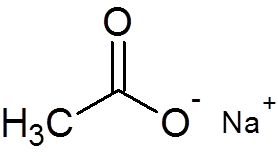
29. Natriumasetaatti (C2H3JOMPIKUMPI2Na)
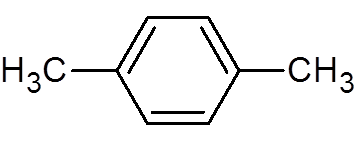
30. P-ksyleeni (c8H10-A
Viitteet
- Carey, f., & Giuliano, R. (2013). Orgaaninen kemia, 9. painos (9. painos.-A. New York City, New York: McGraw-Hill Education.
- Linna a., M. G. (S.F.-A. Orgaanisten yhdisteiden ja funktionaalisten ryhmien pääluokat. Palautettu Yhdistyneestä yhdistymisestä.Edu.MX
- Chang, R., & Goldsby, K. -Lla. (2012). Kemia, 11. painos (11. ed.-A. New York City, New York: McGraw-Hill Education.
- Klein, D. R -. (2011). Orgaaninen kemia (1.-lla Ed.-A. Hoboken, New Jersey: Wiley.
- Morrison, r. T., & Boyd, R. N. (2003). Orgaaninen kemia (6. ed.-A. Boston, Massachusets: Allyn & Bacon.

