Glyseraldehydin rakenne, ominaisuudet, toiminnot
- 3269
- 1053
- Mr. Clifford Kshlerin
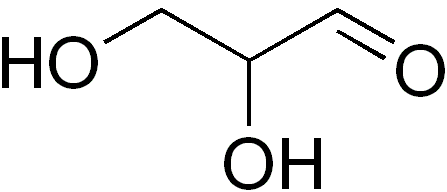
Hän glyseraldehydi Se on ainoa kolmen hiilen monosakkaridi, joka on vuorostaan ainoa triosa. Se on myös aldotriosa, koska siinä on aldehydiryhmä. Sana glyseraldehydi tulee glyseriini- ja aldehydiyhdistelmästä. Tämä johtuu siitä, että glyseraldehydi on samanlainen kuin glyseriini, mutta Carbon One (C-1) on aldehydi.
Glyseraldehydin kemiallinen synteesi suoritetaan eri menetelmillä, esimerkiksi entsyymejä käyttämällä. Glyseraldehydi on melko reaktiivinen molekyyli, joka pystyy muodostamaan törkeää proteiinien välillä.
 Lähde: DRTW Hollannin Wikediassa [CC BY-SA 3.0 (http: // creativecommons.Org/lisenssit/by-SA/3.0/]]
Lähde: DRTW Hollannin Wikediassa [CC BY-SA 3.0 (http: // creativecommons.Org/lisenssit/by-SA/3.0/]] [TOC]
Rakenne
Glyseraldehydillä on epäsymmetrinen tai kiraalinen keskus (hiiliatomi 2, C-2). Se muodostaa kaksi enantiomeeriä D (dekstrogyr) ja L (levógiro), jotka kiertävät polarisoidun valon tasoa vastakkaisiin suuntiin: D-glyseraldehydi kääntää sen oikealle ja L-glyseraldehydi vasemmalle.
D-glyseraldehydin spesifinen optinen kierto 25 ºC: n lämpötilassa on +8,7º ja D-glyseraldehydin spesifinen optinen kierto, 25 ° C: ssa, on -8,7º. D-glyseraldehydi löytyy usein luonnossa, pääasiassa glyseraldehydi 3-fosfaattina.
L-glyseraldehydi-kokoonpano käytetään kuinka vakioviite hiilihydraateille. Biologisissa molekyyleissä D-sokeri on runsaasti. Glyseraldehydin hiiliatomi 3 (C-3) on hydroksimetyleeniryhmä (-CH2VAI NIIN).
Ominaisuudet
Glyseraldehydikiteitä ovat värittömiä ja niillä on makea maku. Tämän sokerin empiirinen kaava on c3H6JOMPIKUMPI3 ja sen molekyylipaino on 90 g/mol.
Vesipitoisessa liuoksessa DL-glyseraldehydi on pääasiassa aldehydrolina, joka on aldehydin hydratoitunut muoto. Kiteinen dl-gliceraldehido on dimic.
Glyseraldehydikiteiden analyysi röntgensäteillä on osoittanut, että sillä on 1,4-dioksaanirengasta kaikkien substituenttien kanssa päiväntasaajan suunnassa.
Vesipitoisessa liuoksessa glyseraldehydi kokee itsensä hapettumista, joka tuottaa vapaata radikaalia. Tämä liittyy nopeaan hapenkulutukseen.
Se voi palvella sinua: ProtocooperationHapenkulutuksen nopeus pienenee hitaasti superoksididysmutaasin läsnä ollessa. Tämä viittaa siihen, että glyseraldehydi -autooksidaation aikana on superoksidien muodostumista. Glyseraldehydi -autoxidin rajoittava kulku
D-glyseraldehydin synteesiä katalysoivat primaariset ja sekundaariset aminohappot, jotka ovat suosittuja matalalle pH-arvolle (3-4).
Funktiot
Ristien linkityksessä proteiinien välillä
Proteiini-proteiini-vuorovaikutus on monikompleksisten biologisten prosessien molekyylimekanismi. Nämä vuorovaikutukset voivat olla väliaikaisia, proteiinin vuorovaikutus metabolisesta reitistä tai signaalin translaatiosta.
Kemiallinen silloitus muodostaa suora menetelmä siirtymä- ja stabiilien proteiini-proteiini-vuorovaikutusten tunnistamiseksi.
Proteiinin välistä linkintätekniikkaa koostuu kovalenttisten sidosten muodostumisesta, joille käytetään bifuncional -reaktiivisia ryhmiä, jotka reagoivat aminohuryhmien ja aminohappojätteen proteiiniryhmien kanssa.
Erityisesti agentit reagoivat primaaristen amingiryhmien kanssa (kuten liisinien jätteiden Epsilon-amino) ja muodostavat leikkauksen sekä proteiinien alayksikön ja proteiinien alayksiköiden välillä.
Kaupallisesti saatavia edustajia on laaja valikoima. Vaikka glyseraldehydi on ristikkäinen linkki -aine, on muitakin suositumpia edustajia, kuten glutaraldehydi. Tämä johtuu siitä, että gluteraldehydi ylläpitää proteiinin rakenteellista jäykkyyttä, mikä on tärkeä vaatimus monissa tutkimuksissa.
Muita suosittuja tekijöitä ovat homobifunktionaaliset jäljittäjät, jotka vaihtelevat välikappaleiden pituudesta heidän reaktiivisten ryhmien keskuudessa. Joitakin esimerkkejä imidoestereista ovat dimetyyliapimidato (DMA), dimetyylisuberimidaatti (DMS) ja dimetyylipimilimidato (DMP).
Voi palvella sinua: Homopolysakkaridit: Ominaisuudet, rakenne, toiminnot, esimerkitRistien linkityksessä gelatiinimikropallojen välillä
Gelatiinimikropalloilla on potentiaali palvella hallittuun lääkkeen vapautumiseen. Tämä johtuu siitä, että nämä mikropallot eivät ole myrkyllisiä ja että niiden tuotteet erittyvät helposti. Gelatiini on kuitenkin liukoinen polymeeri, joten sitä on modifioitava lääkkeen kuljetusjärjestelmänä toimimaan.
D, L-Glyeraldehydi voidaan pitää myrkyttömänä silloitusaineena (tappava annos, DL50 I I.p. Rotilla se on 2000 mg/kg). Lisäksi ihmiskehossa triosa-kinaasi fosforyloidaan D-glyseraldehydiin. Tällä tavoin muodostuu 3-fosfaattihylyysi, joka tulee glykolyysiin.
Gelatiinimikropallojen käsittely D, L-glyseraldehydin kanssa 24 tunnin ajan tuottaa mikropalloja, joissa on useita pienentyneet vapaat lysiiniaminohapot. Siksi mikropallojen kyky pidentää esimerkiksi kloodiniinihydrokluridin vaikutus, joka on verenpainelääke.
Mikropalloja annettiin ihonalaisella injektiolla pilkkaamaan albiineja ja rotilla. Injektion jälkeen systolinen verenpaine laski kahden tunnin ajan, myöhemmin palauttaen sen perusarvo. Injektiopaikan kankaat analysoitiin ja mikropäätä ei löytynyt, vaikka tulehduksia havaittiin.
Prebioottisissa reaktioissa
Prebioottisissa olosuhteissa - kuten sellaisissa, joiden oletetaan olevan primitiivinen maa - formaldehydi olisi voinut palvella glyseraldehydin synteesiä, kemiallisiin prosesseihin osallistuvan kemiallisen välittäjän kanssa, joka olisi voinut saada aikaan elämän.
Aikaisempi hypoteesi perustuu siihen, että sekä glykolyysillä että fotosynteesillä on glyseraldehydi 3-fosfaatti metabolisena välittäjänä.
On ehdotettu kemiallista mallia, joka selittää formaldehydin glyseraldehydin biosynteesiä syklisen reitin kautta. Glyseraldehydin synteesi tapahtuu lisäämällä formaldehydiä triosaan (glyseraldehydi ↔ dihydroksiasetoni) tetrosan (↔ aldotrosa ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ ↔ aldot.
Voi palvella sinua: Erythous: Ominaisuudet, rakenne, toiminnotFormaldehydin lisääminen glysaldehydiin täydentää sykliä. Kahden triosa -molekyylin synteesi kuudesta formaldehydimolekyylistä tapahtuu.
Yleensä sokerien prebioottinen synteesi uskotaan, että formosan reaktio on mukana, jossa formaldehydi pienen määrän glykalehydiä muunnetaan sokereiksi aldoolisten kondensaatioreaktioiden avulla.
On ehdotettu, että prebioottinen sokerin hapettuminen (glykaldehydi, triosas, tetrosas) tuottivat polyhydroksiasideja, jotka toimivat itse -metaliittisina aineina.
Glyseraldehydin muuntaminen maitohapoksi ja glykemihapoksi, oksidista riippuvainen rautahydroksidista, viittaa näiden hydroksasidien oligoéstereihin tämän materiaalin pinnalla.
Viitteet
- Breslow, R., Ramalingam, V., Appaeee, c. 2013. Glyseraldehydin synteesin katalyysi primaaristen tai sekundaaristen aminohappojen kanssa prebioottisissa olosuhteissa pH: n funktio. Elämän evoluutio biosfana. Doi 10.1007/S11084-013-9347-0.
- Carey, f. -Lla., Giuliano, r. M. 2016. Orgaaninen kemia. McGraw-Hill, New York.
- Robyt, J.F. 1998. Hiilihydraattikemian olennaiset. Springer, New York.
- Thornalley, P., Wolff, s., Crabbe, J., Stern, a. 1984. Glyseraldehydin ja muiden yksinkertaisten monosakkaridien autoksidointi fysiologisella katalysoimalla puskurilla. Biochimica et Biophysica Acta, 797, 276-287.
- Vandelli, m.-Lla., Rivas, f., Sota, P., Forni, f., Arletti, r. 2001. Mikropallot gelatiini silloitettuna D: n, L-glyseraldehydin kanssa potentiaalisena Drarug-toimitusjärjestelmänä: valmistus, karakterisointi, in vitro ja in vivo -tutkimukset. International Journal of Pharmaceutics, 215, 175-184.
- Weber, a.Lens. 1987. Pose -malli: Glyseraldehydi energian ja monomeerien lähteenä prebioottisten kondensaatioiden reaktioille. Elämän alkuperä, 17, 107-19.
- « Erytrious -ominaisuudet, rakenne, toiminnot
- Seriinin ominaisuudet, toiminnot, aineenvaihdunta, ruoka »

