Quiraral Rankic -seos, esimerkkejä
- 4832
- 808
- Ronald Reilly
Eräs Racmic Mix o Racmatics on se, joka koostuu kahdesta enantiomeeristä yhtä suurissa osissa, ja siksi se on optisesti passiivinen. Tämä optinen aktiivisuus viittaa sen ratkaisujen kykyyn kiertää aikataulussa tai antifoliossa, polarisoidun valon säde, joka kulkee niiden läpi suuntaan.
Enantiomeerillä on kyky kiertää polarisoitua valoa, esimerkiksi vasemmalle (Levógiro), joten sen puhdas liuos on optisesti aktiivinen. Kuitenkin, jos tämä alkaa lisätä enantiomeeriä, joka kiertää valoa oikealle (dekstrogia), sen optinen aktiivisuus vähenee, kunnes se on inaktivoitu.
 Rypäleklusterit, joilla on sukulaisuus, jossa on etymologian ulkopuoliset seokset. Lähde: Pexels.
Rypäleklusterit, joilla on sukulaisuus, jossa on etymologian ulkopuoliset seokset. Lähde: Pexels. Kun tämä tapahtuu, sanotaan, että Levogiro- ja Dextrógiro -enantiomeerejä on samat määrät; Jos molekyyli rikkoo polarisoituneen valon vasemmalle, sen vaikutus peruutetaan heti, kun se "kompastuu" toisella molekyylillä, joka pyörii sitä oikealle. Ja niin edelleen. Siksi meillä on rannekerma sekoitus.
Ranskalainen kemisti Louis Pasteur teki ensimmäisen parannuksen havainnon vuonna 1848, joka tutki tartarihappon enantiomeeristen kiteiden seosta (siihen mennessä Rankic Atch -niminen). Kun tämä viinintuotantoon käytettyjen rypäleiden happo.
[TOC]
Kengät ja kiraalisuus
Ensinnäkin on perustelut seosta, on oltava kaksi enantiomeeria (tavallinen), mikä tarkoittaa, että molemmat molekyylit ovat kiraaleja ja että niiden peilikuvat eivät ole päällekkäisiä. Pari kenkiä kuvaa tätä täydellisesti: riippumatta siitä, kuinka paljon vasen kenkiä yritetään oikealla, ne eivät koskaan sovi.
Voi palvella sinua: heikko happoOikea kenkä, sanoen, ohjaa polarisoidun valon vasemmalle; Vaikka vasen kenkä tekee sen oikealle. Hypoteettisessa ratkaisussa, jossa kengät ovat molekyylejä, jos on vain oikeuksien kenkiä, kiraaleja, tämä on optisesti aktiivinen. Samalla tavalla se tapahtuu, jos ratkaisussa on vain jätettyjä kenkiä.
Jos kuitenkin on tuhansia vasemmistokenkiä sekoitettuna tuhansien oikeuksien kengät, siellä on silloin ranskalainen seos, joka on myös optisesti passiivinen, koska sisäpuolella olevan valon kärsimät poikkeamat peruutetaan molemminpuolisesti.
Jos kengän sijasta ne olisivat palloja, esineitä, jotka ovat vesijohtoja, heillä olisi mahdotonta olemassa olevia sekoituksia näistä, koska ne eivät edes pystyisi olemaan enantiomeerisinä pareina.
Esimerkit
Viinihappo
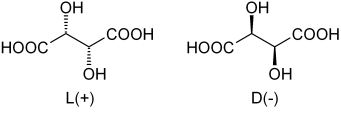 Tartarihappoentimeerit. Lähde: Dschanz [julkinen alue]
Tartarihappoentimeerit. Lähde: Dschanz [julkinen alue] Palattuaan viiniinihappoon, sen rannekinen seos oli ensimmäinen tapaamassa. Yläkuvassa on esitetty sen kaksi enantiomeeriä, joista kukin kykenee muodostamaan kiteitä "vasemman" tai "oikean" morfologisilla kasvoilla. Pasteur, auttamalla mikroskooppia ja tiukkaa ponnistelua, onnistui erottamaan nämä enantiomeeriset kiteet toisistaan.
Enantiomeerien L (+) ja D (-) kiteet ovat erikseen, esittävät optista aktiivisuutta ohjaamalla polarisoitua valoa oikealle tai vasemmalle, vastaavasti. Jos molemmat samoissa molaarisuhteissa olevat kiteet liukenevat veteen, saadaan optisesti inaktiivinen rannek -seos.
Huomaa, että molemmilla enantiomeereillä on kaksi kiraalista hiilihiiliä (neljällä eri substituentilla). L (+): ssä OH on hiilirunko- ja COOH -ryhmien muodostama tason takana; Kun taas D (-) nämä OH ovat mainittua tason yläpuolella.
Ne, jotka syntetisoivat viinihappoa. Enantiomeerin L (+) erottamiseksi d (-) on välttämätön quiraal-resoluutio, jossa tämä seos reagoitiin kiraalisen emäksen kanssa diasteroisomeerisuolojen tuottamiseksi, joka kykenee erottamaan sitten fraktionaalisella kiteytymisellä.
Voi palvella sinua: kuparisulfidi: rakenne, ominaisuudet, käytötKiniini
 Kiniinimolekyylin rakenteellinen luuranko. Lähde: Benjah-BMM27.
Kiniinimolekyylin rakenteellinen luuranko. Lähde: Benjah-BMM27. Edellisessä esimerkissä viitataan viittaus happona (±) -tartaric -tatartaksi. Siten kiniinin (ylivoimainen kuva) tapauksessa se on (±) -Quinina.
Kiniinin isomeria on monimutkainen: siinä on neljä kiraalista hiilyä, mikä aiheuttaa kuusitoista diasteroisomeeriä. Mielenkiintoista on, että kaksi sen enantiomeeria (toinen OH: n kanssa tason yläpuolella ja toinen sen alapuolella), ovat tosiasiallisesti diasthelisomeerejä, koska ne eroavat heidän muiden kiraalisten hiilien kokoonpanoissa (polkupyörän N -atomin kanssa).
Nyt on vaikea määritellä, mitkä kiniinin stereoisomeerit ohjaavat polarisoidun valon oikealle tai vasemmalle.
Talidomidi
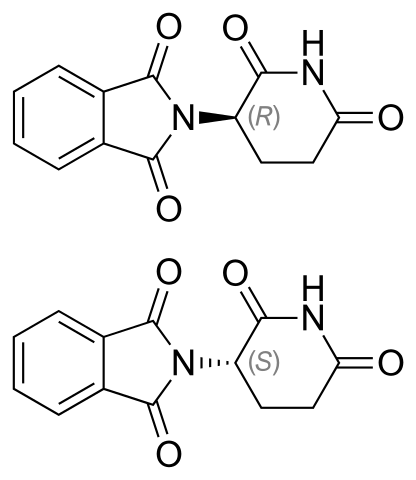 Talaidomidi -enantimeerit. Lähde: Rokotus [julkinen alue]
Talaidomidi -enantimeerit. Lähde: Rokotus [julkinen alue] Talidomidi -enantiomeerit on esitetty yllä. Siinä on vain quiral hiili: sellainen, joka liittyy typeen, joka liittyy molemmille renkaille (yksi ftalimidasta ja toisesta gluteramidista).
Enantiomeerissä R (sedatiivisilla ominaisuuksilla) ftalimida -rengas (vasemmalla) on suunnattu tason yläpuolelle; enantiomeerissä (mutageenisilla ominaisuuksilla), alla.
Prosenttia kahdesta ei tunneta, mikä kahdesta ohjaa valon vasemmalle tai oikealle. Tiedetään, että seos 1: 1 tai 50% molemmista enantiomeereistä muodostaa ranskalaisen seoksen (±) -alidomidin.
Jos haluat markkinoida talidomidia vain hypnoottisena sedatiivisena, on pakollista toimittaa sen rypistyksen seos jo mainittuun kiraaliseen resoluutioon, niin että puhdas enantiomeeri saadaan.
Voi palvella sinua: kvaternääriset yhdisteet: ominaisuudet, koulutus, esimerkit1,2-epoksipropaani
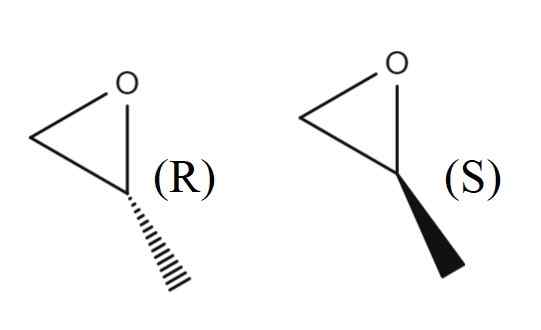 1,2-epoksipropane-enantiomeerit. Lähde: Gabriel Bolívar.
1,2-epoksipropane-enantiomeerit. Lähde: Gabriel Bolívar. Yläkuvassa on 1,2-epoksipropanon enantiomeerien pari. Enantiomeeri r ohjaa polarisoidun valon oikealle, kun taas S ohjaa sen vasemmalle; Eli ensimmäinen on (r)-(+)-1,2-epoksipropano ja toinen (s)-(-)-1,2-epoksipropano.
Niistä kaksi, jälleen, taas 1: 1 tai 50%: n suhteessa, tulee (±) -1,2 -epoksipropaani.
1-fenyylietyyliamiini
 1-penyylietyyliamiinin enantiomeerit. Lähde: Gabriel Bolívar.
1-penyylietyyliamiinin enantiomeerit. Lähde: Gabriel Bolívar. Esitetään toinen ylempi rannekerma-seos, jonka muodostavat 1 feniletyyliamiinin kaksi enantiomeeriä. Enantiomeeri R on (r)-(+)-1-fenyylietyyliamiini ja enantiomeerit S (s)-(-)-1-feniletilamiini; yhdellä on metyyliryhmä, Cho3, osoittaa aromaattisen rengastason ulkopuolelle ja toinen osoittaa tämän alle.
Huomaa, että kun kokoonpano on r, se tapahtuu joskus sen tosiasian kanssa, että enantiómero kiertää polarisoitua valoa oikealle; Sitä ei kuitenkaan aina sovelleta, eikä sitä voida pitää yleisesti.
Lopullinen kommentti
Tärkeämpi kuin Rankic -seosten olemassaolo tai ei. Tämä koskee erityisesti yhdisteitä, joilla on farmakologisia vaikutuksia, jotka riippuvat sellaisesta stereoisomista; Toisin sanoen enantiomeeristä voi olla hyödyllistä potilaalle, kun taas toinen voi vaikuttaa siihen.
Siksi nämä kiraaliset päätöslauselmat turvautuvat niiden komponenttien erillisiin ryntarieoksiin, ja siten pystyy markkinoimaan niitä puhtaina lääkkeinä, jotka eivät ole haitallisia epäpuhtauksia.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. Amiini. (10. painos.-A. Wiley Plus.
- Steven a. Kovettuja. (2017). Orgaanisen kemian kuvitettu sanasto: raseeminen seos. Kemian ja biokemian laitos, UCLA. Palautettu: Chem.UCLA.Edu
- Nancy Devino. (2019). Racemic Seos: Määritelmä ja esimerkki. Opiskelu. Toipunut: Opiskelu.com
- James Ashenhurst. (2019). Stereokemia ja kiraalisuus: Mikä on raseeminen sekoitus? Toipunut: MasterorganicChemistry.com
- John C. Leffingwell. (2003). Kiraalisuus ja bioaktiivisuus I.: Farmakologia. [PDF]. Toipunut: Leffingwell.com

