Oksidoreduktaasien ominaisuudet, rakenne, toiminnot, esimerkit
- 2660
- 810
- Edgar VonRueden
Se oksidoreduktaasit Ne ovat proteiineja, joilla on entsymaattinen aktiivisuus, jotka ovat vastuussa ruosteen vähentämisen reaktioiden katalysoinnista, ts. Reaktiot, jotka tarkoittavat vety- tai elektroniatomien poistamista substraateissa, joihin ne toimivat.
Näiden entsyymien katalysoimat reaktiot, kuten nimestä päätetään, ovat oksidien vähentämisreaktioita, toisin sanoen reaktioita, joissa molekyyli luovuttaa elektroneja tai vetyatomeja ja toinen vastaanottaa ne, muuttaen niiden vastaavia hapettumistiloja.
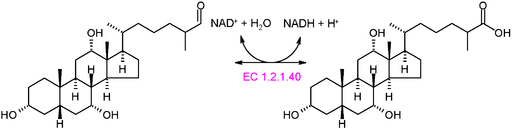 Tyypin ec 1: n oksidortaasin reaktion graafinen kaavio.2.1.40 (lähde: Akane700 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)] Wikimedia Commonsin kautta)
Tyypin ec 1: n oksidortaasin reaktion graafinen kaavio.2.1.40 (lähde: Akane700 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)] Wikimedia Commonsin kautta) Esimerkki luonteeltaan hyvin yleisistä oksidortisten entsyymeistä on dehydrogenaasit ja oksidaasit. Se voidaan mainita alkoholidehydrogenaasin entsyymille, joka katalysoi etanolin dehydrogmenaatiota asetaldehydin tuottamiseksi NAD+ -riippuvaisessa tai käänteisessä reaktiossa, jotta saadaan etanolia alkoholifermentoinnin aikana, jota jotkut kaupallisesti tärkeät heetit ovat suorittaneet alkoholin käymisen aikana.
Aerobisten solujen elektronikuljetinketjun entsyymit ovat protonien pumppauksen oksidortaita.
[TOC]
Yleiset luonteenpiirteet
Oksidoreduktaasientsyymit ovat entsyymejä, jotka katalysoivat yhdisteen hapettumista ja toisen samanaikaisen pelkistyksen.
Nämä yleensä vaativat erityyppisten koentsyymien läsnäolon niiden toimintaan. Koentsyymit täyttävät lahjoittamisen tai hyväksymisen tehtävän.
Nämä koentsyymit voivat olla NAD+/NADH Torus tai FAD/Fadh2 -vääntömomentti. Monissa aerobisissa aineenvaihduntajärjestelmissä nämä elektronit ja vetyatomit siirtyvät lopulta happea koskevista koentsyymeistä.
Ne ovat entsyymejä, joilla on voimakas substraattispesifisyyden "puute", jolloin ne voivat katalysoida ristikorkearktioita erityyppisissä polymeereissä, onko kyse proteiinista tai hiilihydraatteista.
Luokittelu
Näiden entsyymien nimikkeistö ja luokittelu perustuu monta kertaa sekä niiden käyttämään pää substraattiin että heidän toimintaansa tarvittavaan koentsyymiin.
Kansainvälisen biokemian ja molekyylibiologian (NC-IBMB) nimikkeistökomitean suositusten mukaan nämä entsyymit kuuluvat luokkaan E.C. 1 ja sisältää enemmän tai vähemmän 23 eri tyyppiä (E.C.1.1-E.C.1.23), jotka ovat:
Voi palvella sinua: erytropoietiini (EPO): Ominaisuudet, tuotanto, toiminnot- JA.C. 1.1: jotka toimivat avunantajien CH-OH-ryhmissä.
- JA.C. 1.2: jotka toimivat aldehydiryhmässä tai Oxo de los -luovuttajaryhmässä.
- JA.C. 1.3: jotka toimivat CH-CH-ryhmissä avunantajien ryhmissä.
- JA.C. 1.4: jotka toimivat CH-NH2-ryhmissä avunantajaryhmissä.
- JA.C. 1.5: jotka toimivat avunantajien CH-NH-ryhmissä.
- JA.C. 1.6: jotka toimivat Nadhissa tai Nadphissa.
- JA.C. 1.7: jotka vaikuttavat muihin typpiyhdisteisiin, kuten luovuttajiin.
- JA.C. 1.8: jotka toimivat avunantajien rikkiryhmissä.
- JA.C. 1.9: jotka toimivat luovuttajien Hemo -ryhmissä.
- JA.C. 1.10: jotka toimivat luovuttajissa, kuten difenolit ja muut siihen liittyvät aineet.
- JA.C. 1.11: jotka toimivat peroksidissa vastaanottajana.
- JA.C. 1.12: jotka toimivat vedyn kanssa luovuttajana.
- JA.C. 1.13: jotka vaikuttavat yksinkertaisiin luovuttajiin sisällyttämällä molekyylin happea (oksygenaasit).
- JA.C. 1.14: jotka toimivat "pariksi" luovuttajiin, molekyylin hapen sisällyttämisellä tai vähentämisellä.
- JA.C. 1.15: jotka toimivat superoksidien kanssa vastaanottajina.
- JA.C. 1.16: jotka hapettavat metalli -ionit.
- JA.C. 1.17: jotka toimivat CH2 -ryhmissä.
- JA.C. 1.18: jotka vaikuttavat proteiineihin, jotka sisältävät rautaa ja olettavat luovuttajina.
- JA.C. 1.19: jotka vaikuttavat vähentyneen flavodoksiinin luovuttajana.
- JA.C. 1.20: jotka toimivat luovuttajissa, kuten fosfori ja arseeni.
- JA.C. 1.21: jotka toimivat reaktiossa x-h + y-h = x-y.
- JA.C. 1.22: jotka toimivat luovuttajien halogeenissa.
- JA.C. 1.23: jotka vähentävät c-o-c-ryhmiä vastaanottajina.
- JA.C. 1.97: Muut oksidoriaduktaasit.
Jokainen näistä luokista sisältää myös alaryhmät, joissa entsyymit erotetaan substraattien suosimisen mukaan.
Voi palvella sinua: Ensisijainen peräkkäisyys: Ominaisuudet ja esimerkitEsimerkiksi luovuttajiensa CH-OH-ryhmiin vaikuttavien oksidoreduktaasien ryhmässä on joitain, jotka mieluummin NAD+ tai NADP+ -häiriöt, kun taas toiset käyttävät sytokromeja, happea, rikkiä jne.
Rakenne
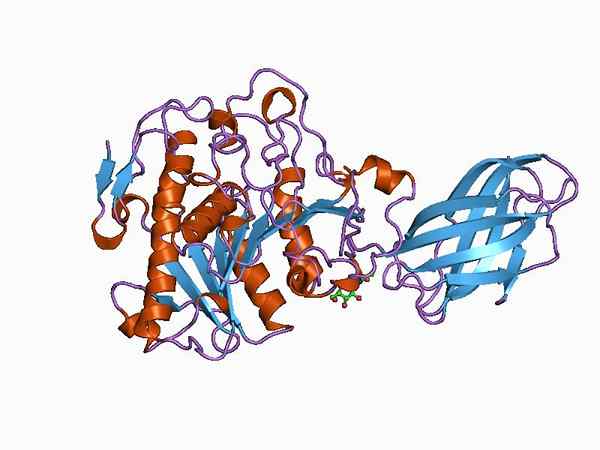
Koska oksidoroitujen taitaasien ryhmä on erittäin monipuolinen, määritellyn rakenteellisen ominaisuuden luominen on melko monimutkaista. Sen rakenne ei vain vaihtele entsyymistä entsyymiin, vaan myös lajien tai elävien olentojen ja jopa solujen välillä soluihin eri kudoksissa.
 Bioinformatics -malli oksduktaasientsyymin rakenteesta (lähde: Jawahar Swaminathan ja MSD: n henkilökunta Euroopan bioinformatiikan instituutissa [julkinen verkkotunnus] Wikimedia Commonsin kautta)
Bioinformatics -malli oksduktaasientsyymin rakenteesta (lähde: Jawahar Swaminathan ja MSD: n henkilökunta Euroopan bioinformatiikan instituutissa [julkinen verkkotunnus] Wikimedia Commonsin kautta) Esimerkiksi entsyymi pyruvaattidehydrogenaasi on kompleksi, joka koostuu kolmesta peräkkäin kytkettystä katalyyttisestä alayksiköstä ja tunnetaan nimellä E1.
Jokainen näistä alayksiköistä puolestaan voidaan koostua useammasta kuin yhdestä samantyyppisestä proteiinimonomeeristä tai erityyppisistä, ts. Ne voivat olla homodimeerisiä (ne, joilla on vain kaksi yhtä suurta monomeeriä), Heterotrimérica (joilla on kolme monomeeriä erilainen) ja niin edelleen.
Se on yleensä entsyymejä, jotka koostuvat eri muodoista järjestetyistä alfa-salista ja β-levytetyistä levyistä, erityyppisten erityyppisten molekyylien välisten vuorovaikutusten kanssa.
Funktiot
Oksidoroidut entsyymit katalysoivat oksidien pelkistysreaktioita käytännössä kaikkien biosfäärin elävien olentojen kaikissa soluissa. Nämä reaktiot ovat yleensä palautuvia, joissa yhden tai useamman atomin hapetustila samassa molekyylissä muuttuu.
Yleensä hapettimet tarvitsevat kahta substraattia, joista toinen toimii vedyn tai elektronien luovuttajana (joka hapettuu) ja toisena, joka toimii vedyn tai elektronien vastaanottajana (joka on vähentynyt).
Nämä entsyymit ovat erittäin tärkeitä monille biologisille prosesseille erityyppisissä soluissa ja organismeissa.
Ne toimivat esimerkiksi melaniinin synteesissä (pigmentti, joka muodostuu ihmisten ihon soluissa), ligniinin (kasvisolujen rakenneyhdiste) muodostumisessa ja hajoamisessa, proteiinien taittaessa jne.
Se voi palvella sinua: Galapagos -saarilla esitetyt lajitNiitä käytetään teollisesti joidenkin elintarvikkeiden tekstuurin modifiointiin, ja esimerkki näistä ovat peroksidaasit, oksidaasiglukoosi ja toiset.
Lisäksi tämän ryhmän merkittävimmät entsyymit ovat ne, jotka osallistuvat elektronisina kuljettajina mitokondriaalikalvon, kloroplastien ja sisäisen bakteerien sisäisen plasmamembraanin kuljettimissa, joissa ne ovat transmembranalproteiineja.
Esimerkkejä oksidortaista
Luonnossa ja teollisuudessa on satoja esimerkkejä oksidoroiduista entsyymeistä. Näillä entsyymeillä, kuten mainittiin, on erittäin tärkeitä funktioita solujen toiminnalle ja siten elämälle sinänsä.
Oksididuktaaaseja eivät sisällä vain peroksidaasientsyymejä, lakkaa, oksidaasiglukoosia tai dehydrogeenista alkoholia; Ne yhdistävät myös tärkeät kompleksit, kuten glyseraldehydi-entsyymi 3-fosfaattidehydrogenaasi tai komplimenus-dehydrogenaasi jne., välttämätön glukoosikabolismin näkökulmasta.
Se sisältää myös kaikki elektronisen kuljetuskompleksin entsyymit sisäisessä mitokondriaalisessa kalvossa tai bakteerien sisäisessä kalvossa, samanlainen kuin jotkut kasvi -organismien kloroplastien entsyymeistä.
Peroksidaasit
Peroksidaasit ovat hyvin monimuotoisia entsyymejä ja käyttävät vetyperoksidia elektronia vastaanottajana monien substraattien, mukaan lukien fenolit, amiinit tai tiolet, hapettumisen katalysointia. Reaktioissaan ne vähentävät vetyperoksidia, kunnes se tuottaa vettä.
Ne ovat erittäin tärkeitä teollisuuden kannalta, koska ne ovat mausteisen retiisin peroksidaasi tärkeimpiä ja kaikkein tutkituimmin.
Biologisesti ottaen peroksidaasit ovat tärkeitä reagenssin happiyhdisteiden poistamiselle, jotka voivat aiheuttaa merkittäviä vaurioita soluille.
Viitteet
- Britannica Encyclopaedia. (2019). Haettu 26. joulukuuta 2019, www.Britannica.com
- Ercili-Cura, D., Hupperz, t., & Kelly, a. Lens. (2015). Maitotuotteen tekstuurin entsymaattinen modifikaatio. Elintarvikkeiden tekstuurin muokkaamisessa (PP. 71-97). Puunjulkaisu.
- Mathews, c. K -k -., Van Holde, K. JA., & Ahern, k. G. (2000). Biokemia. LISÄTÄ. Wesley Longman, San Francisco.
- Nelson, D. Lens., Lehninger, a. Lens., & Cox, M. M. (2008). Lehninger -biokemian periaatteet. Macmillan.
- Kansainvälisen biokemian ja molekyylibiologian kansainvälisen liiton nimikkeistökomitea (NC-IBMB). (2019). Haettu www.Qmul.Ac.UK/SBCS/IUBMB/Entsyymi/Hakemisto.HTML
- Patel, m. S., Nemeria, n. S., Furey, w., & Jordan, f. (2014). Pyruvaattidehydrogenaasikompleksit: rakenne-emäksen toiminta ja säätely. Journal of Biological Chemistry, 289 (24), 16615-16623.

