Analyyttinen kemia

- 3567
- 40
- Louis Moen

Mikä on analyyttinen kemia?
Se analyyttinen kemia Kemian haara on omistettu tutkimaan tai analysoimaan (tästä nimen) koostumuksen koostumusta. Tämä tarkoittaa, että se on vastuussa aineiden tekemisestä, samoin kuin missä osassa sen komponentteja.
Se on puhtaasti kokeellinen kurinalaisuus, joka yhdistää tiedon ja taidot eri alueilta, jotka vaihtelevat tilastoista nykyaikaiseen ja optiseen fysiikkaan analyyttisten menetelmien kehittämiseksi, jotka mahdollistavat riittävän luottamuksen tasolla, mitä näyte sisältää.
Tieteellisen tutkimuksen tärkeyden lisäksi tätä kemian haaraa sovelletaan käytännössä kaikilla teollisuudenaloilla. Tämä johtuu siitä, että se sallii seurannan kemikaalin tai elintarvikkeiden laadusta, ympäristöön ladattavien jätteiden esiintyvien aineiden tasoihin.
Lyhyt analyyttisen kemian historia
Analyyttisen kemian alkuperät voidaan jäljittää Antoine Lavoisierin teoksiin 1800 -luvun lopulla, jotka tekivät tärkeitä tutkimuksia, jotka liittyivät mineraalien ja ilman koostumukseen, samoin kuin palamisen ja eläinten hengitysprosessiin.
 Lavoisier
Lavoisier Kuitenkin vasta 1800 -luvulla, kun Saksan lääketieteellinen oppipoika Carl Freseius Mohr kehitti, mikä olisi ensimmäinen analyyttiset marssit näytteen laadullisen koostumuksen määrittämiseksi. Mohrin julkaisemaa kirjaa pidetään analyyttisen kemian ensimmäisenä tekstinä, ja monia sen periaatteita opetetaan edelleen luokkahuoneessa.
Mohr teki muutakin kuin vain julkaisi löytönsä. Hän keksi myös tilavuustekniikat ja rakensi ja rakensi joitain analyyttisen kemian tärkeimmistä tilavuusanalyysivälineistä, kuten tilavuuspihetteistä ja buretesta.
Lisäksi Frankfurtin laboratoriossaan hän koulutti monia muita oppisopimusopiskelijoita hänen kehittämiinsä tekniikoihin. Kvantitatiivisten tekniikoiden, kuten tilavuus- ja gravimetrian lisäksi, hän opetti myös laadullisia kemiallisia analyysitekniikoita. Tätä ja paljon muuta häntä pidetään analyyttisen kemian isänä.
Analyyttisen kemian haarat
Analyyttinen kemia voidaan jakaa laajoihin iskuihin kahteen luokkaan kemiallisen analyysin tavoitteesta riippuen:
Laadullinen analyyttinen kemia
Ensimmäinen ongelma, jolla pyritään ratkaisemaan analyyttisen kemian, on määrittää, mikä sisältää tuntemattoman näytteen. Eli etsi tai tunnista, mitkä niiden komponentit ovat. Tämän tyyppistä analyysiä kutsutaan laadulliseksi analyysiksi, joten tätä analyyttisen kemian haaraa kutsutaan myös laadulliseksi analyyttisiksi kemiaksi.
Voi palvella sinua: Rauta (elementti): Ominaisuudet, kemiallinen rakenne, käyttöKvantitatiivinen analyyttinen kemia
Tämä analyyttisen kemian haara vastaa siitä, kuinka paljon näytteessä on jokainen komponentti. Toisin sanoen sen tarkoituksena on mitata, mikä määrä, osuus tai pitoisuus ovat eri komponentteja, joita kutsutaan analysointi.
Useimmissa tapauksissa kvantitatiivista analyysiä edeltää aina kvalitatiivinen analyysi, koska ei voida määrittää, kuinka paljon analyyttiä on näytteessä, jos ei tiedetä, mitä analyysejä on samassa.
Siksi, lukuun ottamatta muutamassa tilanteessa, kun se on tiedossa etukäteen, mitä analysoidaan, laadullinen ja kvantitatiivinen analyyttinen kemia menee aina yhdessä.
analyyttiset metodit
Analyyttinen kemia käyttää sekä laadullisia että kvantitatiivisia menetelmiä aineen koostumuksen ymmärtämiseksi:
1. Laadulliset menetelmät
Laadulliset menetelmät perustuvat kemiallisiin reaktioihin, kuten saostumiseen ja kompleksin muodostumiseen, samoin kuin erotustekniikoiden käyttöön näytteen komponenttien tunnistamiseksi. Nämä ovat klassisia menetelmiä ja sisältävät seuraavat esimerkit:
- Kationiset analyyttiset marssit: systemaattinen kemiallisten testien joukko, jotka tunnistavat tiettyjen metallikationien läsnäolon.
- Anioniset analyyttiset marssit: Systemaattinen kemiallisten testien joukko, jotka vahvistavat tiettyjen yleisten anionien läsnäolon.
- Liekin testit: Yksinkertainen analyysi, jonka avulla voit tunnistaa joitain metalleja liekinvärin mukaan, kun näyte poltetaan.
2. Kvantitatiiviset menetelmät
Ne koostuvat lajin pitoisuuden määrittämisestä näytteessä. Analyyttiset menetelmät on yleensä jaettu klassisiin märkätekniikoihin, kuten tilavuus- ja gravimetriaan, sekä nykyaikaiset instrumentaalitekniikat, kuten spektrometriset tekniikat ja kromatografia, jotka selitetään alla:
-
Tilavuusanalyysimenetelmät
 Kemiallinen analyytikko suorittamalla tutkinto
Kemiallinen analyytikko suorittamalla tutkinto Volumetria viittaa tekniikoihin analyytin pitoisuuden epäsuora määritys näytteessä tai saman alikvootissa, joka perustuu tunnettujen pitoisuusreagenssin määrän mittauksen mittaamiseen, joka on välttämätöntä analyytin stoikiometrisesti. Näitä tekniikoita kutsutaan myös asteiksi tai arvoiksi.
Voi palvella sinua: OxácidoKaikki tilavuusmenetelmät perustuvat ekvivalenssipisteen löytämiseen, jossa on täytettävä, että:
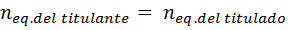
Koska ekvivalentit ovat yhtä suuret kuin normaali pitoisuus tilavuudella, ja nimikkeen pitoisuus tunnetaan, sen tilavuuden mittaaminen merkitsee sitä, että titlerin ekvivalenttien lukumäärä tunnetaan, ja siksi analyytin tai otsikon, kuten esitetään, kuten esitetään Jatkamiseen:
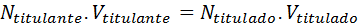
Volumetriin perustuu monia analyyttisiä menetelmiä, jotka eroavat niiden käyttämän kemiallisen reaktion tyypin mukaan. Tästä riippuen voidaan erottaa seuraavat tilavuusmenetelmät:
-
- Happo-emäksinen tilavuus: Näissä tapauksissa joko analyytti on happo ja otsikko A -emäs tai päinvastoin. Reaktio on happo-emäs neutralointi ja asteen päätepiste määritetään kemiallisen indikaattorin värinmuutoksella.
- Sademäärä Volumetria: Tässä tekniikassa reaktio on liukenemattoman sakan muodostuminen.
- Kompleksin muodostumisen arviointi tai tilavuus: Tässä tapauksessa reaktio on metallikompleksin muodostuminen, joskus värillinen, joskus ei.
- Redox -tilavuus: Se viittaa tilavuuteen, joka merkitsee hapettumista ja pelkistysreaktiota nimellisen ja analyytin välillä. Yksi on hapettavan aineen ja toisen pelkistimen rooli.
-
Gravimetriset analyysimenetelmät
 Gravimetrisessä analyysissä käytetyt analyyttiset asteikot
Gravimetrisessä analyysissä käytetyt analyyttiset asteikot Toisin kuin edellisessä tapauksessa, nämä menetelmät perustuvat massan mittaamiseen tai näytteen massamuutokseen sen jälkeen, kun niille on tehty erityyppisiä kemiallisia ja lämpökäsittelyjä.
Joitakin esimerkkejä analyyttisen kemian laboratorion yleisistä gravimetrisistä menetelmistä ovat:
-
- Sademenetelmät: Näissä tapauksissa analyytti on yleensä ioni, joka saostuu kvantitatiivisesti liukenemattoman suolan muodossa. Sanoi suolasuodattimet ja kuivua ja määritä sitten sen massa. Tällä massalla määritetään sitten analyytin määrä alkuperäisessä näytteessä.
- Haihtumismenetelmät: Toisin kuin edellinen, analyytti on tässä tapauksessa erotettu näytteen matriisista kaasun muodossa. Joissakin menetelmissä tämä kaasu kerätään reagoimalla riittävän reagenssin kanssa ja punnitsemalla sitten mainitun reaktion tuote. Toisissa kaasun massa määritetään painon erolla ennen ja jälkeen haihtumisen.
- Elektrodepositio: Se on samanlainen kuin saostumismenetelmät, paitsi että analyytti on kerrostettu elektrodiin sähkövirran tuottaman redox -reaktion takia. Elektrodimassan kasvu mahdollistaa analyytin määrän määrittämisen näytteessä.
-
Instrumentaalimenetelmät
 Automaattinen analyyttinen instrumentti
Automaattinen analyyttinen instrumentti Nykyaikaiset analyyttiset menetelmät perustuvat enimmäkseen edistyneiden tieteellisten instrumenttien käyttöön, jotka kykenevät analysoimaan monimutkaisia näytteitä tehokkaasti, tarkasti ja joissain tapauksissa automatisoituneet. Nämä menetelmät perustuvat jonkin fysikaalisen ominaisuuden mittaamiseen, joka voidaan korreloida analyytin pitoisuuden kanssa näytteessä.
Voi palvella sinua: alkali metallit: fysikaaliset ja kemialliset ominaisuudet, käyttö, hankkiminenJotkut tekniikat mittaavat eroja sähköpotentiaalissa tai virran intensiteetissä, kun taas toiset mittaavat atomien tai molekyylien lähettämän tai absorboivan valon määrän tietyillä aallonpituuksilla. Joitakin esimerkkejä instrumentaalisista analyyttisistä menetelmistä ovat:
-
- Spektrometriset menetelmät: Nämä menetelmät perustuvat atomien ja molekyylien valon imeytymisilmiöön tai valon säteilyyn, kun atomit lämmitetään korkeissa lämpötiloissa. Ensimmäisessä tapauksessa tekniikoita kutsutaan absorptiospektrometriaksi (atomi- tai molekyylien tapaus) ja toisessa niitä kutsutaan atomiemissiospektrometriaksi.
- Elektroanalyyttiset menetelmät: Toisin kuin aikaisemmat, nämä mittaavat sähkön muutokset tai näytteen sähköominaisuudet analyytin läsnä ollessa. Tämä sisältää virran voimakkuuden mittaukset (kuten polarografian tapauksessa), jännite (kuten ph-menetelmien tapauksessa), sähkönjohtavuus jne.
-
Kromatografiset menetelmät
Kromatografiaa voidaan pitää luokkana erillisen analyyttisen menetelmän lisäksi, koska se sisältää erottelun, laadullisen tunnistamisen ja kvantifioinnin kaikki yhdessä. Nämä menetelmät voidaan yhdistää tilavuus- tai instrumentaalitekniikoihin erillisten analyyttien analysoimiseksi.
Tässä tekniikassa monimutkainen näyte liukenee riittävään liuottimeen ja virtaa huokoisen materiaalin, kuten geelin, suodatinpaperin tai hienon hiekan läpi, työntämällä sama liuotin.
Näytteessä olevilla eri liuenneilla aineilla on erilaiset affiniteetit huokoisesta materiaalista, joten jotkut liikkuvat sen läpi nopeammin kuin toiset. Loppujen lopuksi fraktiot, jotka lähtevät analyysiin.

