Atomiradio
- 2943
- 200
- Gustavo Runte DVM
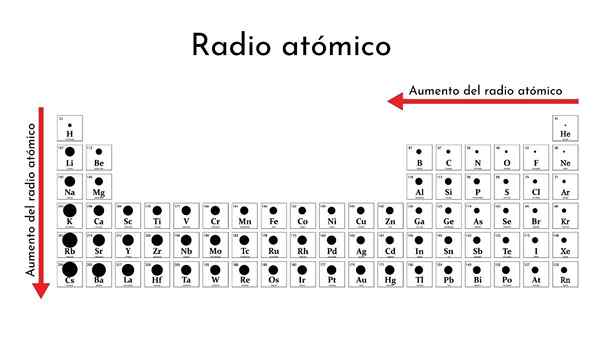
 Elementtien jaksollinen taulukko atomiradioilla
Elementtien jaksollinen taulukko atomiradioilla Mikä on atomiradio?
Hän atomiradio Se on tärkeä parametri jaksollisen taulukon elementtien jaksollisille ominaisuuksille. Se liittyy suoraan atomien kokoon, koska suurempi radio, suurempi tai iso. Samoin se liittyy saman elektronisiin ominaisuuksiin.
Vaikka atomilla on enemmän elektroneja, sitä suurempi sen atomiskoko ja radio. Molemmat määrittelevät Valencia -kerroksen elektronit, koska niiden kiertoratojen ulkopuolella olevilla etäisyyksillä elektronin löytämisen todennäköisyys lähestyy nollaan. Päinvastoin tapahtuu ytimen läheisyydessä: elektronin löytämisen todennäköisyys lisääntyy.
 Puuvillapallopakkaus. Tapa, jolla he tiivistetään
Puuvillapallopakkaus. Tapa, jolla he tiivistetään Yläkuva edustaa puuvillapallopakkausta. Huomaa, että jokaista ympäröi kuusi naapuria, lukuun ottamatta toista mahdollista tai alhaisempaa riviä. Tapa, jolla puuvillapallot tiivistetään, määrittelee koonsa ja siten niiden radiot; Kuten atomien kanssa.
Kemiallisen luonteensa mukaan olevat elementit ovat vuorovaikutuksessa omien atomiensa kanssa tavalla tai toisella. Siksi atomisäteen suuruus vaihtelee läsnä olevan sidoksen tyypin ja sen atomien kiinteän pakkauksen mukaan.
Kuinka atomisäde mitataan?
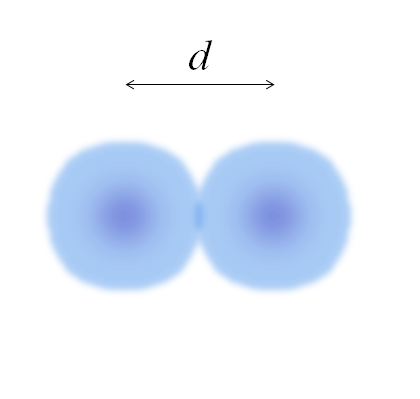 Kuva kahdesta atomista, joiden reunoja ei ole täysin määritelty. Lähde: Gabriel Bolívar
Kuva kahdesta atomista, joiden reunoja ei ole täysin määritelty. Lähde: Gabriel Bolívar Edellisessä kuvassa se voi olla yksinkertainen. Atomin palloa ei kuitenkaan ole täysin määritelty. Koska? Koska elektronit kiertävät ja hämärtyvät avaruuden betonialueilla: kiertoradat.
Siksi atomia voidaan pitää pallona, jolla on impalpable reunat, joita on mahdotonta sanoa varmasti, mihin ne päättyvät. Esimerkiksi ylemmässä kuvassa ytimen lähellä sijaitsevan keskuksen alue näyttää voimakkaammalta väriltä, kun taas sen reunat ovat hämärtyneet.
Voi palvella sinua: SolvaatioKuva edustaa diatomista molekyyliä ja2 (Kuten CL2, H2, JOMPIKUMPI2, jne.-A. Olettaen, että atomit ovat pallomaisia kappaleita, jos etäisyys määritettiin d -d Se erottaa molemmat ytimet kovalenttisessa linkissä, se riittää sitten jakaa se kahteen puolikkaaseen (d -d/2) atomisäteen saamiseksi; Tarkemmin sanottuna E: n kovalenttinen säde E: lle2.
Entä jos E ei muodostanut kovalenttisia sidoksia itsensä kanssa, mutta se oli metallinen elementti? Niin d -d Se osoittaisi niiden metallirakenteessa E -ympäröivien naapureiden lukumäärä; toisin sanoen koordinaationumerolla (n.C) pakkauksen sisällä olevan atomin (muista kuvan puuvillapallot).
Sisäisen etäisyyden määrittäminen
Määrittämiseksi d -d, joka on molekyylin tai pakkauksen kahden atomin sisäinen etäisyys, tarvitaan fysikaalisia analyysitekniikoita.
Yksi eniten käytetyistä on X -ray -diffraktio. Se säteilee valonsäteen lasin läpi, ja elektronien ja sähkömagneettisen säteilyn vuorovaikutuksista johtuvaa diffraktiokuviota tutkitaan.
Pakkauksesta riippuen voidaan saada erilaisia diffraktiokuvioita ja siten muita arvoja d -d.
Jos atomit ovat "tiukkoja" kiteisessä verkossa, ne esittävät erilaisia arvoja d -d verrattuna niihin, jotka olisivat, jos he olisivat "mukavia".
Samoin nämä sisäiset etäisyydet voivat vaihdella arvoista, joten atomisäde todella koostuu tällaisten mittausten keskimääräisestä arvosta.
Kuinka atomisäde ja koordinaationumero liittyvät? V. Goldschmidt loi kahden välisen suhteen, jossa n.C 12, suhteellinen arvo on 1; 0.97 pakkaukselle, jossa atomilla on n.C yhtä suuri kuin 8; 0.96, N: lle.C yhtä suuri kuin 6; ja 0.88 N: lle.C 4.
Voi palvella sinua: natriumpermanganaatti (namno4): ominaisuudet, riskitYksiköt
N: n arvoista.C Vastaa 12, monet taulukoista on rakennettu, missä verrataan kaikkien jaksollisen taulukon kaikkien elementtien atomiradioita.
Koska kaikki elementit eivät muodosta tällaisia kompakteja rakenteita (n.C alle 12), V -suhdetta käytetään. Goldschmidt laskemaan atomiradiot ja ilmaisemaan ne samasta pakkauksesta. Tällä tavoin atomiradioiden mittaukset standardisoidaan.
Mutta mitä yksiköitä ilmaistaan? Kun otetaan huomioon d -d Se on hyvin pieni, angstrom Å: n yksiköt (10 ∙ 10-10m) tai myös laajasti, pikometri (10 ∙ 10-12m).
Kuinka vaihdat jaksollisessa taulukossa?
Aikana
Metallielementeille määritettyjä atomiradioita kutsutaan metalliradioiksi, kun taas niille ei -metallisille elementeille, kovalenttisille radioille (kuten fosfori, p4, tai rikki, s8-A. Molempien radiotyyppien välillä on kuitenkin näkyvämpi ero kuin nimi.
Vasemmalta oikealle samalla ajanjaksolla, ydin lisää protoneja ja elektroneja, mutta jälkimmäiset rajoittuvat samaan energiatasoon (pääkvanttiluku).
Seurauksena on, että ytimessä on kasvava tehokas ydinkuorma valenssielektroneihin, mikä supistuu atomisädettä.
Tällä tavoin ei -metallisilla elementeillä samalla ajanjaksolla on yleensä pienempi atomi (kovalenttinen) radiot.
Ryhmän laskeva
Kun ryhmä laskeutuu, uusia energiatasoja on mahdollista, joiden avulla elektronit voivat olla enemmän tilaa. Siten elektroninen pilvi kattaa suuremmat etäisyydet, sen epäselvä reuna päättyy enemmän ytimestä, ja siksi atomisäde laajenee.
Voi palvella sinua: HydroksyyliryhmäLantanide -supistuminen
Sisäkerroksen elektronit auttavat loistamaan tehokkaan ydinkuorman valenssielektroneihin. Kun sisäisten kerrosten muodostavilla orbitaaleilla on monia ”onteloja” (solmut), kuten F -orbitaalien kanssa, ydin supistuu voimakkaasti atomissädeltä johtuen niiden huonosta kilpivaikutuksesta.
Tämä tosiasia käy ilmi lantanidin supistuksessa jaksollisen taulukon 6. ajanjaksolla 6. HF: stä Orbitaalien F atomi -sädetuote on huomattava supistuminen, jotka ”täytetään” lohko F: Lantanoidien ja aktinoidien ajan kulkevat.
Samanlainen vaikutus voidaan havaita myös jakson 4 lohkon P elementeillä. Tällä kertaa tuote D -kiertoradan heikoista suojausvaikutuksesta, jotka täytetään kuluttamalla siirtymämetallien ajanjaksoja.
Atomiradioesimerkkejä
Määräaikaisen taulukon jaksolle sen elementtien atomiradiot ovat:
-Li: 257 PM
-Ole: klo 232
-B: 88 PM
-C: 77 PM
-N: 74 PM
-O: 186 PM
-F: 184 PM
Huomaa, että litiummetallilla on suurin atomisäde (257 PM), kun taas fluori, joka sijaitsee ajanjakson oikeassa päässä, on pienin niistä kaikista (klo 184). Atomisäde laskeutuu vasemmalta oikealle samalla ajanjaksolla, ja listausarvot osoittavat sen.
Litium, muodostamalla metallisidokset, sen säde on metallinen; ja fluori, muodossa kovalenttisia sidoksia (F-F), sen säde on kovalenttinen.
Entä jos haluat ilmaista atomisradioita Angstrom -yksiköissä? Riittää jakamaan ne 100: lla: (257/100) = 2.57å. Ja niin edelleen muiden arvojen kanssa.
Viitteet
- Kemia 301. Atomisradi. Toipunut: CH301.cm.UTEXAS.Edu
- CK-12-säätiö (2016). Atomisäde. Palautettu: Chem.Librettexts.org
- Atomisteiden trendit. Otettu: Intro.Kemia.OKSTATE.Edu
- Clackamas Community College (2002). Atomiskoko. Haettu osoitteesta: DL.clackamat.Edu
- Clark j. (2012). Atomi- ja ioninen säde. Talteenotettu: Chemguide.yhteistyö.Yhdistynyt kuningaskunta
- Shiver & Atkins. (2008). Epäorgaaninen kemia (neljäs painos, s. 23, 24, 80, 169). MC Graw Hill.

