Kuparisulfaattirakenne (CUSO4) rakenne, ominaisuudet, hankkiminen, käyttö
- 1790
- 288
- Dr. Travis Reichert
Hän kuparisulfaatti Se on epäorgaaninen yhdiste, jonka on muodostanut kuparin (Cu), rikki (S) ja happi (O) -elementit (O). Sen kemiallinen kaava on cuso4. Kupari on hapetustilassa +2, rikki +6 ja happea on Valencia -2.
Se on valkoinen kiinteä kiinteä, että kun se altistuu ympäristön kosteudelle, tulee sen cuso -sininen pennatydraatti4 •5H2JOMPIKUMPI. Valkoinen kiinteä aine saadaan kuumentamalla sinistä veden poistamiseksi.
 Kuparisulfaatti (CuO4) vedetön (ilman vettä sen kiteisessä rakenteessa). W -. OELEN/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons.
Kuparisulfaatti (CuO4) vedetön (ilman vettä sen kiteisessä rakenteessa). W -. OELEN/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons. Sitä on käytetty antibakteerisena aineena vuosisatojen ajan ihmisten ja eläinten haavojen parantamiseksi. Se toimii myös sienitautien torjunta -aineena, eläimissä. Sitä käytetään myös antihongos -aineena kasveissa.
Jotkut niiden käytöstä on kuitenkin lopetettu, koska niiden ylimääräinen voi olla myrkyllistä sekä ihmisille, eläimille ja kasveille. Pitoisuusväli, jossa sitä voidaan käyttää, on kapea ja riippuu lajista.
Sitä käytetään katalysaattorina kemiallisissa reaktioissa ja liuottimina. Se mahdollistaa joidenkin polymeerien vastustuskyvyn ja joustavuuden parantamisen.
Liialliset määrät tätä yhdistettä voivat olla haitallisia maaperille, koska se on myrkyllinen kasveille hyödyllisille mikro -organismeille.
[TOC]
Rakenne
Kuparisulfaatti muodostuu kuparioni (Cu2+) ja sulfaatti -ioni (niin42--A.
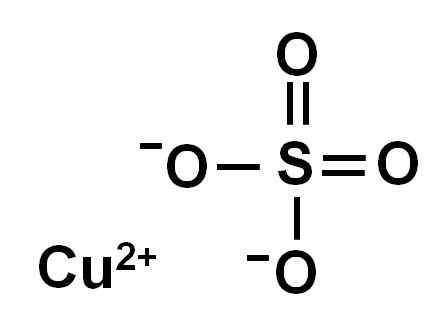 Ionica -kuparisulfaatti (II). Kirjoittaja: Marilú Stea.
Ionica -kuparisulfaatti (II). Kirjoittaja: Marilú Stea. Kahden elektronin menetyksen vuoksi kuparioni (II) on seuraava elektroninen konformaatio:
1s2 2s2 2 p6 3s2 3P6 3D9
Voidaan nähdä, että kiertoradalla on 3D epätäydellinen (siinä on 9 elektronia 10: n sijasta).
Nimikkeistö
- Vedetön kuparisulfaatti
- Kuparisulfaatti (II)
- Kupli -sulfaatti
Ominaisuudet
Fyysinen tila
Vihertävä valkoinen kiinteä tai kidekuulainen.
Molekyylipaino
159,61 g/mol
Sulamispiste
Nopeudella 560 ºC se hajoaa.
Tiheys
3,60 g/cm3
Liukoisuus
22 g/100 g vettä 25 ° C: ssa. Liukenematon etanoliin.
Kemialliset ominaisuudet
Kun se altistetaan ilman kosteutta alle 30 ° C4 •5H2JOMPIKUMPI.
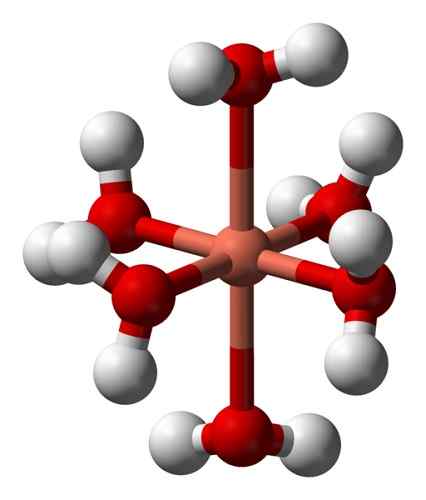
Sen vesiliuokset ovat sinisiä johtuen heksacuocobre -ionin (II) muodostumisesta [Cu (H2JOMPIKUMPI)6-2+ joka tuottaa tällaista väriä. Tässä ionissa kaksi vesimolekyyliä on kauempana metallisesta atomista kuin muut neljä.
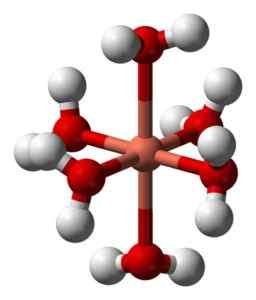 Hexaacuocobre -ionin (II) muodonmuutos rakenne [CU (H2JOMPIKUMPI)6-2+. Benjah-BMM27 / julkinen verkkotunnus. Lähde: Wikimedia Commons.
Hexaacuocobre -ionin (II) muodonmuutos rakenne [CU (H2JOMPIKUMPI)6-2+. Benjah-BMM27 / julkinen verkkotunnus. Lähde: Wikimedia Commons. Tämä johtuu ns. Jahn-Teller -vaikutuksesta, joka ennustaa, että tämäntyyppiset järjestelmät kokevat vääristymisen, joka johtuu siitä, että Cu2+ Sillä on elektroninen rakenne, joka päättyy D9, eli epätäydellinen kiertorata (se olisi täydellinen, jos se olisi D10-A.
Voi palvella sinua: kalsiumhydroksidi (CA (OH) 2): rakenne, ominaisuudet, hankkiminen, käyttöJos ammoniakkia lisätään (NH3) Nämä ratkaisut muodostuvat, joissa NH3 Vesimolekyylit ovat peräkkäin syrjäyttäviä. Ne muodostetaan esimerkiksi [Cu (NH3) (H2JOMPIKUMPI)5-2+ Kunnes [Cu (NH3-A4(H2JOMPIKUMPI)2-2+.
Kun cuso4 Se lämmitetään hajoamiseensa, säteilee myrkyllisiä kaasuja ja muuttuu kuplioksidiksi.
Saada
Vedetön kuparisulfaatti voidaan saada pentahydraattiyhdisteen kokonaiskuivauksella, joka saavutetaan kuumentamalla sitä, kunnes vesimolekyylit haihtuvat.
Cuso4 •5H2O + lämpö → cuo4 + 5 h2Tai ↑
Pentahydraattiyhdiste on sininen, joten cuso -vesi saadaan kadotettaessa kiteytysvettä4 Valkoinen.
Sovellukset
Jotkut sen käytöistä ovat päällekkäisiä pentahydraattiyhdisteen kanssa. Toiset ovat erityisiä vedettömälle aineelle.
Antibakteerisena aineena
Sillä on potentiaalia antimikrobisena aineena. Sitä on käytetty tuhansia vuosia, jopa Etelä -Amerikan ja Keski -Amerikan kulttuureissa, haavan tartunnan estämiseksi tämän yhdisteen liuoksessa kyllästetyn sideharjan kautta.
On arvioitu, että sen antibakteerisen aktiivisuuden mekanismissa ionit cu2+ Ne muodostavat kelaatit entsyymeillä, jotka ovat ratkaisevia bakteerien solutoiminnoille, deaktivoivat ne. Ne indusoivat myös hydroksyyliradikaalien muodostumisen OH •, jotka vahingoittavat bakteerikalvoja ja niiden DNA: ta.
 Cuso4 Se voi toimia joitain patogeenisiä bakteereja vastaan. Kirjoittaja: Gerd Altmann. Lähde: Pixabay.
Cuso4 Se voi toimia joitain patogeenisiä bakteereja vastaan. Kirjoittaja: Gerd Altmann. Lähde: Pixabay. Viime aikoina on ilmoitettu, että cuso -jäljet4 Ne voivat lisätä polyfenoleissa runsaasti luonnontuotteita, kuten jonkin tyyppisiä teekasvien infuusioita.
Eläinlääketieteellisissä sovelluksissa
Sitä käytetään antiseptisenä ja supistavana limakalvojen kohdalla sekä ulkoisen konjunktiviitin ja otiitin hoitoon. Sen tarkoituksena on suorittaa terapeuttisia tai ennaltaehkäisuja kylpyjä karjan, lampaiden ja muiden nisäkkäiden mädäntymisen välttämiseksi.
 CuO -vesiliuokset4 He palvelevat karjan reikiä. Kirjailijat: Ingrid und Stefan Melichar. Lähde: Pixabay.
CuO -vesiliuokset4 He palvelevat karjan reikiä. Kirjailijat: Ingrid und Stefan Melichar. Lähde: Pixabay. Se toimii kaustisena aineena nekroottisissa massoissa nautakarjan, stomatiitin haavaumien ja näiden rakeistetun kudoksen raajoissa. Sillä on käytetty sienien aiheuttamien väriaineiden ja sairauksien hoidossa sienitautien torjunta -aineena.
Sitä käytetään myös Eméticona (agentti oksennuksen provosoimiseksi) sioissa, koirissa ja kissoissa; Antidiarrhealina supistavana vasikoihin ja suoliston moniliaaseen hallitsemiseksi siipikarjassa ja Turkki -trichomoniaasissa.
Eläinten rehujen lisäyksenä
Kuparisulfaattia on käytetty lisäaineena hyvin pieninä määrinä nautojen, sikojen ja siipikarjan ruokintaan. Sen tarkoituksena on hoitamaan kuparin puutosta märehtijöissä. Sikojen ja lintujen tapauksessa sitä käytetään kasvun stimulanttina.
Voi palvella sinua: kromatogrammiKupari on tunnistettu välttämättömäksi hemoglobiinin biosynteesille nisäkkäissä, sydän- ja verisuonirakenne, luun kollageenin synteesi, entsyymijärjestelmät ja lisääntyminen.
Kuten edellisessä osassa mainittiin, se voidaan toimittaa myös lääkityksenä tautien torjuntaa varten. Lisäys- ja/tai lääkitystasot on kuitenkin tarkkailtava huolellisesti.
 Ylimääräinen kuparisulfaatti voi vaikuttaa korjaaviin lintuihin ja niiden muniin. Kirjoittaja: Pexels. Lähde: Pixabay.
Ylimääräinen kuparisulfaatti voi vaikuttaa korjaaviin lintuihin ja niiden muniin. Kirjoittaja: Pexels. Lähde: Pixabay. Tietystä määrästä, joka riippuu kustakin lajista, voi tapahtua kasvun, ruokahalun menetyksen ja painon vähentymisen, tiettyjen elinten vauriot ja jopa eläinten kuolema.
Esimerkiksi kanoilla täydentäminen 0,2% tai enemmän vähenee näiden ruoan nauttimista siitä, kun seurauksena on painonpudotus, vähentynyt munantuotanto ja niiden kuorien paksuus.
Maatalouden sovelluksissa
Orgaanisissa tuotantojärjestelmissä ei ole sallittua käyttää synteettisiä sienitautien torjunta -aineita, vain kupari- ja rikkituotteet hyväksytään, kuten kuparisulfaatti.
Esimerkiksi tietyt sienet, jotka hyökkäävät Apple -kasveja, kuten Venturia inaequalis, poistetaan tällä yhdisteellä. Ajatellaan, että mahdollisesti ionit cu2+ He voivat päästä sienen itiöön, denaturalisoida proteiineja ja estää useita entsyymejä.
 Kuparisulfaatti palvelee joitain sieniä, jotka hyökkäävät omenoita. Algiras LT: llä.Wikipedia / julkinen alue. Lähde: Wikimedia Commons.
Kuparisulfaatti palvelee joitain sieniä, jotka hyökkäävät omenoita. Algiras LT: llä.Wikipedia / julkinen alue. Lähde: Wikimedia Commons. Kuparin merkitys kasveissa
Kuparielementti on tärkeä kasvien fysiologisissa prosesseissa, kuten fotosynteesi, hengitys ja puolustus antioksidantteja vastaan. Sekä tämän elementin puute että sen ylimäärä tuottavat reaktiivisia hapetettuja lajeja, jotka ovat haitallisia näiden molekyyleille ja rakenteille.
Kuparipitoisuusväli kasvien optimaaliseen kasvuun ja kehitykseen on hyvin kapea.
Haitalliset vaikutukset maatalouteen
Kun tätä tuotetta käytetään liikaa maatalouden toiminnassa, se voi olla fytotoksinen, aiheuttaa ennenaikaisia hedelmien kehitystä ja muuttaa sen väriä.
Lisäksi kupari kertyy maahan ja on myrkyllinen mikro -organismeille ja lieroille. Tämä ristiriidassa orgaanisen maatalouden käsitteen.
 Vaikka cuso4 Sitä käytetään orgaanisessa maataloudessa voi olla haitallista maanmatoja varten. Kirjoittaja: Patricia Maine Degrave. Lähde: Pixabay.
Vaikka cuso4 Sitä käytetään orgaanisessa maataloudessa voi olla haitallista maanmatoja varten. Kirjoittaja: Patricia Maine Degrave. Lähde: Pixabay. Kemiallisissa reaktioissa
Cuso4 Vedetön toimii katalysaattorina monille karbonyyliorgaanisten yhdisteiden reaktioille, joilla on diolit tai niiden epoksidit, muodostaen dioksolaanit tai asetonidit. Tämän yhdisteen ansiosta reaktiot voidaan tehdä pehmeissä olosuhteissa.
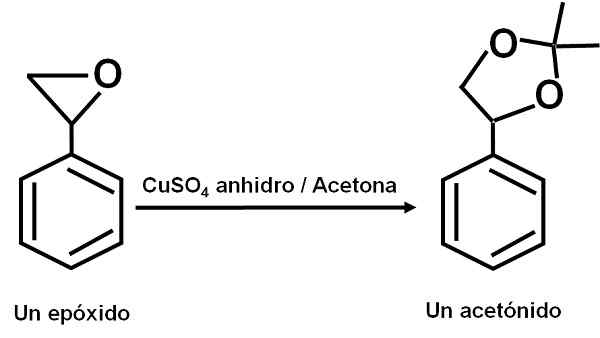 Esimerkki reaktiosta, jossa cuso4 Vedetön toimii katalysaattorina. Kirjoittaja: Marilú Stea.
Esimerkki reaktiosta, jossa cuso4 Vedetön toimii katalysaattorina. Kirjoittaja: Marilú Stea. On myös raportoitu, että sen katalyyttinen toiminta sallii dehydraattien sekundaarisen, tertiäärisen, bentsyyli- ja alilic -alkoholin kuivumisen vastaaviin olefiineihin. Reaktio tehdään hyvin yksinkertaisella tavalla.
Voi palvella sinua: anetolPuhdas alkoholi lämmitetään yhdessä cuson kanssa4 Vedetön lämpötilassa 100-160 ° C aikaan 0,5-1,5 tuntia. Siten esiintyy alkoholin ja olefiinin kuivumista, puhtaat tislat reaktioseoksesta.
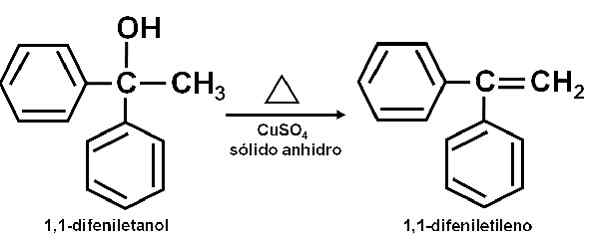 Alkoholin kuivuminen kuparisulfaatille (II) vedetön. Kirjoittaja: Marilú Stea.
Alkoholin kuivuminen kuparisulfaatille (II) vedetön. Kirjoittaja: Marilú Stea. Kuivausaineena
Tätä yhdistettä käytetään kemian laboratorioissa kuivausaineena. Se kuivuttaa orgaanisia nesteitä, kuten liuottimia. Imeä vettä, joka muodostaa cuo -pentahydraattiyhdisteen4 •5H2JOMPIKUMPI.
 Kun cuso4 Valkoisesta anhydro absorboi vettä4.5H2JOMPIKUMPI. Crystal Titan/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons.
Kun cuso4 Valkoisesta anhydro absorboi vettä4.5H2JOMPIKUMPI. Crystal Titan/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons. Polymeerien parantamiseksi
Cuso4 Anhydroa on käytetty parantamaan tiettyjen polymeerien ominaisuuksia ja sallimaan niiden olevan kierrätettävä.
Esimerkiksi asetonilaitteen hiukkaset on sekoitettu akryylinitriili-butadieenikumin kanssa erityisessä myllyssä yrittäen tehdä cuso-hiukkasia4 Olla hyvin pieni.
Kuparisulfaatti parantaa polymeeriliittopisteitä, jotka muodostavat seoksen, jolla on korkea vastus, kovuus ja yllättävä joustavuus.
Lopetetuissa terapeuttisissa sovelluksissa
Aikaisemmin käytettiin kuparisulfaattiliuoksia mahalaukun pesuun, kun joku kärsi valkoisesta fosforimyrkytyksestä. Liuos sekoitettiin kuitenkin nopeasti kuparimyrkytyksen välttämiseksi.
Tämän yhdisteen liuoksia käytettiin myös yhdessä muiden aineiden kanssa ihon ajankohtaisiin palovammoihin fosforilla.
Joskus he palvelivat tietyissä ravitsemusmuodoissa.
Tietyt ekseema-, impetigo- ja intertrigo -voiteet sisälsivät CuO: ta4. Ratkaisuja käytettiin supistavana silmäinfektioissa. Joskus kiteitä levitettiin suoraan palovammoihin.
Kaikkia näitä sovelluksia ei enää tehdä myrkyllisyyden vuoksi, joka voi indusoida ylimääräistä yhdistettä.
Viitteet
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Kuparisulfaatti. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Lyijy, d.R -. (Toimittaja) (2003). CRC: n kemian ja fysiikan käsikirja. 85th CRC -lehdistö.
- Montag, J. et al. (2006). In vitro -tutkimus jstk Venturia inaequalis. J -. Maatalous-. Elintarvikekemia. 2006, 54, 893-899. Linkki palautettu.Jousto.com.
- Holloway, a.C. et al. (2011). Koko ja subfraktioidun valkoisen teen antimikrobisten aktiivisuuksien parantaminen kuparin (II) sulfaatin ja C-vitamiinin riippuvuudella Staphylococcus aureus; Mekaaniseen lähestymistapaan. BMC Complement Altern Med 11, 115 (2011). Haettu BMCComplementMedTherapies.biolääketieteellinen.com.
- Sanz, a. et al. (2018). Kuparin imeytymismekanismi Thalian Arabidopsis Korkeanrvoisuus Copt -kuljettajat. Protoplasma 256, 161-170 (2019). Linkki palautettu.Jousto.com.
- Griminger, P. (1977). Kuparisulfaatin vaikutus munan tuotantoon ja kuoren paksuuteen. Siipikarjan tiede 56: 359-351, 1977. Toipunut akateemisesta.Oppi.com.
- Hanzlik, r.P. Ja Leinwetter, M. (1978). Epoksidien ja karbonyyliyhdisteiden reaktio, jota katalysoivat vedettömän kuparisulfaatin avulla. J -. Org. Kemia., Osa.43, ei.3, 1978. Pubista toipunut.ACS.org.
- Okonkwo, a.C. et al. (1979). Kuparivaatimus puhdistettua ruokavaliota ruokituista sikoista. The Journal of Nutrition, osa 109, numero 6, kesäkuu 1979, sivut 939-948. Toipunut akateemisesta.Oppi.com.
- Hoffman, R.V. et al. (1979). Vedetön kupari (II) Sulfaatti: Efficicieen. J -. Org. Kemia., 1980, 45, 917-919. Pubista toipunut.ACS.org.
- Shao, c. et al. (2018). Akryylitriili-butadieenikumin/vedettömien kuparisulfaattikomposiittien parannettu vetolujuus koordinaatiolla, joka on valmistettu silloittamalla. Polymio. Sonni. 76, 1435-1452 (2019). Linkki palautettu.Jousto.com.
- Vedonlyönti, j.W -. et al. (2018). Uudet antibakteerit: vaihtoehtoja perinteisille antibiooteille. Kupari. Mikrobifysiologian edistyksessä. ScienEdirect.com
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Google -sivustot. Tehdä vedetöntä kuparisulfaattia. Paradoksissa kotikemiassa. Paikoilta palautettu.Google.com.
- « Sääntö T -ominaisuudet, niin että se palvelee esimerkkejä
- Vakio (ohjelmointi) käsite, tyypit, esimerkit »

