Sinkkisulfidi (ZNS)
- 4382
- 704
- Joshua Emmerich
 Sinkkisulfidi. Lähde: Wikimedia Commons
Sinkkisulfidi. Lähde: Wikimedia Commons Mikä on sinkkisulfidi?
Hän Sinkkisulfidi Se on epäorgaaninen yhdiste kaava ZnS, muodostettu Zn -kationit2+ ja anionit s2-. Sitä löytyy luonnosta pääasiassa kahtena mineraalina: Wurtzite ja Spheny (tai sinkkisekoitus), jälkimmäinen on sen päämuoto.
Sphenhell esitetään mustassa luonteessa sen esittämien epäpuhtauksien takia. Puhtaasti esittelee valkoisia kiteitä, kun taas wurtzitalla on harmahtavia valkoisia kiteitä.
Sinkkisulfidi on liukenematon veteen. Se voi aiheuttaa ympäristövahinkoja, koska se tunkeutuu maahan ja saastuttaa pohjaveden ja niiden virrat.
Sinkkisulfidia voi esiintyä muun muassa reaktioissa, korroosiolla ja neutraloinnilla.
Korroosiolla:
Zn +H2S => Zns +H2
Neutraloimalla:
H2S +Zn (OH)2 => Zns +2H2JOMPIKUMPI
Sinkkisulfidi on fosforesoiva suola, joka antaa sille useita käyttötarkoituksia ja sovelluksia. Lisäksi se on puolijohde ja valokasvatus.
Sinkkisulfidirakenne
Sinkkisulfidi omaksuu kiteisiä rakenteita, joita säätelevät sähköstaattiset nähtävyydet Zn -kationin välillä2+ ja anionin s2-. Nämä ovat kaksi: Spheny- tai sinkkisekoitus ja Wurzita. Molemmissa ioneissa minimoivat vastenmieliset ionit.
Sinkkisekoitus on vakain maanpäällisissä paine- ja lämpötilan olosuhteissa; Ja Wurzita, joka on vähemmän tiheä, johtuu kiteisestä uudelleenorganisoinnista lämpötilan noususta johtuen.
Kaksi rakennetta voivat esiintyä samanaikaisesti samassa Zns -kiinteässä muodossa, vaikka hyvin hitaasti Wurzita päättyy pääasiassa.
Sinkkisekoitus
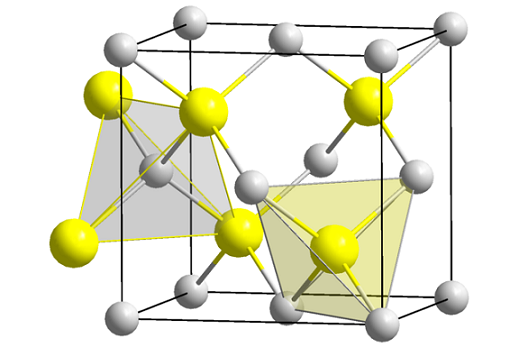
 Sinkkiseulun rakenne (Spheny). Lähde: Wikimedia Commons
Sinkkiseulun rakenne (Spheny). Lähde: Wikimedia Commons Ylivoimainen kuva näyttää kuutiosolun, joka on keskittynyt sinkkiseulun rakenteen kasvoihin. Keltaiset pallot vastaavat S -anioneja2-, ja harmaa zn -kationeista2+, Sijaitsee kuution kasvojen kulmissa ja.
Voi palvella sinua: Isobutil: nimikkeistö, koulutus, rakenne ja ominaisuudetHuomaa tetraedriset geometriat ionien ympärillä. Sinkkiseulua voi edustaa myös nämä tetraedrat, joiden reikillä lasin sisällä on sama geometria (tetraedriset ontelot).
Myös ZNS -osuus saavutetaan yksikkösoluissa; eli osuus 1: 1. Siten jokaiselle Zn -kationille2+ On anionia s2-. Kuvassa voi vaikuttaa siltä, että harmaat pallot ovat runsaasti, mutta todellisuudessa, kun ne ovat navan nurkissa ja keskustassa, ne jakavat muut solut.
Esimerkiksi, jos laatikon sisällä olevien neljän keltaisen pallon otetaan, kaikkien ympärillä olevien harmaan pallon "kappaleiden" tulisi lisätä sama (ja tehdä niin), neljä. Siten kuutiometriä yhtenäisessä solussa on neljä Zn: tä2+ ja neljä s2-, ZNS -stoikiometrinen osuus on toteutunut.
Samoin on tärkeää korostaa, että keltaisten pallojen edessä ja takana on tetraedriset reikiä (tila, joka erottaa ne toisistaan).
Wurzita
 Wurzite -rakenne. Lähde: Wikimedia Commons
Wurzite -rakenne. Lähde: Wikimedia Commons Toisin kuin sinkkiseoksen rakenne, Wurzita omaksuu kuusikulmaisen kiteisen järjestelmän (ylivoimainen kuva). Tämä on vähemmän kompakti, joten kiinteä on vähemmän tiheyttä.
Wurzitan ioneilla on myös tetraedrisia ympäristöjä ja 1: 1 -osuus, joka sopii ZNS -kaavan kanssa.
Sinkkisulfidiominaisuudet
Väri
Se voidaan esittää kolmella tavalla:
-Wurtzita, valkoiset ja kuusikulmaiset kiteet.
-Valkoisten ja kristallien ja kuutiokiteiden Sphenhell.
-Valkoisen tai harmahtavan tai kellertävän valkoisen jauheena ja kuutiometriä kellertäviä kiteitä.
Sulamispiste
1.700 ° C.
Vesiliukoisuus
Käytännössä liukenematon (0,00069 g/100 ml 18 ° C: ssa).
Liukoisuus
Liukenematon alkaliin, liukoinen laimennettuihin mineraalihapoihin.
Tiheys
Pallot 4,04 g/cm3 ja Wurtzita 4,09 g/cm3.
Kovuus
Sen kovuus on 3 - 4 mohs -asteikolla.
Vakaus
Vettä sisältävää hitaasti hapettaa sulfaatin. Kuivassa ympäristössä se on vakaa.
Hajoaminen
Kun lämmitetään korkeissa lämpötiloissa, hän emittoi myrkyllistä sinkkiä ja rikkioksidihöyryjä.
Se voi palvella sinua: natriumhydridi (NAH): Ominaisuudet, reaktiivisuus, vaarat, käyttöSinkkisulfidi -nimikkeistö
Zn: n elektroninen kokoonpano on [AR] 3D104S2. Kun menetät 4S -kiertoradan kaksi elektronia, se on kuin Zn -kationi2+ Orbitaaliensa kanssa. Siksi, koska Zn sähköisesti2+ Se on paljon vakaampi kuin Zn+, Sen valenssi on vain +2.
Siksi se jätetään pois varastossa olevalle nimikkeistölle, lisäämällä sen valenssi, joka on suljettu suluihin ja roomalaisilla numeroilla: sinkkisulfidi (II).
Systemaattiset ja perinteiset nimikkeet
Mutta on myös muita tapoja soittaa ZNS: lle jo nostetun lisäksi. Systemaattisessa määrin kunkin elementin atomien lukumäärä määritetään kreikkalaisten numeroijien kanssa, lukuun ottamatta elementtiä oikealle, kun se on vain yksi. Siten ZNS on nimetty seuraavasti: pullaSinkkisulfidi (eikä monozinc -monosulfuro).
Perinteisen nimikkeistön suhteen sinkkiin, kun sillä on yksi valenssi +2, se lisätään lisäämällä jälkiliite -Co. Tämän seurauksena sen perinteinen nimi on: Zínc -sulfidiICO.
Sinkkisulfidi käyttää
Pigmentteinä tai pinnoitteina
Sachtoliitti
Sachtholith on valkoinen pigmentti, joka on valmistettu sinkkisulfidilla. Sitä käytetään puttiesissa, mastikissa, tiivisteissä, alempien kannen, lateksimaalien ja opastuksissa.
Sen käyttö yhdistettynä ultraviolettivalojen absorboiviin pigmentteihin, kuten mikrotitaani- tai läpinäkyviä rautaoksidipigmenttejä, on välttämätöntä sääoluupigmenteissä.
Zns ja lateksimaalaukset
Kun ZNS: ää levitetään lateksi- tai kuvioituihin maalauksiin, se on pitkittynyt mikrobiditoiminta.
Windows- ja lentokoneiden kehykset
Suuren kovuuden ja rikkoutumisen, eroosion, sateen tai pölyn vuoksi se tekee siitä sopivan ulkomuotoisiin ikkunoihin tai lentokoneiden kehyksiin.
Pinnoite ja muut käyttötarkoitukset
ZNS: tä käytetään yhdisteiden kuljetuksessa käytettyjen roottorien päällysteessä kulumisen vähentämiseksi. Lisäksi sitä käytetään tulostusmusteiden, eristävien yhdisteiden, kestomuovisen pigmentaation, elektroluminesoivien liekkien ja lamppujen muovien tuotannossa.
Voi palvella sinua: Tunnsen Ligher: Ominaisuudet, toiminnot, esimerkit käytöstäNight Vision -laitteet ja näytöt
-Sinkkisulfidi voi olla läpinäkyvää, sitä voidaan käyttää ikkunana näkyvälle optiikalle ja infrapunaoptille. Sitä käytetään Night Vision -laitteissa, televisionäytöissä, tutkanäytöissä ja fluoresoivissa päällysteissä.
Elektroluminesenssi
ZNS -dopingia CU: lla käytetään elektroluminesenssipaneelien tuotannossa. Lisäksi sitä käytetään rakettien työntövoimassa ja gravimetriassa.
Sen fosfori -
Sen fosforesenssia käytetään kellojen neulojen värjäytymiseen ja siten visualisointiin ajan pimeässä; Myös lelujen, hätäsignaalien ja liikenteen ilmoitukset.
Fosforesenssi mahdollistaa sinkkisulfidin käytön katodiräteputkissa ja X -gray -näytöillä paistaa pimeissä pisteissä. Fosforenssin väri riippuu käytetystä aktivaattorin.
Puolijohde, valokasvatus ja katalyytti
- Spheny ja wurtzite ovat laajakaistainen rako -puolijohde. Sphaleriitissa on 3,54 eV -kaista, kun taas Wurtzitalla on 3,91 eV -kaistainen bitti.
- ZNS: ää käytetään CDS - ZNS/Zirconium - Titanium -fosfaatista koostuneen fotokatalyytin valmistuksessa, jota käytetään vedyntuotantoon näkyvällä valossa.
- Puuttuu katalysaattorina orgaanisten epäpuhtauksien hajoamiselle. Sitä käytetään värisynkronointin valmistuksessa LED -lamppuissa.
- Sen nanokiteitä käytetään ultrafiiliproteiinien havaitsemiseen. Esimerkiksi antamalla ZNS: n kvanttipisteet. Sitä käytetään yhdistetyn fotokatalysaattorin (CDS/ZNS) -tiO2: n valmistuksessa sähköiseen tuotantoon fotoelektrokatalyysin avulla.
Viitteet
- Pubchem (2018). Sinkkisulfidi. Otettu: Pubchem.NCBI.Nlm.NIH.Hallitus
- Quiminet (16. tammikuuta 2015). Sinkkisulfidiin perustuva valkoinen pigmentti. Toipunut: quiminet.com
- Wikipedia (2018). Sinkkisulfidi. Otettu: sisään.Wikipedia.org
- II-VI UK (2015). Sinkkisulfidi (ZNS). Otettu: ii-vi.On
- Rob Toreki (30. maaliskuuta 2015). Sinkkihallinta (ZNS) rakenne. Otettu: ILPI.com
- Kemian libretTexts (22. tammikuuta 2017). Structure-Zinc Blende (ZNS). Otettu: Chem.Librettexts.org
- Reade (2018). Sulfidisulfidi/ sinkki (ZNS). Otettu: Reade.com

