Puhtaat aineet

- 3526
- 294
- Arthur Terry II
Määrittelemme, mitkä ovat puhtaat aineet, niiden fysikaaliset ja kemialliset ominaisuudet, mitä tyyppejä on ja annamme sinulle useita esimerkkejä.
Mitkä ovat puhtaat aineet?
Se puhtaat aineet ovat kaikki niitä, jotka esittävät vakiona ja oman kemiallisen koostumuksen. Eli he ovat homogeeninen, Joten ne muodostuvat vain atomit tai molekyylit, jotka esiintyvät niiden symboleissa tai kemiallisissa kaavoissa.
Puhtaat aineet voidaan luokitella Yksinkertaiset (elementit) tai yhdisteet. Ne ovat yksinkertaisia, kun ne vain sisältävät Yhden tyyppinen atomi. Are yhdisteet Jos heillä on Kaksi tai useampaa erilaista atomia Heterogeenisten molekyylien muodostaminen.
Esimerkkejä yksinkertaisista puhtaista aineista ovat kulta (AU), kupari (Cu) tai sinkki (Zn). Jos löydämme muita erilaisia atomeja tai elementtejä, ne lakkaavat puhtaana: kulta sekoitettuna kuparin tai kuparin kanssa sekoitettuna sinkin kanssa. Siksi, seokset eivät ole puhtaita aineita.
Esimerkki puhtaan aineen yhdisteestä on hiilidioksidi (CO₂), joka koostuu kahdesta happiatomista ja yhdestä hiilestä. Voimme tunnistaa, että se on puhdas aine, koska Voit kirjoittaa kaavan.
Vesi (h₂o) on toinen esimerkki yhdisteestä puhdasta ainetta. Se ei kuitenkaan lakkaa olemasta puhdasta, jos lisäämme sokeria: sokerin ja veden seos on seos, ei puhdas aine. Sama sovellettaisiin, jos siihen liuentaan suolat.
Puhtaiden aineiden propertit
Puhtaalla aineilla on sarja fysikaalisia ja kemiallisia ominaisuuksia:
Homogeenisuus
He ovat homogeenisia, joten voit sanoa, että heillä on a Jatkuva koostumusE kaikessa massassaan tai laajennuksessaan.
Oletetaan, että meillä on puhdas aine, kuten rauta (usko). Jos jaamme sen pienempiin rautapaloihin, sillä on edelleen samat fysikaaliset ja kemialliset ominaisuudet.
Voi palvella sinua: propeenia (C3H6)Sen ominaisuuksien jatkuvat suuruudet
Jolla on yksi tyyppi atomit tai molekyylit Puhtaissa aineissa niiden fysikaaliset tai kemialliset ominaisuudet ovat erittäin hyvin määriteltyjä, eivätkä ne ole suuria variaatioita. Toisin sanoen niiden ominaisuuksilla on vakioita suuria arvoja tai arvoja samassa lämpötilassa tai paineessa.
Esimerkiksi: Puhdas vesi (H₂O) on aina kiteinen ja kiehuu samassa lämpötilassa. Muiden aineiden kanssa sekoitettuna siitä voi kuitenkin tulla pilvistä tai muuttaa väriä. Sitten sen ominaisuudet alkavat olla erilaisia: vaihda tiheys, viskositeetti, haju, lämpötila, jossa se jäätyy tai kiehuu, jne.
Eri fyysiset tilat
Puhtaita aineita voi esiintyä erilaisia tiloja tai fysikaalisia vaiheita, säilyttäen sen koostumuksen ja puhtauden.
Tislattu vesi on puhdasta ainetta. Jäädyttäessäsi se muuttuu jääksi, mutta sen koostumus ei muutu. Sama tapahtuu, kun se haihtuu: h₂o -molekyylit pysyvät samoina.
Vesi ylläpitää puhtauttaan kolmessa fysikaalisessa tilassa, ellei sekoitettu muiden elementtien tai yhdisteiden kanssa.
Kuvaus kemiallisella kaavalla
Puhtaat aineet voidaan kuvata täydellisesti Kemiallinen kaava.
Esimerkiksi H₂O -kaava kuvaa vettä ja sen molekyyliä, joten puhdas vesisäiliö voidaan kuvata h₂o: ksi ei enää.
Jos lisäämme suolaa (NaCl) tähän puhtaan vesisäiliöön, meillä on seos, jota ei enää voida kuvata H₂O -kaavalla, ja siksi se ei ole puhdas aine.
Kun ainetta (neste, kiinteä tai sooda) ei voida helposti kuvata yhdellä kemiallisella kaavalla, niin se ei ole puhdas.
Pureiden tyypit
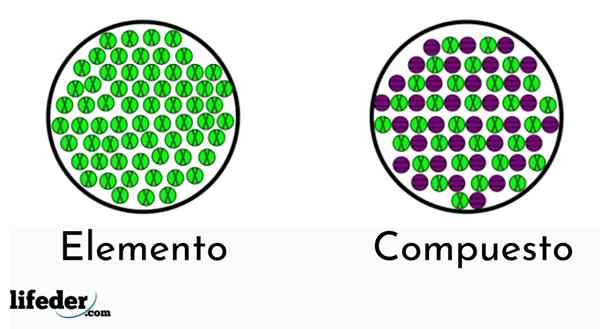 Elementeillä on vain yhden tyyppinen atomi, kun taas yhdisteillä on useampi kuin yksi tyyppi
Elementeillä on vain yhden tyyppinen atomi, kun taas yhdisteillä on useampi kuin yksi tyyppi Puhtaita aineita on kahta tyyppiä: yksinkertaiset (kemialliset elementit) ja kemialliset yhdisteet.
Voi palvella sinua: Kalsiumkarbonaatti: rakenne, ominaisuudet, muodostuminen, käyttötarkoituksetYksinkertaiset aineet (kemialliset elementit)
Aine, jonka muodostuu vain Eräänlainen atomi Kemiallista elementtiä vastaavaa voidaan pitää puhtaana aineena. Tämä on niin, että toisen kemiallisen elementin atomien esiintymisen tai erilaisten kemiallisten elementtien atomien esiintymisen vuoksi ei ole asianmukaista saastumista.
Puhdas hopea (AG) muodostuu vain hopeametalliatomilla (AG). Samoin nikkeliä (Ni) tai kuparia (Cu) -metalleja voidaan pitää puhtaina aineina, mikäli niitä ei ole niiden kappaleiden saastumisessa muiden kemiallisten elementtien saastumista.
Päinvastoin, seokset eivät ole puhtaita aineita, koska ne johtuvat kahden tai useamman metallin seoksesta. Siksi esimerkiksi pronssi tai messinki eivät ole puhtaita aineita.
Kemialliset yhdisteet
Puhdas aine on kemiallinen yhdiste, jos se muodostuu kaksi tai useampia kemiallisia elementtejä, Tämä muodostavat heterogeeniset molekyylit tai joukko ionisia verkkoja (suolat, oksidit, sulfaatit jne.-A.
Esimerkki kemiallisesta yhdisteestä on ammoniakki (NH3), muodostettu kolmella vetyatomilla ja typpiatomilla (NH3-A. Se on puhdas aine, jos kaikki sen molekyylit ovat samantyyppisiä ja niillä on NH -kaava3. Kuitenkin, jos se sekoitetaan kaasumaisen hapen tai vesihöyryn kanssa, se lakkaa olemasta puhdasta ainetta (se on kaasumainen seos).
Esimerkkejä puhtaista aineista
Yksinkertaiset puhtaan aineet
- Magnesium (mg)
- Kalsium (CA)
- Natrium (Na)
- Rauta (usko)
- Tina (SN)
- Kaasumainen happi (tai2-A
- Helio (hän)
- Elohopea (HG)
- Kupari (Cu)
- Nikkeli (Ni)
Yhdistettäviä puhdasta ainetta
- Hiilidioksidi (CO₂).
- Hiilimonoksidi (CO).
- Glukoosi (c6H12JOMPIKUMPI6.-A.
- Sitrushappo (C6H8JOMPIKUMPI7-A.
- Natriumsulfaatti (Na2Sw4-A.
- Natriumhydroksidi (NaOH).
- Vesi (h₂o).
- Natriumkarbonaatti (NA2Yhteistyö3-A.
- Rikkihappo (H2Sw4.-A.
- Natriumkloridi (NaCl).
Neuvoja puhtaan aineen tunnistamiseksi
Jos pystyt kirjoittamaan aineen kaavan tai se on puhdas elementti, se on puhdas aine.
Kiinnostavia teemoja
Homogeeniset seokset
Heterogeeniset seokset
Viitteet
- Helmestine, Anne Marie, PH.D -d. Puhdas aineen määritelmä. Toipunut: Admingco.com
- CK-12 Foundation et ai. Puhtaat aineet ja seokset. Kemian librettexts. Palautettu: Chem.Librettexts.org


