Elektronien meren teoria perusteet ja ominaisuudet
- 798
- 213
- Kelly Kilback
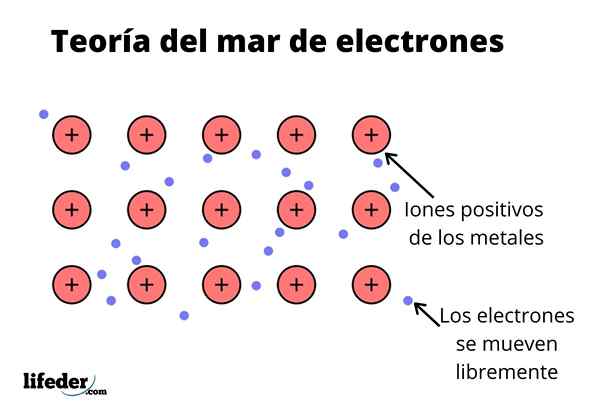
Se Elektronimeren teoria Se on hypoteesi, joka selittää poikkeuksellisen kemiallisen ilmiön, joka esiintyy metallisidoksissa matalalla elektronegatiivilla elementtien välillä. Tämä on elektronien jakaminen eri yhdistyneiden atomien välillä metallisidosten kautta.
Näiden sidosten välinen elektroninen tiheys on sellainen, että elektronit siirretään ja muodostavat "meren", jossa ne liikkuvat vapaasti. Se voidaan ilmaista myös kvanttimekaniikoilla: Jotkut elektronit (yleensä on yksi tai seitsemään atomia) on järjestetty kiertoradalle, joissa on useita keskuksia, jotka venyvät metallisella pinnalla.
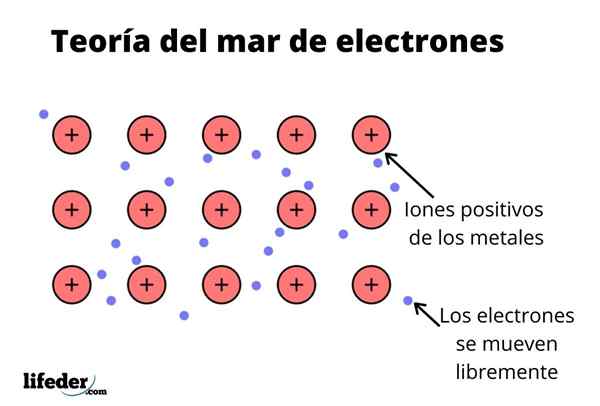
Lisäksi elektronit säilyttävät jonkin verran metallia, vaikka elektronisen pilven todennäköisyysjakauma on suurempi tiheys joidenkin spesifisten atomien ympärillä. Tämä johtuu siitä, että kun tiettyä virtaa käytetään, ne osoittavat johtavuutensa tiettyyn suuntaan.
[TOC]
Elektronimeren teorian perusteet
Metallielementeillä on suuri taipumus lahjoittaa viimeisimmän energiatason (valenssikerros) elektroneja johtuen niiden alhaisesta ionisaatioenergiasta suhteessa muihin elementteihin.
Tietäen tämän, kutakin metallista elementtiä voidaan pitää kationina, joka on kytketty sen viimeisen energiatason elektroniin, joka olisi alttiimpi lahjoittaa.
Kuten metallissa on suuri määrä atomeja, jotka on kytketty toisiinsa, voidaan olettaa, että tämä metalli muodostaa ryhmän metallikationeja, jotka on upotettu eräänlaiseksi valenssielektronien merelle, jolla on suuri siirtäminen.
Kun otetaan huomioon, että kationin (positiivinen kuormitus) ja elektronin (negatiivinen kuormitus) välissä sähköstaattiset vetovoimat ovat kytkettyjen metallin atomit voimakkaasti, kuvittele valenssielektronien siirtäminen, jotka käyttäytyvät sähköstaattisena liimana, joka säilyttää metallikationeihin kytkettynä.
Voi palvella sinua: polymeeritTällä tavalla voidaan päätellä, että mitä suurempi metallin Valencia -kerroksessa olevien elektronien lukumäärä, tällaisella sähköstaattisella liimalla on suurempi lujuus.
Ominaisuudet
Elektronimeren teoria tarjoaa yksinkertaisen selityksen metallilajien, kuten resistenssin, johtavuuden, ulottuvuuden ja muokattavuuden ominaisuuksille, jotka vaihtelevat metallista toiseen.
On havaittu, että metalleille annettu vastus johtuu niiden elektronien suuresta siirtämisestä, mikä tuottaa erittäin korkean koheesiovoiman sen muodostavien atomien välillä.
Tällä tavoin taipuisuus tunnetaan tiettyjen materiaalien kyvynä sallia rakenteensa muodonmuutokset antamatta tarpeeksi rikkoa, kun niille kohdistuu tiettyjä voimia.
Delokalisointi kerrosten muodossa
Sekä metallin taipuisuus että muokattavuus määritetään sen perusteella, että Valencia -elektronit puretaan kaikkiin suuntiin kerrosten muodossa, mikä saa ne syrjäyttämään toisiaan ennen ulkoisen voiman vaikutusta välttäen metallirakenteen hajoamista, mutta sallii sen muodonmuutos.
Samoin siirrettyjen elektronien liikkumisen vapaus mahdollistaa sähkövirran virtauksen, mikä aiheuttaa metallien erittäin hyvän sähkönjohtavuuden.
Lisäksi tämä elektronien vapaan liikkumisen ilmiö mahdollistaa kineettisen energian siirron eri metallialueiden välillä, mikä edistää lämmönsiirtoa ja tekee metalleista, jotka osoittavat suuren lämmönjohtavuuden.
Se voi palvella sinua: jodoosihappo (HIO2): Ominaisuudet ja käytötElektronien meren teoria metallikiteissä
Kiteet ovat kiinteitä aineita, joilla on fysikaalisia ja kemiallisia ominaisuuksia - tiheytenä, sulamis- ja kovuuspisteinä -, jotka määritetään sellaisten voimien avulla, jotka tekevät niitä muodostavat hiukkaset, joita pidetään yhdessä.
Tavallaan katsotaan, että metallisilla kiteillä on yksinkertaisimmat rakenteet, koska jokainen lasiverkon "piste" on miehittänyt itse metallin atomi.
Tässä mielessä on määritetty, että metallikiteiden rakenne on yleensä kuutio ja keskittyy kasvoihin tai vartaloon.
Näillä lajeilla voi kuitenkin olla myös kuusikulmainen muoto ja niillä on melko kompakti pakkaus, mikä antaa heille sen valtavan tiheyden.
Tästä rakenteellisesta syystä metallikiteissä muodostuvat linkit eroavat niistä, joita esiintyy muissa kiteissä. Koko kiteisen rakenteen ajan elektronit, jotka voivat muodostaa sidoksia, kuten edellä selitetään, selitetään aiemmin.

Teorian haitat
Metalliatomeissa on pieni määrä valenssielektroneja suhteessa niiden energiatasoon; Toisin sanoen energiatiloja on enemmän kuin kytkettyjen elektronien määrä.
Tämä tarkoittaa, että koska on olemassa vahva elektroninen siirtäminen ja myös osittain täytetty energiakaistat, elektronit voivat liikkua retikulaarisen rakenteen läpi, kun niille altistetaan sähkökenttä ulkomailta, elektronien valtameren muodostamisen lisäksi, mikä myöntää läpäisevyyden verkko.
Voi palvella sinua: OxácidoJoten metallien liitto tulkitaan positiivisten ionien ryhmittymäksi, joka yhdistää elektronien meri (negatiivinen kuorma).
On kuitenkin ominaisuuksia, joita ei selitetä tällä mallilla, kuten tiettyjen seoksien muodostuminen metallien välillä, joilla on spesifisiä koostumuksia tai kollektiivisten metallilinkkien stabiilisuutta, muun muassa muun muassa.
Nämä haitat selitetään kvanttimekaniikoilla, koska sekä tämä teoria että monet muut lähestymistavat on määritetty yhden elektronin yksinkertaisimman mallin perusteella yrittäen soveltaa paljon monimutkaisempiin monelektronisten atomien rakenteisiin.
Viitteet
- Wikipedia. (2018). Wikipedia. Haettu jstk.Wikipedia.org
- Holman, J. S., Ja kivi, s. (2001). Kemia. Palautettu kirjoista.Google.yhteistyö.mennä
- Parkin, G. (2010). Metallihame. Palautettu kirjoista.Google.yhteistyö.mennä
- Rohrer, G. S. (2001). Rakenne ja sitoutuminen kiteisiin materiaaleihin. Palautettu kirjoista.Google.yhteistyö.mennä
- Ibach, h., ja Lüth, H. (2009). Kiinteän valtion fysiikka: Johdatus materiaalitieteen periaatteisiin. Palautettu kirjoista.Google.yhteistyö.mennä
- « Kulttuurinen hybridisaatioprosessi, tyypit ja esimerkit
- 20 Aguascalientes -turistikohtaa (valokuvia) »

