Kalium -tiokianaattirakenne (KSCN) rakenne, ominaisuudet, käyttää

- 4524
- 1373
- Kelly Kilback
Hän Kalium -tiokerianaatti Se on epäorgaaninen yhdiste, jonka on muodostanut kalium (k), rikki (S), hiili (C) ja typpi (N) -elementit (n). Sen kemiallinen kaava on KSCN. Se on väritön tai valkoinen liukoinen kiinteä kiinteä kiinteä. Muodostuu ionikaliumk+ ja SCN Tiocianate -ioni-. KSCN löytyy sylkeä runsaasti.
Kalium -tiokianaattia käytetään laboratorioreagenssina erityyppisiin kemiallisiin analyyseihin. Sitä käytetään myös musteissa ja maalauksissa.
 Kiinteä KSCN -kalium -tiosyanaatti. JOMPIKUMPI.Luci/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons.
Kiinteä KSCN -kalium -tiosyanaatti. JOMPIKUMPI.Luci/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons. KSCN: tä on käytetty dentiinihyytelön liuottamiseen (hampaiden emalin alla) ennen hampaiden korjaavan materiaalin tai hartsin levittämistä. Sitä käytetään myös rokotutkimuksessa, koska se antaa meille mahdollisuuden purkaa tiettyjä biokemiallisia elementtejä bakteereista.
Sitä käytetään liuoksen muodossa, jossa metallit liukenevat kiillotusprosessin aikana sähkön tai elektropulidin avulla. Häntä on käytetty myös väärän veren saamisessa elokuviin ja näytelmiin.
Joskus sitä käytetään väärin maidon vakauden lisäämiseen, kun sitä ei pidetä jäähdytettynä. Mutta sillä on haittaa aiheuttaa kilpirauhasen vajaatoiminta, sairaus, jossa kilpirauhanen toimii huonosti.
[TOC]
Rakenne
Kalium -tiokianaatti muodostuu kaliumkationista k+ ja NCS Tiocianate Anion-. Jälkimmäinen muodostuu typellä (N), joka on kiinnitetty hiileen (C) kolminkertaisella sidoksella ja hiilihiilellä (S) yksinkertaisella sidoksella yksinkertaisella sidoksella.
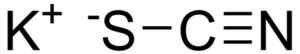 KSCN -kalium -tiosyanaatin kemiallinen rakenne. Edgar181 / pubi -verkkotunnus. Lähde: Wikimedia Commons.
KSCN -kalium -tiosyanaatin kemiallinen rakenne. Edgar181 / pubi -verkkotunnus. Lähde: Wikimedia Commons. Nimikkeistö
- Kalium -tiokerianaatti
- Kaliumsulfosyanaatti
- Potasic Tiocian -happosuola
- Kalium rodanato
- Kalium rodanuro
Ominaisuudet
Fyysinen tila
Väritön tai valkoinen kiinteä.
Molekyylipaino
97,18 g/mol
Sulamispiste
173 ºC
Hajoamislämpötila
500 ºC
Tiheys
1,88 g/cm3
Liukoisuus
Hyvin liukoinen veteen: 217 g/100 ml 20 ° C: ssa, 238 g/100 ml 25 ° C: ssa. Liukoinen etanoliin.
PHE
5% KSCN -liuoksessa on pH välillä 5,3 - 8,7.
Muut ominaisuudet
Puhtaan ja kuivan kalium -tiosyanaatin näytteet ovat stabiileja, jos niitä pidetään pimeässä hyvin peitetyissä lasipurkkeissa. Kuitenkin kosketuksessa auringon suoran valon kanssa värittömät kiteet muuttuvat nopeasti kellertäviksi.
Puhtaat suojatut KSCN -suolaliuokset ovat täysin vakaita.
KSCN pystyy turvottamaan gelatiinia ja kollageenia. Kalium -tiosyanaatin vesipitoiset liuokset reagoidessaan mangaanidioksidin kanssa2 Ne hapettelevat ja muodostavat tiokianogeenin (SCN)2.
Se voi palvella sinua: Silver Yoduro (AGI): rakenne, ominaisuudet, hankkiminen, käyttöSaada
Kalium -tiokianaatti voi valmistaa sulamiskaliumsyanidia (KCN) rikkiä (S). Reaktio on nopeaa ja kvantitatiivista.
KCN + S → KSCN
Se voidaan saada liuoksessa, joka liuottaa rikkiä (S) bentseeniin tai asetoniin ja lisäämällä kaliumsyanidiliuosta (KCN) isopropanoliin. Tämä reaktio aikoo analysoida liuoksen rikin määrää.
Kalium -tiokianaatti voidaan saada puhtaana peräkkäisillä uudelleenkiteytyksillä vedestä tai etanolista.
Läsnäolo luonnossa
Kalium -tiokianaatti on sylkeä runsaasti (15 mg/100 ml), mutta veressä ei ole.
Myös joidenkin nisäkkäiden (kuten lehmän) maidossa on hyvin pieniä määriä tiodiatoa luonnollisella tavalla.
Sovellukset
Useissa sovelluksissa
Kalium -tiokianaattia on käytetty erilaisissa kemiallisissa analyyseissä. Sitä on käytetty hopea -ionin analysointiin tai titraukseen, myös muiden analyysien reagenssina ja indikaattorina.
KSCN: tä käytetään väriaineissa ja pigmenteissä. Sitä käytetään maalauksissa ja musteissa.
Valokuvateollisuudessa sitä käytetään erityisesti valokuvauskalvojen valmistuksessa, koska se tarjoaa muovikalvojen hyytelön kiinteän laskeutumisen.
Tiosyanaatin pitoisuutta veressä on käytetty lääketieteellisissä kokemuksissa määritettäessä, missä määrin jotkut ihmiset tupakoivat, koska tiosyanaatti on tupakansavussa läsnä oleva vetysyanidi (HCN), joka on johdettu.
Hammassovelluksissa
Kalium -tiokianaattia on käytetty eläinten hampaiden korjaamisessa. Sitä on levitetty onnistuneesti dentiinin pintaan esikäsittelynä ennen kuin agentti levitetään avoimen reiän saamiseksi tai kytkemiseksi.
Dentin on kerros, joka on hampaiden emalin alapuolella.
 KSCN on tarjonnut hampaiden dentiinin pinnan käsittelemiseksi ennen karies -reikiä täyttävän materiaalin levittämistä. Kirjoittaja: Mudassar Iqbal. Lähde: Pixabay.
KSCN on tarjonnut hampaiden dentiinin pinnan käsittelemiseksi ennen karies -reikiä täyttävän materiaalin levittämistä. Kirjoittaja: Mudassar Iqbal. Lähde: Pixabay. Kalium -tiosyanaatti suosii dentiinissä olevan gelatiinin turvotusta, joten tämä kerros poistetaan helposti ja on parempi tarttuvuus tai kiinnitetty materiaaliin, jota hammas havaitaan (hartsi).
Lääketieteen laboratorioissa
KSCN: tä käytetään rokotteiden tai bakteeriuutteiden valmistuksessa.
Patogeeniset bakteerit kasvavat inkuboimalla riittävissä laboratorioastioissa. Sitten astiaan lisätään fosfaatin pH -säätelijä ja KSCN, jossa bakteerien viljely sijaitsee.
Voi palvella sinua: kloorobentseeni (C6H5CL) Bakteerikasvit uutetaan KSCN: llä rokotteiden saamiseksi lääketieteellisistä kokemuksista. Kirjoittaja: Wikiimages. Lähde: Pixabay.
Bakteerikasvit uutetaan KSCN: llä rokotteiden saamiseksi lääketieteellisistä kokemuksista. Kirjoittaja: Wikiimages. Lähde: Pixabay. Osa tästä bakteerien valmistuksesta otetaan ja asetetaan pulloon. Sitä sekoitetaan riittävästi aikaa ja suspensio sentrifugoituu nesteen erottamiseksi kiinteästä materiaalista. Supernatantti (neste) kerätään ja diad.
Tuloksena on uute, jota käytetään rokottamaan tieteellisiä kokemuksia laboratorioeläimistä.
Metalliteollisuudessa
Kalium -tiokeriaaattia käytetään metallielektropolidissa. Elektropolidi on kemiallinen prosessi, joka mahdollistaa metallin pinnan käsiteltäväksi sen micoruguestiuden vähentämiseksi, ts. Sileä metallipinta.
Tämä tehdään sähköllä, mikä tekee metallista sileän toiminnan positiivisena napa- tai elektrolyyttisenä solun anodina. Karheus liukenee kalium -tiosyanaattiliuokseen ja metalli on siten sileä.
Kuvaamisessa tai teatterin kuvaamisessa
KSCN: tä käytetään verisimulaatiossa elokuva- ja televisioelokuvissa tai näytelmissä.
Esimerkiksi kehon alueelle levitetään kalium -tiosyanaatin (KSCN) liuos, joka "kärsii" simuloidusta leikkauksesta tai aggressiosta. Muoviveitsi tai objektin leikkaus simulointi kylpee ferrikloridiliuoksessa (FECL3-A.
"Leikkaus" -objekti, jolla on fadl, ohitetaan varovasti3 iholle kostutettu KSCN: ssä. Välittömästi punainen piste tai tahra muodostuu hyvin samanlaisesta kuin veri.
 KSCN: tä on käytetty väärän veren saamiseen elokuvissa tai teatterissa. Kirjoittaja: Corey Ryan Hanson. Lähde: Pixabay.
KSCN: tä on käytetty väärän veren saamiseen elokuvissa tai teatterissa. Kirjoittaja: Corey Ryan Hanson. Lähde: Pixabay. Tämä johtuu ferri- ja vesi -tiosyanaattikompleksin [Fe) muodostumisesta (H2JOMPIKUMPI)5-2+ mikä on voimakas punainen hyvin samanlainen kuin veri:
KSCN + FECL3 + 5 h2O → [Fe (NC) (H2JOMPIKUMPI)5-2+ + 2 Cl- + Kcl
 Kscn -kalium -tiosyanaatti sekoitettuna ferrikloridiin vedessä muodostaa voimakkaan punaisen yhdisteen, joka on samanlainen kuin veri. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay.
Kscn -kalium -tiosyanaatti sekoitettuna ferrikloridiin vedessä muodostaa voimakkaan punaisen yhdisteen, joka on samanlainen kuin veri. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay. Kalium -tiosyanaatin virheellinen käyttö
Kalium -tiosyanaattia käytetään häikäilemättä estämään maitoa bakteerien tai sienten hyökkäyksestä, menettää ominaisuutensa ja heikentävän.
Trooppisissa maissa käytetään menetelmää, jota kutsutaan ”lakto-butxidaasijärjestelmää” tai LP-järjestelmää, mikä lisää varastoinnin vakautta varastossa korkeissa ympäristölämpötiloissa, kun sen jäähdytys ei ole mahdollista.
 Joissakin maissa ei ole mahdollista jäähdytysmaitoa, ja siksi kalium -tiosyanaattia käytetään estämään sen heikentymistä. Kirjoittaja: Thomas B. Lähde: Pixabay.
Joissakin maissa ei ole mahdollista jäähdytysmaitoa, ja siksi kalium -tiosyanaattia käytetään estämään sen heikentymistä. Kirjoittaja: Thomas B. Lähde: Pixabay. Tämä menetelmä käyttää maidon luonnollista antibakteerista järjestelmää, joka aktivoituu lisäämällä tiosyanaatin pitoisuutta (jo pieninä määrinä maidossa) ja vetyperoksidia (H2JOMPIKUMPI2-A.
Viranomaiset eivät kuitenkaan salli tätä menetelmää monissa maissa, jotka säätelevät jalostettuja elintarvikkeita.
Voi palvella sinua: titaani: historia, rakenne, ominaisuudet, reaktiot, käyttötarkoituksetJotkut häikäilemättömät ihmiset lisäävät KSCN: n maito irrationaalisesti H: n kanssa tai ilman H: tä2JOMPIKUMPI2, Se, mikä on vaaraa kuluttajien terveydelle, koska tiiolesiaatteet ovat aineita, jotka aiheuttavat kilpirauhanen vaurioita ja voivat aiheuttaa kilpirauhasen vajaatoimintaa, kun ne nautitaan korkeissa pitoisuuksissa.
 Kalium -tiokianaattimaido voi aiheuttaa vaurioita sen nauttivien terveydelle. Kirjailija: Titapic. Lähde: Pixabay.
Kalium -tiokianaattimaido voi aiheuttaa vaurioita sen nauttivien terveydelle. Kirjailija: Titapic. Lähde: Pixabay. Riskejä
Sitä tulisi välttää kalium -tiosyanaatin pölyn asuttamista. Käsineitä ja suoja -linssejä on kätevää manipuloidessaan. Lyhyen altistumisen jälkeen kalium -tiosyanatolle, se voi aiheuttaa vaikutusta hermostoon, kuten liialliset tunteet ilman aiheita, levottomuutta ja kouristuksia.
Pitkän altistumisen jälkeen kilpirauhasen ja keskushermoston jälkeen voidaan vaikuttaa, mikä ilmenee kilpirauhasen vajaatoiminnana ja joidenkin toimintojen heikkenemisenä. Nielemisen yhteydessä voi aiheuttaa sekaannusta, pahoinvointia, oksentelua, kohtauksia ja heikkouksia.
Jos KSCN kytkeytyy päälle tai palaa, erittäin myrkylliset syanidikaasut vapautuvat; Tämä tapahtuu myös happojen lisäämisessä. Laboratoriossa sitä on manipuloitava erittäin hyvin tuuletetun uuttokellon sisällä.
Viitteet
- Jarvinen, L.Z -z. et al. (1998). Kanien suojaamisen induktion immuniteetti on inaktivoitu COAD -antaminen Multicide Pasteurella Toksiinin ja kalium -tiosyanaattiuutteen. Infektio ja immuniteetti, elokuu 1998, s. 3788-3795. NCBI toipunut.Nlm.NIH.Hallitus.
- Tani, ja. ja Togaya, t. (tuhatyhdeksänsataayhdeksänkymmentäviisi). Dentiinin pintakäsittely ilman happoa. Dental Materials Journal 14 (1): 58-69, 1995. Jtagesta toipunut.JST.Mennä.JP.
- Kolthoff, minä.M. ja lingaani, J.J -. (1935). Kalium -tiosyanaatti ensisijaisena standardiaineena. American Chemical Society -lehti 1935, 57, 11, 2126-2131. Pubista toipunut.ACS.org.
- Balmasov, a.V. et al. (2005). Hopean elektropolointi vesi-orgaanisissa liuoksissa kalium-tiosyanaatissa. Prot Met 41, 354-357 (2005). Linkki palautettu.Jousto.com.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Lyijy, d.R -. (Toimittaja) (2003). CRC: n kemian ja fysiikan käsikirja. 85th CRC -lehdistö.
- Tyner, t. ja Francis, J. (2017). Kaliumitiosyanaatti. ACS -reagenssikemikaalit. Pubista toipunut.ACS.org.
- Kanthale, P. et al. (2015). Laadullinen testi vieraan tiosyanaatin havaitsemiseksi maidossa. J Food Sci Technol (maaliskuu 2015) 52 (3): 1698-1704. NCBI toipunut.Nlm.NIH.Hallitus.
- Roy, D. et al. (2018) Piilääke DOT-pohjainen fluoresoiva koetin: Tiosyanaatin synteesin karakterisointi ja tunnistaminen ihmisen veressä. ACS Omega 2018, 3, 7, 7613-7620. Pubista toipunut.ACS.org.
- Gammon, k. (2018). Väärennetyn veren tiede. Tieteen sisällä. Haettu sisäpuolelta.org.

