Absorbanssi mikä on, esimerkit ja harjoitukset ratkaistu
- 2696
- 597
- Dr. Travis Reichert
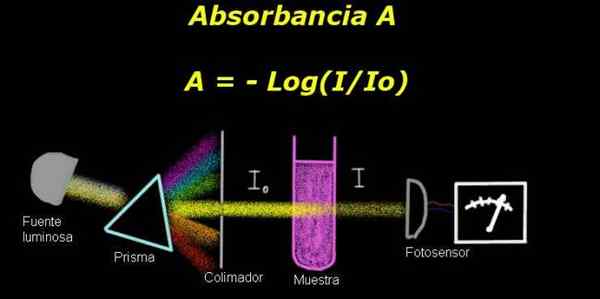
Se absorbanssi Se on logaritmi, jolla on negatiivinen merkki kehittyvän valon voimakkuuden ja valon voimakkuuden välisestä osamäärästä läpikuultavan liuoksen näytteessä, joka on valaistu yksivärisellä valolla. Tämä osuus on läpäisy.
Näytteen läpi valon läpäisyprosessia kutsutaan valaistuslähetys, Ja absorbanssi on sen mitta. Siksi absorbanssista tulee vähiten läpäisyn logaritmia ja on tärkeä tosiasia näytteen pitoisuuden määrittämiseksi, joka yleensä liuentuu liuottimeen, kuten veteen, alkoholiin tai muuhun.
 Kuvio 1. Absorbanssiprosessin kaavio. Valmistettu f. Zapata
Kuvio 1. Absorbanssiprosessin kaavio. Valmistettu f. Zapata Absorbanssin mittaamiseksi vaaditaan laite Elektrofotometri, jonka kanssa mitataan virta, joka on verrannollinen sen pinnalla tapahtuvaan valaiseeseen voimakkuuteen.
Laskettaessa lähetys Io.
Sitten liuottimeen liuenneen näytteen samoilla valaistusolosuhteilla asetetaan. Elektrofotometrillä mitattu mitta on merkitty Yllyttää, jonka avulla voit laskea läpäisevyyden T Seuraavan kaavan mukaan:
T = i / ijompikumpi
Se on vapautettu määrä. Se Absorbanssi a Tämä ilmaistaan seuraavasti:
A = - log (t) = - log (i / ijompikumpi-A
[TOC]
Molaarinen absorbanssi ja imeytyminen
Kemikaalin muodostavat molekyylit kykenevät absorboimaan valoa, ja tämän mitta on tarkalleen absorbanssi. Se on seurausta fotonien ja molekyylielektronien välisestä vuorovaikutuksesta.
Siksi se on suuruus, joka riippuu näytteen muodostavien molekyylien tiheydestä tai pitoisuudesta ja myös valon kulkevasta optisesta polusta tai etäisyydestä.
Voit palvella sinua: Newtonin kolmas laki: sovellukset, kokeet ja harjoituksetKoetiedot osoittavat, että absorbanssi -Lla on lineaarisesti verrannollinen pitoisuuteen C ja etäisyys d -d Valo kulki. Joten sen laskemiseksi näiden parametrien perusteella voidaan määrittää seuraava kaava:
A = ε⋅c⋅d
Edellisessä kaavassa, ε Se on vakio suhteellisuus, joka tunnetaan nimellä Molaarinen absorboiva.
Molaarinen imeytyminen riippuu aineen tyypistä ja aallonpituudesta, jolla absorbanssi mitataan. Se Molaarinen absorboiva Se on myös herkkä näytteen lämpötilaan ja sen pH: lle.
Olut-lambert-laki
Tämä suhde absorbanssin, absorbaation, konsentraation ja etäisyyden välillä näytteessä olevan valon paksuuden paksuudesta tunnetaan olut-lambert-laki.
 Kuva 2. Olutlaki - Lambert. Lähde: f. Zapata,
Kuva 2. Olutlaki - Lambert. Lähde: f. Zapata, Alla on joitain esimerkkejä siitä.
Esimerkit
Esimerkki 1
Kokeen aikana näyte, jolla on punainen valo helium-neon-laservalot, joiden aallonpituus on 633 nm. Elektro-fotometri mittaa 30 mV, kun laservalo vaikuttaa suoraan ja 10 mV, kun se kulkee näytteen läpi.
Tässä tapauksessa läpäisevyys on:
T = i / io = 10 mV / 30 mV = ⅓.
Ja absorbanssi on:
A = - log (⅓) = log (3) = 0,48
Esimerkki 2
Jos sama aine asetetaan astiaan, jolla on puolet paksusta.
On katsottava, että jos paksuus laskee puoleen, niin optiseen paksuuteen verrannollinen absorbanssi pienenee puoleen, toisin sanoen A = 0,28. Tonnit läpäisevyys annetaan seuraavalla suhteella:
Voi palvella sinua: Pystysuora laukaus: Kaavat, yhtälöt, esimerkitT = 10-A = 10^(-0.28) = 0,53
Elektro-fotometri merkitsee 0,53*30 mV = 15,74 mV.
Ratkaisut
Harjoitus 1
Tietyn patentoidun yhdisteen molaarinen absorboivuus halutut määrittää. Tätä varten 589 nm: n natriumvalaisimen valolla on valaistu valaistu. Näyte asetetaan 1,50 cm paksulle.
Se perustuu pitoisuusliuokseen 4,00 × 10^-4 moolia litralta ja läpäisevyys mitataan, mikä johtaa 0,06. Määritä näillä tiedoilla näytteen molaarinen imevyys.
Ratkaisu
Ensinnäkin määritetään absorbanssi, joka määritellään vähiten logaritmiin, joka perustuu kymmenen läpäisevyydestä:
A = - log (t)
A = - log (0,06) = 1,22
Sitten käytetään Lambert-beerin lakia, joka luo suhteen absorbanssin, molaarisen imeytymisen, pitoisuuden ja optisen pituuden välillä:
A = ε⋅c⋅d
Molaarisen absorbaation puhdistaminen saadaan seuraava suhde:
ε = A/(C⋅D)
Annetujen arvojen korvaaminen:
ε = 1,22/(4,00 × 10^-4 m⋅1,5 cm) = 2030 (m⋅cm)^-1
Aikaisempi tulos on pyöristetty kolmeen merkittävään numeroon.
Harjoitus 2
Tarkkuuden parantamiseksi ja näytteen 1 molaarisen absorboivan virheen määrittämiseksi näyte 1 laimennetaan peräkkäin puolessa konsentraatiosta ja läpäisevyys mitataan kutakin tapausta.
Alkaen CO = 4 × 10^-4 m läpäisy T = 0,06 Seuraava tietosekvenssi läpäisevyydestä ja absorbanssista, joka on laskettu läpäisevyydestä:
CO/1-> 0,06-> 1,22
CO/2-> 0,25-> 0,60
CO/4-> 0,50-> 0,30
CO/8-> 0,71-> 0,15
CO/16-> 0,83-> 0,08
CO/32-> 0,93-> 0,03
CO/64-> 0,95-> 0,02
CO/128-> 0,98-> 0,01
CO/256-> 0,99-> 0,00
Tee näiden tietojen kanssa: tee:
Se voi palvella sinua: paikallaan olevat aallot: kaavat, ominaisuudet, tyypit, esimerkita) pitoisuuteen perustuva absorbanssikaavio.
b) tietojen lineaarinen säätö ja löydä kaltevuus.
c) Laske saadusta kaltevuudesta molaarinen imeytyminen.
Ratkaisu
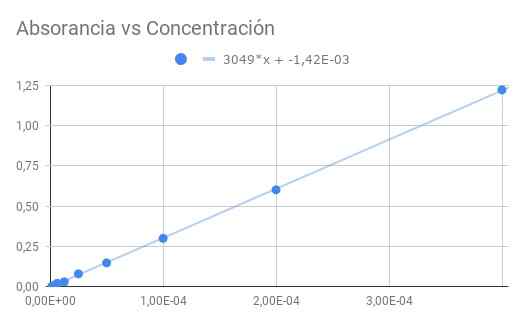 Kuva 3. Absorbanssi vs. pitoisuus. Lähde: f. Zapata.
Kuva 3. Absorbanssi vs. pitoisuus. Lähde: f. Zapata. Saatu kaltevuus on molaarisen absorbaation tuote optisella etäisyydellä, joten rinteen jakaminen 1,5 cm: n pituudella saamme molaarisen absorboivan
ε = 3049/1,50 = 2033 (m⋅cm)^-1
Harjoitus 3
Harjoituksen 2 tiedoilla:
a) Laske kunkin datan absorbaatio.
b) Määritä keskimääräinen arvo molaariselle absorbaatiolle, sen keskihajontaan ja keskiarvoon liittyvän tilastollisen virheen.
Ratkaisu
Molaarinen absorbointi lasketaan jokaiselle testatulle pitoisuudelle. Muista, että valaistusolosuhteet ja optinen etäisyys pysyvät kiinteinä.
Molaarisen absorbaation tulokset ovat:
2033, 2007, 2007, 1983, 2158, 1681, 2376, 1 872, 1862 yksiköissä 1/(m*cm).
Näistä tuloksista voimme ottaa keskiarvon:
= 1998 (m*cm)^-1
Vakiopoikkeamalla: 184 (m*cm)^-1
Keskimääräinen virhe on keskihajonta jaettuna datanumeron neliöjuurilla, ts
Δ = 184/9^0,5 = 60 (m*cm)^-1
Lopuksi päätellään, että patentoidun aineen absorboiva absorbointi taajuudella 589 nm, joka on tuotettu natriumlamppu:
= (2000 ± 60) (m*cm)^-1
Viitteet
- Atkins, p. 1999. Fysikaalinen kemia. Omega -versiot. 460-462.
- Opas. Läpäisy ja absorbanssi. Palautettu: kemia.Laguia2000.com
- Ympäristömyrkytys. Lambertin läpäisevyys, absorbanssi ja laki. Palautettu: arkistosta.Innovationumh.On
- Seikkailufysiikka. Absorbanssi ja läpäisevyys. Toipunut: rpfisica.Blogin.com
- Sistofotometria. Palautettu: Chem.Librettexts.org
- Ympäristömyrkytys. Lambertin läpäisevyys, absorbanssi ja laki. Palautettu: arkistosta.Innovationumh.On
- Wikipedia. Absorbanssi. Toipunut: Wikipedia.com
- Wikipedia. Spektrofotometria. Toipunut: Wikipedia.com
- « Latinalaisamerikkalainen avant -garde -konteksti, ominaisuudet, kirjoittajat
- Totalitarismin alkuperä, ominaispiirteet, syyt ja seuraukset »

