Adeniinirakenne, biosynteesi, toiminnot
- 1757
- 63
- Edgar VonRueden
Se adeniini Se on puriinin typpipohja, jota löytyy elävien organismien ja virusten ribonukleiinihapoista (RNA) ja deoksihiobonukleisista (DNA). Jotkut näiden biopolymeerien (RNA ja DNA) toiminnoista ovat varastointi, replikaatio, rekombinaatio ja geneettisen tiedon siirto.
Nukleiinihappojen muodostamiseksi adeniinin typpiatomi 9 muodostaa ensinnäkin glukosidisen sidoksen hiili 1 -palkkiolla (C1 ') riboosista (RNA) tai 2'-desexirribosalle (DNA) (DNA) (DNA) (DNA). Tällä tavoin adeniinin adenosiini- tai adenosiininukleosidin muoto.
 Lähde: Pepemonbu [CC BY-SA 3.0 (http: // creativecommons.Org/lisenssit/by-SA/3.0/]]
Lähde: Pepemonbu [CC BY-SA 3.0 (http: // creativecommons.Org/lisenssit/by-SA/3.0/]] Toiseksi adenosiinin oksidryyli (-oh) hiili 5 'sokeri (ribose tai 2'-disaksiribus) hiili) muodostaa esterin yhteyden fosfaattiryhmään.
Elävissä soluissa läsnä olevien fosfaattiryhmien lukumäärästä riippuen se voi olla adenosín-5'-monofosfaatti (AMP), adenosiini-5'-difosfaatti (ADP) ja adenosín-5'-trifosfaatti (ATP). Vastaavia, joilla on myös 2'-desexirribosa. Esimerkiksi deoksyadenosín-5'-monofosfaatti (kostea) jne.
[TOC]
Rakenne ja ominaisuudet
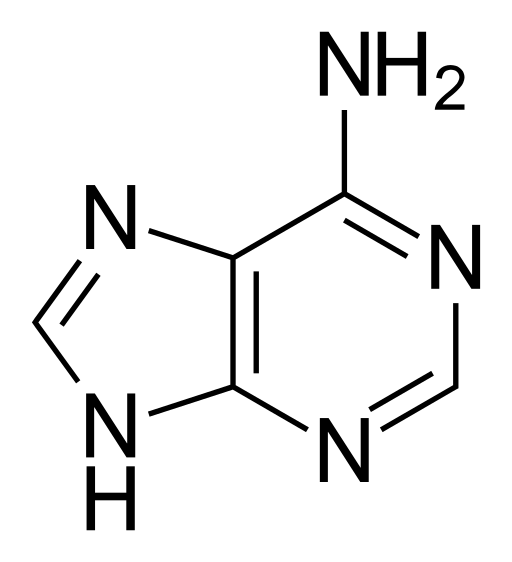
Adeniinilla, jota kutsutaan 6-aminopuriiniksi, on empiirinen kaava C5H5N5, Ja sen molekyylipaino on 135,13 g/mol, puhdistetaan heikkona keltaisena kiinteänä aineena, 360ºC kiehumispisteellä.
Sen molekyylissä on kaksoisrenkaan kemiallinen rakenne kaksoiskonjugaattisidoksilla, mikä on pyrimidiinin fuusio imidatsoliryhmän kanssa. Tämän vuoksi adeniini on litteä heterosyklinen molekyyli.
Sen suhteellinen liukoisuus on 0,10 g/ml (25 ° C: ssa) happamissa ja emäksisissä vesiliuoksissa, PKA: n ollessa 4,15 (25 ° C: ssa).
Samasta syystä se todennäköisesti havaitaan absorbanssilla 263 nm: llä (E -absorptiokertoimella1,2 mm = 13,2 m-1.cm-1 HCL: ssä 1,0 m), sähkömagneettinen spektrialue, joka vastaa lähellä ultraviolettia.
Biosynteesi
Puriininukleotidi -biosynteesi on identtinen käytännössä kaikissa elävissä olennoissa. Se alkaa aminoryhmän siirtämällä glutamiinista 5-fosforribosyyli-pyrofosfaatin (PRPP) substraattiin ja tuottaa 5-fosforribosyllamiinia (PRA).
Tämä on reaktio, jota katalysoi glutamiini-PRPP-transferaasi, keskeinen entsyymi tämän metabolisen reitin säätelyssä.
Aminohappojen glutamiinin, glysiinin, metenyyli-folaton, aspartaatin, aspartaatin, aminohappojen peräkkäisten lisäysten jälkeen10-Formil-PRA: n refolaatti, joka sisältää kondensaatiot ja renkaiden sulkemisen, inosiini-5'-monofosfaatin (IMP), jonka heterosyklinen yksikkö on hypoksantiinia (6-oksipuriini)), joka on 6-oksipuriini).
Näitä lisäyksiä ohjaa ATP -hydrolyysi ADP: lle ja epäorgaaniselle fosfaatille (PI). Myöhemmin aspartaatin aminohuryhmä, joka liittyy guanosín-teiffosfaatin (GTP) hydrolyysiin, lisätään lopulta AMP: n tuottamiseksi.
Jälkimmäinen hallitsee tämän biosynteettisen reitin hallintaa negatiivisen palautteen kautta vaikuttaen entsyymeihin, jotka katalysoivat PRA: n muodostumista ja IMP: n modifiointia.
Voi palvella sinua: kvaternääriset kuluttajatKuten muiden nukleotidien hajoaminen, adenosiininukleotidien typpipohja käy läpi "kierrätys" -prosessin.
Kierrätys koostuu fosfaattiryhmän siirtämisestä PRPP: stä adeniiniin ja AMP -muodon ja pyrofosfaatin (PPI). Se on yksivaiheinen adeniinin fosforibosyylitransferasferaasi katalysoima.
Toiminnot oksidatiivisessa ja pelkistimen aineenvaihdunnassa
Adeniini on osa useita tärkeitä oksidatiivisen aineenvaihdunnan molekyylejä, jotka ovat seuraavat:
- Flavinan ja Adeninan dyukleotidi (Fad/Fadh2) ja nikotiinamidia adeniinidyukleotidi (NAD+/Nadh), jotka osallistuvat oksidin vähentämisreaktioihin siirtämällä hydridi-ionit (: h--A.
- Koentsyymi A (COA), joka osallistuu asyyliryhmien aktivointiin ja siirtoon.
Oksidatiivisen aineenvaihdunnan aikana NAD+ Se toimii elektronia vastaanottaja -substraattina (hydridi -ionit) ja NADH -muodossa. Vaikka villitys on kofaktori, joka hyväksyy elektronit ja muuttuu fadhiksi2.
Toisaalta adeniini muodostaa adeniinin nikotiinamidin disoottisen fosfaatin (NADP+/Nadph), joka osallistuu vähentämään aineenvaihduntaa. Esimerkiksi NADPH on elektronien luovuttajien substraatti lipidi- ja deoksihiobonukleotidien biosynteesin aikana.
Adeniini on osa vitamiineja. Esimerkiksi niasiini on Nadin edeltäjä+ ja NADP: stä+ Ja riboflavina on villitysesiasema.
Toiminnot geeniekspressiossa
Adeniini on osa S-adenosyylimeioniinia (SAM), joka on metyyliradikaali luovuttaja (-CH3) ja osallistuu adeniini- ja sytosiinijätteiden metylointiin prokaryooteissa ja eukaryooteissa.
Prokaryooteissa metylaatio tarjoaa oman DNA: n tunnistusjärjestelmän, joka suojaa omien rajoittavien entsyymiensa DNA: ta.
Eukaryooteissa metylaatio määrittää geenien ilmentymisen; toisin sanoen se määrittelee, mitkä geenit on ilmaistava ja mitkä eivät. Lisäksi adeniinimetylaatiot voivat merkitä vaurioituneet DNA: n korjausalueet.
Monilla DNA: han, kuten transkriptiotekijöihin sitoutuvat proteiinit, on glutamiini- ja parsagiinin aminohappotähteet, jotka muodostavat vety sidoksia N: n n -atomin kanssa7 adenine.
Toiminnot energian aineenvaihdunnassa
Adeniini on osa ATP: tä, joka on molekyyli, jolla on korkea energia; Toisin sanoen sen hydrolyysi on eksergonista, ja Gibbs-vapaa energia on korkea ja negatiivinen arvo (-7.0 kcal/mol). Soluissa ATP osallistuu moniin reaktioihin, jotka vaativat energiaa, kuten:
- Edistää enderin grattisia kemiallisia reaktioita entsyymeillä, jotka osallistuvat välittäjäaineenvaihduntaan ja anaboliaan, muodostamalla korkeanergian välittäjät tai kytkettyjä reaktioita.
Se voi palvella sinua: Quintana Roo Flora ja eläimistö- Edistää proteiinin biosynteesiä ribosomeissa sallimalla aminohappoesterfikaation vastaavalla siirto-RNA: lla (ART), aminohaksiili-Arntin muodostamiseksi.
- Edistää kemiallisten aineiden liikettä solukalvojen kautta. Kuljetinproteiineja on neljä tyyppiä: P, F, V ja ABC. Tyypit P, F ja V Transport -ionit ja ABC -tyyppi kuljettaa substraatteja. Esimerkiksi Na Atasa+/K+, Luokka P, tarvitset ATP: n kahden k -solun pumppaamiseen sisälle+ ja ulos kolme na+.
- Ajaa lihasten supistumista. Se tarjoaa energian, jonka ohjaa aktiinifilamenttien liukuminen myosiiniin.
- Ydinkuljetusten lisääminen. Kun heterodimeerisen reseptorin beeta -alayksikkö liittyy ATP: hen, on vuorovaikutuksessa ydinhuokoskompleksin komponenttien kanssa.
Muut toiminnot
Adenosiini toimii ligandina vastaanottavien proteiinien ja suoliston epiteelisolujen läsnäolon saamiseksi, missä se toimii solunulkoisena tai neuromodulaattorin lähettiläänä, kun muutokset soluenergian aineenvaihdunnassa tapahtuvat.
Adeniinia on läsnä voimakkaissa viruslääkkeissä, kuten Arabiniladenina (ARAA), jonka tuottavat jotkut mikro -organismit. Lisäksi se on puromiciinissa, antibiootissa, joka estää proteiinien biosynteesiä ja sen tuottajaa suvun mikro -organismit Streptomyces.
AMP: ssä se toimii reaktioiden alustana, joka tuottaa toisen syklisen AMP -lähettilään (AMPC). Tämä adenylaattisyklaasientsyymin tuottama yhdiste on välttämätön suuressa osassa solunsisäisiä signalointeja, jotka ovat välttämättömiä solujen lisääntymiseen ja eloonjäämiseen, samoin kuin tulehdukseen ja solukuolemaan.
Sulfaatti vapaassa tilassa ei ole reaktiivinen. Kun solu tulee sisään, siitä tulee adenosiini-5'-fosfosulfaatti (APS) ja sitten 3'-fosfoadenosín-5'-fosfosulfaatissa (PAPS). Nisäkkäissä PAPS on sulfaattiryhmien luovuttaja ja muodostavat orgaanisten sulfaattien estereitä, kuten hepariinin ja kondroitiinin.
Kysteiinin biosynteesissä S-adenosyylimeioniini (SAM) toimii edeltäjänä S-adenosylhomosysteiinin synteesille, joka transformoi useita vaiheita, entsyymien katalysoimana, kysteiinissä.
Prebioottinen synteesi
Kokeellisesti on osoitettu, että syanidin (HCN) ja ammoniakin (NH: n (NH3;. Tämä tapahtuu ilman, että joku elävä solu tai solumateriaali on läsnä.
Prebioottiset olosuhteet sisältävät vapaan molekyylin hapen puuttumisen, erittäin pelkistävän ilmakehän, voimakkaan ultraviolettisäteilyn, myrskyissä syntyneet suuret sähkökaarit ja korkeudet lämpötiloissa. Tämä olettaa, että adeniini oli tärkein ja runsas typpipohja, joka muodostettiin prebioottisen kemian aikana.
Voi palvella sinua: kasvisto ja eläimistö EuroopastaSiten Adeninan synteesi muodostaisi avainvaiheen, joka mahdollistaisi ensimmäisten solujen alkuperän. Näillä oli oltava kalvo, joka muodosti suljetun osaston, jonka sisällä olisi molekyylit, joita tarvitaan ensimmäisten biologisten polymeerien rakentamiseksi, jotka ovat tarpeen itsensä jatkamiseen.
Käytän solu- ja terapeuttisena viljelytekijänä
Adeniini on yhdessä muiden orgaanisten ja epäorgaanisten kemiallisten yhdisteiden kanssa, mikä on välttämätön ainesosa käytetystä reseptistä, jota käytetään maailman biokemiassa, geneettisessä, molekyylibiologiassa ja maailman mikrobiologialaboratorioissa, elinkelpoisten solujen viljelyyn ajan myötä.
Tämä johtuu siitä, että solujen normaalit villilajikkeet voivat havaita ja vangita käytettävissä olevan adeniinin ja käyttää sitä omien adeniininukleosidien syntetisoimiseen.
Tämä tarkoittaa solujen selviytymisen muotoa, joka taloudellinen sisäiset resurssit syntetisoivat monimutkaisempia biologisia molekyylejä ulkomailta otetuista yksinkertaisista esiasteista.
Kroonisen munuaissairauden kokeellisissa malleissa hiirillä on mutaatio adeniinin fosforribosyylitransferaasigeenissä, joka tuottaa entsyymin ei -aktiivisen. Näitä hiiriä annetaan adeniinipitoisuuden, natriumsitraatin ja glukoosin pitoisuudella, laskimonsisäisesti niiden nopean palautumisen edistämiseksi.
Tämä käsittely perustuu siihen tosiasiaan, että PRPP, alkuperäinen puriinibiosynteesin metaboliitti, syntetisoidaan riboosi-5-fosfaatista pentoosifosfaattipolulla, jonka käynnistysmetaboliitti on glukoosi-6-fosfaatti. Kansainväliset sääntelyelimet eivät kuitenkaan hyväksy monia näistä ratkaisuista ihmisen käyttöön.
Viitteet
- Burstock, G. 2014. Puriinit ja purinoketit. Molekyylibiologian yleiskatsaus. Viitteet moduulit biolääketieteellisissä tieteissä. Word Wide Web -osoite: https: // doi.org/10.1016/B978-0-12-801238-3.04741-3
- Claramount, D. et al. 2015. Lasten kroonisen sairauden eläinmallit. NefrologiaYllyttää-lla,35 (6): 517-22.
- S. S. Ja Pearson, J. 1989. Adeniininukleotidien metabolia. Kiertotutkimus, 65: 531-37
- Dawson, R. et al. 1986. Tiedot biokemiallisesta tutkimuksesta. Clarendon Press, Oxford.
- Drougbank. 2019. Adenine -kemikka. Word Wide Web -osoite: https: // www.Lääkekankki.CA/Drugs/DB00173
- Horton, R; Moran, L; Scrimgeour, G; Perry, m. Ja rawn, d. 2008. Biokemian periaatteet. 4. painos. Pearson -koulutus.
- Ritari, G. 2009. Purinergiset vastaanottimet. Neurotieteen tietosanakirja. 1245-52. Word Wide Web -osoite: https: // doi.org/10.1016/B978-008045046-9.00693-8
- Mathews, Van Holde, Ahern. 2001. Biokemia. 3. painos.
- Murgola, E. 2003. Adeniini. Genetiikan tietosanakirja. Word Wide Web -osoite: https: // doi.org/10.1006/rwgn.2001.0008
- Murray, R; Granner, D; Mayes, P. Ja Rodwell, V. 2003. Harperin kuvitettu biokemia. 26th Painos. McGraw-Hill -yritykset.
- Nelson, DL & Cox, M. 1994. Lehninger. Biokemian periaatteet. 4. painos. Ed Omega.
- Sigma-Aldrich. 2019. Adeniinikemiallinen arkki. Word Wide Web -osoite: https: // www.Sigmaaldrich.com/cag/tuote/aldrich/ga8626?Lang = sisään
- « Laktogeneesin ominaisuudet ja vaiheet
- Lämmön absorboivat kaavat, kuinka se lasketaan ja ratkaistu harjoitus »

