Alanina -ominaisuudet, rakenne, toiminnot, biosynteesi
- 4110
- 518
- Juan Breitenberg V
Se tytölle (Wing) on yksi 22 tunnetusta aminohapposta, jotka muodostavat kaikkien organismien proteiinien rakenteen bakteereista miehiin. Kuten organismi voi syntetisoida, tämä luokitellaan ei -välttämättömäksi aminohapoksi.
Proteiineilla on emäksinen tai primaarirakenne, joka koostuu aminohappiketjusta, jota kutsutaan polypeptidiketjuksi, näissä ketjuissa jokainen aminohappo muodostuu keskushiilellä, jota kutsutaan hiili a.
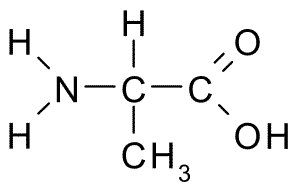
 Alaniinin aminohapon kemiallinen rakenne (lähde: Borb, Wikimedia Commonsin kautta)
Alaniinin aminohapon kemiallinen rakenne (lähde: Borb, Wikimedia Commonsin kautta) Α-hiili liittyy neljään ryhmään: aminoryhmä (-NH2), karboksyyliryhmä (-COH), vetyatomi (-H) ja ryhmä- tai sivuketju (-R), joka tunnistaa jokaisen aminohappon. Sivuketjussa hiilit ottavat peräkkäin kirjaimet ß, γ, Δ ja ε.
Aminohapot luokitellaan niiden sivuketjujen polaarisuuden mukaan, ja siten on hydrofobisia ja hydrofiilisiä polaarisia aminohappoja, jotka puolestaan voivat olla neutraaleja, emäksisiä ja happamia. Alaniini on hydrofobinen apolaarinen aminohappo ja on yksinkertaisin aminohappo glysiinin jälkeen ja runsaimmin useimmissa proteiineissa.
Alaniini voidaan muodostaa lihakseen ja kuljettaa maksaan, missä se johdetaan glukoneogeeniselle reitille, toisin sanoen reitti glukoosin muodostumiseen ei -glukosidisista aineista. Alaniini voidaan syntetisoida myös maksassa tryptofaanin ja urasiilin katabolismin kautta ja voi hajottaa pyruvaatin muodostamiseksi.
Osallistu tryptofaanin, pyridoksiinin (B6) ja lihan synteesiin.
Sitä käytetään ruokavalion lisäyksenä urheilun suorituskyvyn parantamiseksi ja sitä esiintyy luonnollisesti lehmän, sianlehden ja kalan lihassa sekä maidossa sekä niiden johdannaisissa ja munissa. Jotkut palkokasvit, hedelmät ja pähkinät ovat myös runsaasti alaniinia.
[TOC]
Rakenne
Aikaisemmin kommentoitiin, että alaniinilla, kuten kaikilla aminohapolla, on a-hiili, jossa on neljä ryhmää, jotka ovat siihen yhdistyneitä, ovat R-ryhmän A metyyliryhmä (-CH3).
Siksi kehon pH: lle (noin 7.4) Alaniinin a-hiili on kytketty amino-protoniryhmään (-NH3+) karboksyyliryhmään, joka on menettänyt protonin (-CO-) vedyyn ja metyyliryhmään (-CH3).
Useimmat aminohapot ovat ionisoitavissa pH: lle 7.0 ja geometrisesti heillä voi olla isomeerejä, jotka tunnetaan enantiomeereinä, jotka ovat spekulaarisia kuvia, kuten oikean ja vasemman käden kanssa.
Voi palvella sinua: Histokemia: perusta, käsittely, värjäysSitten kaikkia aminohappoja voidaan löytää "kiraaliparisiksi", jotka on merkitty D tai L: ksi (vastaavasti dekstro ja Levo), hiili -a ympäröivien atomien sijainnin mukaan.
Kuitenkin alaniini, kuten useimpien aminohappojen kanssa.
Tätä aminohappoa voidaan löytää myös β-alaniinina, jossa aminoryhmä on kiinnittynyt sen β-hiileen, toisin sanoen sen sivuketjun ensimmäiseen hiileen.
P-alaniinia löytyy pantaanihaposta (B5-vitamiini) ja joissakin luonnollisissa peptideissä. D-alaniinia löytyy joistakin polypeptideistä, jotka ovat osa joidenkin bakteerisolujen seinämiä.
Ryhmä R (Metilo, CH3-A
Alaniinin sivuketjun metyyli on tyydyttynyt hiilivety, joka antaa apolaarisen hydrofobisen ominaisuuden tälle aminohapolle. Tämä alaniinin ominaisuus on yleinen tämän ryhmän muiden aminohappojen kanssa, kuten glysiini, valiini, leusiini ja isoleusiini.
Aminohapot, jotka muodostavat alifaattisen ryhmän, ovat kemiallisesti neutraaleja aminohappoja ja niillä on erittäin tärkeä rooli proteiinien kolmen dimensionaalisen rakenteen muodostumisessa ja ylläpidossa, koska niillä on taipumus reagoida toisiinsa ilman vettä.
Nämä aminohapot, mukaan lukien alaniini, sisältävät saman määrän ionisoitavia ryhmiä, joilla on vastakkaiset kuormat, joten niillä ei ole nettokuormaa ja niitä kutsutaan "Viiveet ".
Funktiot
Tunnetuimpana aminohapona, alaniinia käytetään peptidien ja proteiinien synteesissä yleensä, ja se osallistuu polypeptidirakenteen ja joidenkin proteiinien tertiääriseen rakenteeseen muodostumiseen.
Toinen alaniinin tärkeistä toiminnoista on osallistua epäsuorasti glykemian hallintaan:
Se voi aiheuttaa pyruvaattia ja päinvastoin, se voi myös saavuttaa maksan ja tulla glukoosiksi glukoneogeneesin avulla, joka on havaittu verenkiertoon tai käytettäväksi glykogeenisynteesissä, tarpeen mukaan tarvittaessa tarvittaessa.
Alaniini osallistuu ammoniumin kuljettajana lihaksesta maksaan, koska se voidaan syntetisoida pyruvaatin aminaationa, maksan kuljettamisessa ja transaminaatiolla transaminaatiolla.
Tämä tapahtuu samanaikaisesti a-zotoglutaraatin muuntamisen kanssa glutamaatiksi, joka voi päästä ureasykliin ja tulla pyruvaatiksi.
Muut toiminnot
Tämä aminohappo on välttämätön tryptofaanin ja pyridoksiinin synteesille. Vaikka se on kemiallisesti hyvin vähän reaktiivista, alaniinilla voi tunnistaa substraatin ja entsymaattisen säätelyn tunnistamisen.
Voi palvella sinua: Parafilettinen ryhmäYksi β-alaniinin toiminnoista on ruokavalion lisäys, koska sitä käytetään liikunnan ergogeenisenä apuna. Β-alaniinin saanti lisää lihaksen (β-alaniinin ja histidiinin muodostama dipéptidi) konsentraatiota luustolihakseen, joka toimii "puskuri".
Normaalisti lihainen ei vaikuta merkittävästi lihassolun kokonaispuskurin kapasiteettiin ja tämä johtuu sen alhaisesta pitoisuudesta. Β-alaniinin antaminen lisää tätä pitoisuutta ja siten puskurikapasiteettia, joten se parantaa vastustuskykyä vähentämällä väsymystä.
Biosynteesi
Alaniinin tärkein synteesi ihmiskehossa tapahtuu pyruvihapon pelkistävällä aminaatiolla. Tämä reaktio vaatii yhden entsymaattisen vaiheen.
Pyruvaatti tarjoaa hiiliruenton ja glutamaatti tarjoaa aminoheryhmän, joka siirretään pyruvaattiin. Tätä palautuvaa reaktiota katalysoi entsyymi on transaminaasi -alaniini.
Tämän reaktion seurauksena tuotetaan alaniini ja a-da-dateglutaraatti. Alaniini voi sitten olla läsnä glukoneogeneesissä, glykolyysissä ja Krebs -syklissä.
Toinen alaniinilähde tulee tryptofaanin hajoamisesta asetyyli-CoA: ksi. Tällä reitillä, kun 3-hydroksi-kinureniinin hydrolysi-kinureninaasientsyymit muodostuvat 3-hydroksien antranilaatin ja alaniinin kanssa. Alanine vapautuu ja 3-hydroksinen antranilaatti seuraa aineenvaihdunnan reittiä.
Urasiilin hajoaminen on toinen alaniinin lähde. Tässä tapauksessa on β-alaniini, joka voi seurata useita metabolisia reittejä, joista yhdestä on tulla asetyyli-CoA.
Heikkeneminen
Aminohappojen hajoamisen yleinen prosessi
Aminohappoja ei varastoida hiilihydraateiksi ja rasvoiksi, joten ne, jotka vapautuvat proteiinien hajoamisen aikana, tulisi käyttää uudelleen uusien proteiinien ja nukleotidien synteesiin.
Toisaalta aminohappoja voidaan hajottaa ja niiden hiilihapotettuja luurankoja voidaan käyttää katabolisissa tai anabolisissa reaktioissa.
Kun aminohapot hajoavat, muodostuu ylimääräinen typpiammoniakki, joka on myrkyllinen aine, joka on poistettava ja aminohappojen hajoamisen ensimmäinen vaihe on typen eliminointi.
Nisäkkäissä tämä hajoaminen tapahtuu maksassa; Siellä kaikki aminohappo, joka on ylimääräinen ja jota ei voida käyttää.
Alaniinin heikkeneminen
Alaniinin hajoaminen tapahtuu muuntamalla alaniinin pyruvaatiksi. Tätä reaktiota katalysoi transaminaasi-alaniini, ja se vaatii a-zotoglutaraatin läsnäolon aminoheryhmän hyväksynnänä ja sitä seuraavan glutamaatin muodostumisen; Se on palautuva reaktio.
Voi palvella sinua: virulenssitekijätNämä alaniinin muodostumisreaktiot pyruvaatista ja alaniinin hajoamisesta pyruvaatin muodostamiseksi ovat osa sykliä, johon liittyy luurankoja ja maksa.
Maksa vie glukoosin lihakseen ja lihakseen glykolyysin kautta glukoosin pyruvaatiksi ATP: n tuottamiseksi; Tämä pyruvaatti voi päästä alaniinin synteesiin, joka voidaan kaataa verenkiertoon ja palaa maksaan, mikä tekee siitä jälleen pyruvaatin, joka menee glukoneogeneesiin glukoosin muodostamiseksi.
Tarvittaessa sykli toistetaan. Maksassa alaniinin pyruvaatin tuotanto tuottaa ammoniumioneja, jotka katsovat glutamiinia ja glutamaattia ja ne tulevat urealle. Sitten urea eliminoidaan virtsaan.
Alaniini, glysiini, kysteiini, seriini ja treoniini ovat glykogeenisiä aminohappoja, koska niiden hajoaminen voi aiheuttaa pyruvaattia, a-zetoglutaraattia, sukkinyyli-CoA: ta, fumaraatin tai oksalasetaatin, kaikki glukoosien esiosorit.
Ruokia, joissa on runsaasti alaninaa
Aminohappojen tärkeimmät lähteet ovat vähärasvaiset lihat, kalat, äyriäiset, munat ja maitotuotteet, mutta alaniinia löytyy myös monista kasvien alkuperästä olevista elintarvikkeista. Esimerkki Alaninan rikkaista elintarvikkeista on:
- Lihat, kuten lehmä, sianliha, lampaat, kana, kalkkuna, kani, kalat; Munat, maito ja johdannaiset.
- Kuivat hedelmät, kuten hasselpähkinät, pähkinät, kastanjat, mantelit ja maapähkinät ovat alanina lähteitä.
- Kookospähkinä, avokado, parsa, munakoiso, kassava tai kassava, punajuuret, porkkanat ja bataatit.
- Palkokasvit, kuten maissi, pavut ja herneet.
- Viljat, kuten riisi, ruis, vehnä, kaakao, kaura ja ruki.
Viitteet
- Caruso, J., Charles, J., Unruh, k., Giebel, r., Learmonth, L., & Potter, W. (2012). P-alaniinin ja karnosiinin ergogeeniset vaikutukset: Ehdotettu tulevaisuuden tutkimus tehokkuuden kvantifioimiseksi. Ravintoaineet, 4(7), 585-601.
- Gille, c., Bölling, c., Hoppe, a., Bulik, s., Hoffmann, S., Hübner, k.,… Holzhütter, H. G. (2010). Hepatonet1: Ihmisen hepatosyytin kattava metabolinen rekonstruointi maksafysiologian analysoimiseksi. Molekyylijärjestelmien biologia, 6(411), 1-13.
- Mathews, c., Van Holde, K., & Ahern, k. (2000). Biokemia (3. ed.-A. San Francisco, Kalifornia: Pearson.
- Murray, r., Taivutus, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Harperin kuvitettu biokemia (28. ed.-A. McGraw-Hill Medical.
- Nelson, D. Lens., & Cox, M. M. (2009). Lehninger -biokemian periaatteet. Omega -versiot (5. ed.-A.

