Toissijainen alkoholi Mikä on, rakenne, ominaisuudet, käyttää
- 4332
- 104
- Louis Moen
Mikä on toissijainen alkoholi?
Eräs toissijainen alkoholi Siinä on hydroksyyliryhmän (OH) hiilihiili, joka on kiinnitetty kahteen hiilihiiliin. Samaan aikaan primaarisessa alkoholissa hydroksyyliryhmän hiilihiili on kytketty hiiliatomiin ja kolmen hiiliatomiin kiinnitettyyn tertiääriseen alkoholiin.
Alkoholit ovat hiukan heikompia happoja kuin vesi seuraavan PKA: veden kanssa (15,7); Metyylialkoholit (15,2), etyyli (16), isopropyyli (sekundaarinen alkoholi, 17) ja lämpö (18). Kuten voidaan nähdä, isopropyylialkoholi on vähemmän hapan kuin metyyli- ja etyylialkoholit.
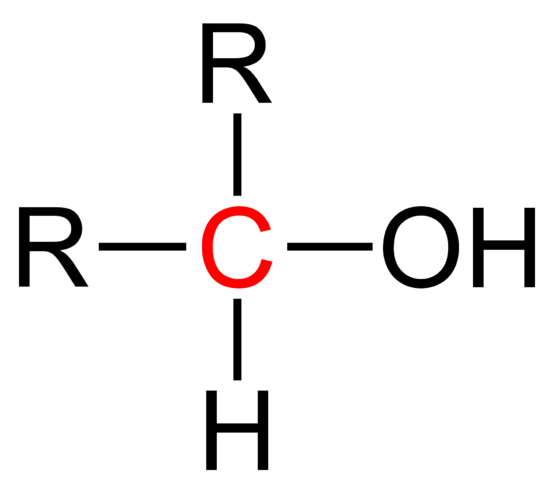
 Toissijaisen alkoholin rakennekaava. Wikimedia Commons
Toissijaisen alkoholin rakennekaava. Wikimedia Commons Yläkuvassa esitetään toissijaisen alkoholin rakennekaava. Punainen hiili on OH: n haltija, ja se on kytketty kahteen alkyyli (tai aryyli) R -ryhmään ja yhteen vetyatomiin.
Kaikilla alkoholeilla on ROH: n geneerinen kaava; Mutta jos haltija hiiltä havaitaan yksityiskohtaisesti, ensisijaiset alkoholit saadaan (RCH2Voi), toissijainen (r2CHOH, täällä nostettu) ja tertiäärinen (R3Coh). Tämä tosiasia vaikuttaa sen fysikaalisiin ominaisuuksiin ja reaktiivisuuteen.
Toissijaisen alkoholin rakenne
Alkoholirakenteet riippuvat R -ryhmien luonteesta. Toissijaisten alkoholien osalta voidaan kuitenkin tehdä joitain esimerkkejä, kun otetaan huomioon, että vain lineaarisia rakenteita voi olla vain lineaarisia rakenteita tai ilman seurauksia tai syklisiä rakenteita. Esimerkiksi sinulla on seuraava kuva:
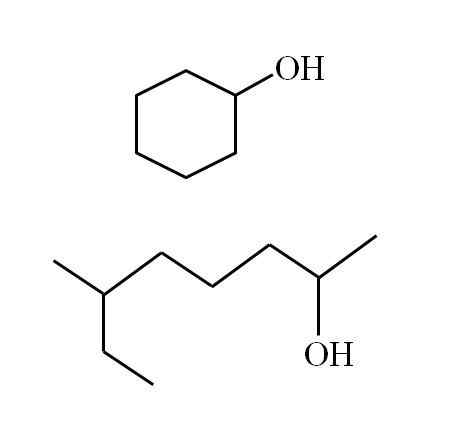 Syklinen sekundaarinen alkoholi ja toinen haarautunut ketju. Lähde: Gabriel Bolívar
Syklinen sekundaarinen alkoholi ja toinen haarautunut ketju. Lähde: Gabriel Bolívar Huomaa, että molemmilla rakenteilla on jotain yhteistä: OH on linkitetty "V: hen". V: n jokainen pää edustaa yhtä suurta ryhmää (kuvan yläosa, syklinen rakenne) tai erilaista (alaosa, haarautunut ketju).
Tällä tavoin kaikki toissijaiset alkoholit tunnistetaan erittäin helposti, vaikka sen nimikkeistöä ei tunneta ollenkaan.
Ominaisuudet
Kiehumispisteet
Toissijaisten alkoholien ominaisuudet eivät eroa liikaa muista alkoholista. Ne ovat yleensä läpinäkyviä nesteitä, ja ne ovat kiinteitä huoneenlämpötilassa, sen on muodostettava useita vety silloja ja niiden korkea molekyylimassa.
Se voi palvella sinua: perbromiinihappo (HBRO4): Ominaisuudet, riskit ja käytötKuitenkin sama rakenteellinen kaava r2CHOH ehdottaa tiettyjä ainutlaatuisia ominaisuuksia näille alkoholille. Esimerkiksi OH -ryhmä on vähemmän altistunut ja saatavana vetyjen sillien vuorovaikutuksiin, R2CH-OH-OHCHR2.
Tämä johtuu siitä, että R -ryhmät, auton hiilihiilen vieressä, voidaan tuoda ja estää vety sitojen muodostumista. Seurauksena on, että sekundaaristen alkoholien kiehumispisteet ovat alhaisemmat kuin ensisijaisella (RCH2VAI NIIN).
Happamuus
Brönsted-Lowryn määritelmän mukaan happo on se, joka luovuttaa protonit tai vety-ionit, H+. Kun tämä tapahtuu toissijaisen alkoholin kanssa, sinulla on:
R -2CHOH + B- => R2Köyhä- + HB
Konjugaatti Ras2Köyhä-, Alkoholianioni, negatiivisen kuorman on vakiintunut. Toissijaisella alkoholilla stabilointi on pienempi, koska kahdella R -ryhmällä on elektroninen tiheys, joka hylkää negatiivisen kuorman happiatomiin tietyssä määrin.
Samaan aikaan primaarisen alkoholin alkoksidianionissa, RCH2JOMPIKUMPI-, Elektronista torjuntaa on vähemmän vain yksi R -ryhmä eikä kahta. Lisäksi vetyatomit eivät käytä merkittävää torjumista, ja päinvastoin, ne edistävät negatiivisen kuormituksen vakauttamista.
Siksi sekundaariset alkoholit ovat vähemmän happamia kuin primaariset alkoholit. Jos näin on, niin ne ovat perusteellisempia ja tarkalleen samoista syistä:
R -2CHOH + H2B -+ => R2ChoH2+ + HB
Nyt R -ryhmät vakauttavat positiivisen kuorman happea antamalla osan elektronisesta tiheydestään.
Reaktiot
Vetyhalligenidi ja fosfori -trihalogenidi
Toissijainen alkoholi voi reagoida vetyhalogenidin kanssa. Isopropyylialkoholin ja bromhytihapon välisen reaktion kemiallinen yhtälö esitetään rikkihappon keskiarvolla ja tuottamalla isopropyylibromidia:
CH3ChoHch3 + Hbr => ch3Chbrch3 + H2JOMPIKUMPI
Ja voit myös reagoida fosforin trihalogenueron kanssa, PX3 (X = br, i):
Se voi palvella sinua: nikkelihydroksidi (III): rakenne, ominaisuudet, käytöt, riskitCH3-CHOH-Ch2-CH2-CH3 + PBR3 => CH3-CHBR-CH2-CH2-CH3 + H3Poikki3
Yllä olevan kemikaali vastaa leikkauksen ja fosforitribromidin välistä reaktiota, aiheuttaen sekunnin penlibromidin.
Huomaa, että molemmissa reaktioissa on sekundaarinen alkyylihalogenidi (R2Chx).
Kuivuminen
Tässä reaktiossa katoaa H ja OH, jotka ovat kadonneet, muodostaen kaksoissidoksen näiden kahden hiiliatomin välillä. Siksi alkeenin muodostuminen on muodostettu. Reaktio vaatii happokatalyytin ja lämmönsyötön.
Alkoholi => alkeeni + h2JOMPIKUMPI
Sinulla on esimerkiksi seuraava reaktio:
Sykloheksanoli => sykloheksen + h2JOMPIKUMPI
Reaktio aktiivisten metallien kanssa
Toissijaiset alkoholit voivat reagoida metallien kanssa:
CH3-CHOH-Ch3 + K => cho3Köyhä-K -k -+CH3 + ½ h+
Tässä isopropyylialkoholi reagoi kaliumin kanssa kalium -isoproksidi- ja vety -ionien muodostamiseksi.
Esteröinti
Toissijainen alkoholi reagoi karboksyylihapon kanssa esterin perustamiseksi. Esimerkiksi seppilisen alkoholin reaktion kemiallinen yhtälö on esitetty etikkahapolla puoliksi butyyliasetaatin tuottamiseksi:
CH3ChoHch2CH3 + CH3Cooh ch3Keittää3CH2CH3
Hapetus
Primaariset alkoholit hapettavat aldehydoja, ja nämä puolestaan hapettelevat karboksyylihappoja. Mutta sekundaariset alkoholit hapettavat asetonin. Reaktioita katalysoi yleensä kaliumdikromaattia (k2Kro7) ja kromihappo (H2Kro4-A.
Globaali reaktio on:
R -2CHOH => r2C = O
Nimikkeistö
Toissijaiset alkoholit nimitetään osoittamalla pääketjun OH -ryhmän asemaan (pidempi). Tämä numero edeltää nimeä tai voi mennä mainitun ketjun vastaavan alkaanin nimen jälkeen.
Esimerkiksi Cho3CH2CH2CH2ChoHch3, Se on 2-heksanoli tai heksaan-2-to.
Jos rakenne on syklinen, osoitinta ei tarvitse sijoittaa; ellei ole muita korvaavia. Siksi toisen kuvan syklistä alkoholia kutsutaan sykloheksanoliksi (rengas on kuusikulmainen).
Voi palvella sinua: amiesitJa saman kuvan muille alkoholille (haarautunut) sen nimi on: 6-etyyli-heptan-2 -ol.
Sovellukset
-Sec-butanolia käytetään liuottimena ja keskiteoksena. Se on läsnä jarrujen, teollisuuspuhdistusaineiden, kiillotuksen, pinting, mineraalien vaahdotusaineiden ja hedelmien ja hajusteiden essenssien hydraulinesteissä.
-Isopropanolialkoholia käytetään teollisena liuottimena ja antikoagulanttina. Sitä käytetään öljyissä ja nopeasti kuivausvärissä, kuten antiseptisissä ja korvikkeissa kosmetiikan etanolille (esimerkiksi: ihoemulaatiot, kapillaarikohtaa ja kitkakohtaista alkoholia).
-Isopropanoli on nestemäisten saippuan, kristallienpuhdistusaineiden, alkoholeiden juomien synteettisten aromatisaattoreiden ainesosa. Lisäksi se on välikemikaali.
-Sykloheksanolia käytetään liuottimena, kudoksen viimeistelyssä, nahka- ja emulgoivien saippuan ja synteettisten pesuaineiden prosessoinnissa.
-Metyylisikoheksanoli on pureskelutuotteiden ainesosa, joka perustuu saippualle ja erityiskudosten pesuaineille.
Esimerkit
2-okthanoli
 2-Ortanol-molekyyli. Lähde: Jü [julkinen verkkotunnus], Wikimedia Commons
2-Ortanol-molekyyli. Lähde: Jü [julkinen verkkotunnus], Wikimedia Commons Se on rasva alkoholi. Se on väritön neste, vähän liukoinen veteen, mutta liukoinen useimmissa ei -polaarisissa liuottimissa. Sitä käytetään muun muassa makujen ja tuoksujen, maalausten ja pinnoitteiden, musteiden, liimojen, kotitaloushoidon ja voiteluaineiden kehittämisessä.
Estradioli tai 17p-stradioli
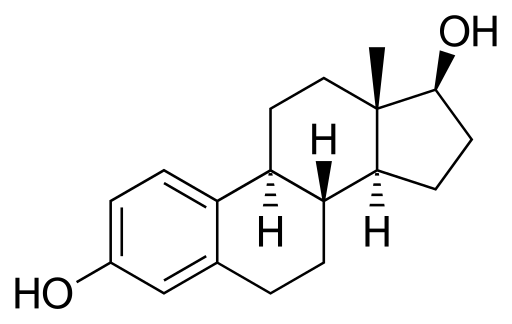 Estradiolimolekyyli. Lähde: Neurotogers [julkinen alue], Wikimedia Commons
Estradiolimolekyyli. Lähde: Neurotogers [julkinen alue], Wikimedia Commons Se on steroidi seksuaalinen hormoni. Sillä on rakenteessaan kaksi hydroksilli -ryhmää. Se on vallitseva estrogeeni lisääntymisvuosina.
20-hydroksi-leukotrieeni
Se on metaboliitti, joka todennäköisesti johtuu leukotrieenilipidin hapettumisesta. Se luokitellaan leukotrieenikystinyyliksi. Nämä yhdisteet ovat tulehduksellisen prosessin välittäjiä, jotka vaikuttavat allergisen nuhan patofysiologisiin ominaisuuksiin.
2-heptanoli
Se on hedelmistä löytyvä alkoholi. Lisäksi sitä löytyy inkivääriöljystä ja mansikoista. Se on läpinäkyvä, väritön ja liukenematon veteen. Sitä käytetään useiden hartsien liuottimena ja puuttuu vaahdotusvaiheeseen mineraalien prosessoinnissa.
Viitteet
- Terveyden ja turvallisuuden tietosanakirja työssä. (S.F.-A. Alkoholit. [PDF]. Toipunut: insht.On
- Alkoholien rakenne ja luokittelu. Kemian librettexts. Palautettu: Chem.Librettexts.org

