Lämpökaavat ja yksiköt, ominaisuudet, miten mitataan, esimerkkejä

- 2865
- 412
- Juan Breitenberg V
Hän lämmitys Fysiikassa se on määritelty Lämpöenergia siirretty edellyttäen, että objektit tai aineet, jotka ovat eri lämpötilassa, asetetaan kosketukseen. Tämä energiansiirto ja kaikki siihen liittyvät prosessit ovat termodynamiikan tutkimuksen kohde, tärkeä fysiikan haara.
Lämpö on yksi monista muodoista, jotka käyttävät energiaa, ja yksi tutuimmista. Siksi on syytä kysyä mistä se tulee. Vastaus on atomeissa ja molekyyleissä, jotka muodostavat asian. Nämä asioiden sisällä olevat hiukkaset eivät ole staattisia. Voimme kuvitella ne pieninä tileinä, joita pehmeät jouset ovat yhdistäneet, kykenevät kutistumaan ja venyttämään helposti.
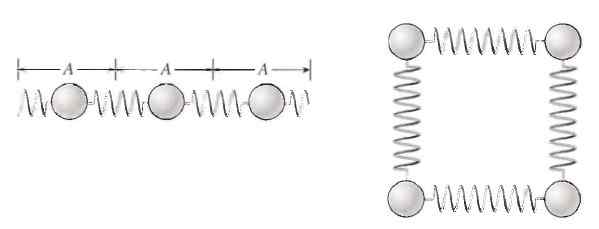 Atomit ja molekyylit värähtelevät aineiden sisällä, mikä tarkoittaa sisäistä energiaa. Lähde: P. Tippens. Fysiikka: Käsitteet ja sovellukset.
Atomit ja molekyylit värähtelevät aineiden sisällä, mikä tarkoittaa sisäistä energiaa. Lähde: P. Tippens. Fysiikka: Käsitteet ja sovellukset. Tällä tavoin hiukkaset kykenevät värisemään ja niiden energia voidaan siirtää helposti muihin hiukkasiin ja myös kehosta toiseen.
Kehon absorboivan tai tuoton lämmön määrä riippuu aineen luonteesta, sen massasta ja lämpötilaerosta. Se on laskettu näin:
Q = m.Cja .Δt
Missä Q - Se on siirretyn lämmön määrä, m Se on esineen massa, Cja Se on aineen erityinen lämpö ja Δt = tlopullinen - Talkukirjain, eli lämpötilaero.
Kuten kaikki energiamuodot, lämpö mitataan Joules, Kansainvälisessä järjestelmässä (SI). Muita asianmukaisia yksiköitä ovat: ergios CGS -järjestelmässä, Btu Ison -Britannian järjestelmässä ja kalori, yleinen käyttö termi ruoan energiapitoisuuden tuntemiseksi.
[TOC]
Lämpöominaisuudet
 Tulipalon lämpö on energiaa siirrossa. Lähde: Pixabay
Tulipalon lämpö on energiaa siirrossa. Lähde: Pixabay On olemassa useita keskeisiä käsitteitä, jotka on otettava huomioon:
-Lämpö on noin Energia kuljetuksessa. Esineillä ei ole lämpöä, ne antavat sen vain olosuhteen mukaan tai absorboivat sen. Mitä esineet tekevät sisäinen energia, Sen sisäisessä kokoonpanossa.
Tämä sisäinen energia puolestaan koostuu kineettisestä energiasta, joka liittyy värähtelyyn ja potentiaaliseen energiaan, tyypillinen molekyylikokoonpanolle. Tämän kokoonpanon mukaan aine siirtää lämmön helpommin ja tämä heijastuu sen erityisessä lämmössä Cja, Yhtälössä mainittu arvo Q: n laskemiseksi.
-Toinen tärkeä käsite on, että lämpö siirretään aina kuumimmasta kehosta kylmimpiin. Kokemus osoittaa, että kuuman kahvin lämpö kulkee aina kupin ja lautasen posliinia kohti tai lusikan metallia, jonka kanssa se on sekoitettu.
-Määritetyn tai absorboituneen lämmön määrä riippuu kyseisen kehon massasta. Lisää sama määrä kaloreita tai Joules -näytteitä, joissa on x taikina, ei kuumene toiseen, jonka massa on 2x.
Voi palvella sinua: Sähkömagneettiset aallot: Maxwell -teoria, tyypit, ominaisuudetSyy? Suurimmassa näytteessä on enemmän hiukkasia, ja jokainen vastaanottaisi keskimäärin vain puolet energiasta kuin pienin näyte.
Lämpötasapaino ja energiansäästö
Kokemus kertoo meille, että kun laitamme kaksi objektia eri lämpötilaan, molempien lämpötila on samaan aikaan. Sitten voidaan vahvistaa, että esineet tai järjestelmät, kuten niitä voidaan kutsua lämpötasapaino.
Toisaalta heijastaen eristetyn järjestelmän sisäisen energian lisäämistä, päätellään, että on olemassa kaksi mahdollista mekanismia:
i) lämmitä se, toisin sanoen energiaa toisesta järjestelmästä.
i) Tee jonkinlainen mekaaninen työ häntä kohtaan.
Kun otetaan huomioon, että energia säilyy:
Järjestelmän sisäisen energian lisääntyminen on yhtä suuri kuin lämmön määrä, joka lisätään enemmän siihen.
Termodynamiikan puitteissa tämä suojeluperiaate tunnetaan Termodynamiikan ensimmäinen laki. Sanomme, että järjestelmä on eristettävä, muuten muut sisäänkäynnin tai energiantuotokset tulisi harkita tasapainossa.
Kuinka lämpö mitataan?
Lämpö mitataan sen tuottaman vaikutuksen mukaan. Siksi kosketustunne ilmoittaa nopeasti, kuinka kuuma tai kylmä on juoma, ateria tai mikä tahansa esine. Sen jälkeen kun lämmön antaminen tai absorbointi muuttuu lämpötilan muutoksiin, tämän mittaamalla on käsitys siitä, kuinka paljon lämpöä se on siirretty.
Lämpötilan mittaamiseen käytetty instrumentti on lämpömittari, laite, joka on varustettu asteikolla lukemisen suorittamiseksi. Tunnetuin on elohopealämpömittari, joka koostuu hienosta elohopea kapillaarista, joka laajenee lämmittäessä.
 Lämpömittari, jonka valmistuminen on Celsius- ja Fahrenheit -asteikkoissa. Lähde: Pixabay.
Lämpömittari, jonka valmistuminen on Celsius- ja Fahrenheit -asteikkoissa. Lähde: Pixabay. Sitten kapillaari, joka on täynnä elohopeaa.
Mitä tarvitaan lämpömittarin tekemiseen?
Aluksi on välttämätöntä olla jonkin verran lämpömetristä ominaisuutta, ts. Yksi, joka vaihtelee lämpötilan mukaan.
Esimerkiksi kaasua tai nestettä, kuten elohopea, laajenee lämmittäessä, vaikka se palvelee myös sähkövastusta, joka emittoi lämpöä, kun se ylittää virtaa,. Lyhyesti sanottuna mitä tahansa helposti mitattavissa olevaa lämpömetristä ominaisuutta voidaan käyttää.
Jos lämpötila t on suoraan verrannollinen lämpömetriseen ominaisuuteen X, Sitten voit kirjoittaa:
t = kx
Missä k -k - Se on suhteellisuusvakio, joka määritetään, kun kaksi sopivaa lämpötilaa asetetaan ja vastaavat arvot X. Asianmukaiset lämpötilat ovat helppo saada laboratoriossa.
Voi palvella sinua: vino parabolinen laukaus: Ominaisuudet, kaavat, yhtälöt, esimerkitKun parit on perustettu (t1, X1) ja (t2, X2-A, Niiden välinen aika on jaettu yhtä suuriin osiin, nämä ovat arvosanoja.
Lämpötila -asteikot
Tarvittavien lämpötilojen valinta lämpötila -asteikon rakentamiseksi tehdään kriteerillä, että niitä on helppo hankkia laboratoriosta. Yksi maailman eniten käytetyistä asteikoista on ruotsalaisen tutkijan Anders Celsiuksen luoma Celsius-mittakaava (1701-1744).
Celsius -asteikon 0 on lämpötila, jossa jää ja nestemäinen vesi ovat tasapainossa 1 paine -ilmakehässä, kun taas ylempi pysäkki valitaan, kun nestemäinen vesi ja vesihöyry ovat yhtä tasapainossa ja 1 paine -ilmakehässä. Tämä aika on jaettu 100 asteeseen, joista jokaista kutsutaan tutkintotodistus.
Tämä ei ole ainoa tapa rakentaa asteikko, paljon vähemmän. On muitakin erilaisia asteikkoja, kuten Fahrenheit -asteikko, joissa on valittu väliajoja muiden arvojen kanssa. Ja siellä on Kelvin -asteikko, jolla on vain pienempi pysäkki: Absoluuttinen nolla.
Absoluuttinen nolla vastaa lämpötilaa, jossa jokainen aineiden hiukkasten liike loppuu kokonaan, vaikka se on ollut melko lähellä, mitään ainetta ei ole vielä jäähdytetty absoluuttiseen nollaan.
Esimerkit
Kaikki kokevat lämpöä päivittäin, joko suoraan tai epäsuorasti. Esimerkiksi, kun kuuma juoma otetaan, kun saadaan keskipäivä aurinko, tutkimalla auton moottorin lämpötilaa, huoneessa, joka on täynnä ihmisiä ja lukemattomissa tilanteissa.

Maapallolla lämpöä on välttämätöntä elämänprosessien ylläpitämiseksi, sekä se, joka tulee auringosta että se, joka jättää planeetan sisätilat.
Samoin ilmastoa ohjaavat ilmakehässä tapahtuvat lämpöenergian muutokset. Auringonlämpö ei saavuta yhtä suurta kuin kaikkialla, päiväntasaajan leveysaste saapuu enemmän kuin pylväät, joten trooppisten kuumin ilma nousee ja liikkuu pohjoiseen ja etelään, jotta saavutetaan lämpötasapaino, josta keskusteltiin aiemmin.

Tällä tavoin ilmavirrat on perustettu eri nopeuksilla, jotka kuljettavat pilviä ja sadetta. Toisaalta kuumien ja kylmien rintamien välinen äkillinen törmäys aiheuttaa ilmiöitä, kuten myrskyjä, tornadoja ja hurrikaaneja.
Toisaalta, lähempänä, lämpö ei ehkä ole yhtä tervetullut kuin auringonlasku rannalla. Lämpö aiheuttaa toimintaongelmia automoottoreissa ja tietokoneen prosessoreissa.
Voi palvella sinua: Watt Law: Mikä on, esimerkkejä, sovelluksiaSe aiheuttaa myös sähkön menettämisen kaapeleiden ja materiaalien laajentumisen suhteen, joten lämpökäsittely on niin tärkeä kaikilla tekniikan alueilla.
Harjoitukset
- Harjoitus 1
Candy -merkinnässä, joka lisää 275 kaloria. Kuinka paljon energiaa Joulesissa vastaa tätä karkkia?
Ratkaisu
Alussa kalori oli mainittu lämmön yksikönä. Ruoat sisältävät energiaa, joka yleensä mitataan näissä yksiköissä, mutta kalorit ovat todella kilokaloreita.
Vastaavuus on seuraava: 1 kcal = 4186 J, ja päätellään, että herkulla on:
275 kilokaloria x 4186 Joule/kilocaloria = 1.15 106 J -.
- Harjoitus 2
100 g kuumennetaan metalliin 100 ° C: seen ja asetetaan sen kalorimetriin 300 g vettä 20 ° C: ssa. Järjestelmän hankkima lämpötila, kun se saavuttaa tasapainon, on 21.44 ° C. Metallin erityinen lämpö pyydetään määrittämään, olettaen, että kalorimetri ei absorboi lämpöä.
Ratkaisu
Tässä tilanteessa metalli antaa lämpöä, jota kutsumme Q: ksiKiinnitys Ja merkki (-) asetetaan ennen tappion osoittamista:
Q -Kiinnitys = mmetalli .EYmetalli. Δt
Kalorimetrin vesi absorboi puolestaan lämpöä, joka merkitään absorboituna:
Q -imeytynyt = mvettä .EY vettä . Δt
Energia säilyy, josta seuraa, että:
Q -Kiinnitys = Qimeytynyt
Lauseesta, jonka voit laskea Δt-
Metalli: Δt = tlopullinen - Talkukirjain= (21.44 - 100) ºC = -78.56 ºC = -78.56 K.
Vesi: Δt = tlopullinen - Talkukirjain= (21.44 - 20) ºC = 1.44 ºC = 1.44 K.
Tärkeä: 1 ºC on samankokoinen kuin 1 Kelvin. Ero molempien asteikkojen välillä on, että Kelvin -asteikko on ehdoton (Kelvin -luokat ovat aina positiivisia).
Veden ominaislämpö 20 ºC: lla on 4186 j/kg. K ja tällä voit jo laskea absorboituneen lämmön:
Q -imeytynyt = mvettä .EY vettä . ΔT = 300 x 10-3 kg . 4186 J/kg . K -k - . 1.44 K = 1808.35 J.
Yhteenvetona voidaan todeta, että metallin erityinen lämpö puhdistetaan:
EY metalli = Q imeytynyt /-M metalli . ΔT metalli = 1808.35 J / -[(100 x 10-3 kg. (-78.56 k)] = 230.2 J/kg.K -k -
Viitteet
- Bauer, W. 2011. Fysiikka tekniikkaan ja tieteisiin. Osa 1. McGraw Hill.
- Cuellar, J.-Lla. Fisca II: Pätevyyslähestymistapa. McGraw Hill.
- Kirkpatrick, L. 2007. Fysiikka: Katsaus maailmaan. 6ta Lyhennetty painos. Cengage -oppiminen.
- Ritari, r. 2017. Tutkijoiden fysiikka ja tekniikka: strategialähestymistapa. Pearson.
- Tippens, P. 2011. Fysiikka: Käsitteet ja sovellukset. 7. painos. McGraw Hill
- « Aikaisemmat värit ominaisuudet ja merkitys
- Natriummetabisulfiitti (NA2S2O5) rakenne, ominaisuudet, käytöt, riskit »

