Centriolos -toiminnot ja ominaisuudet
- 3054
- 457
- Ronald Reilly

Se Centriolos Ne ovat lieriömäisiä solurakenteita, jotka koostuvat mikrotubulusryhmistä. Ne muodostuu tubuliiniproteiini, jota löytyy useimmissa eukaryoottisoluissa.
Associated Centriles -pari, jota ympäröi massaraportti tiheästä materiaalista, nimeltään pericentriololaarinen materiaali (PCM), säveltää rakenteen, jota kutsutaan keskukseksi.
Centriolien tehtävänä on ohjata mikrotubulusten kokoonpano, osallistuminen solujen organisaatioon (ytimen sijainti ja solun spatiaalinen asennus), flagellan ja silian (sylogeneesi) ja solujen jakautumisen (mitoosi ja meioosi) muodostuminen ja toiminta (mitoosi ja meioosi) ja toiminta).
Centrioloja löytyy solurakenteista, joita kutsutaan eläinsoluiksi, ja ne puuttuvat kasvisoluissa.
Kummankin solun keskipisteen tai keskuksen lukumäärän puutteilla voi olla merkittäviä vaikutuksia organismin fysiologiaan, mikä tuottaa muutoksia stressille tulehduksen, miesten hedelmättömyyden, neurodegeneratiivisten sairauksien ja tuumorin muodostumisen aikana.
Centriole on lieriömäinen rakenne. Pari niihin liittyvää keskipistettä, jota ympäröi massaraportti tiheästä materiaalista (nimeltään "percentriololaarinen materiaali" tai PCM), muodostaa yhdistelmärakenteen, jota kutsutaan "keskuksiksi".
He pitivät itseään merkityksettömänä muutama vuosi sitten, jolloin pääorganelit päätettiin solujen jakautumisen ja päällekkäisyyksien (mitoosin) toteuttamisessa eukaryoottisoluissa (pääasiassa ihmisissä ja muissa eläimissä).
Centriol
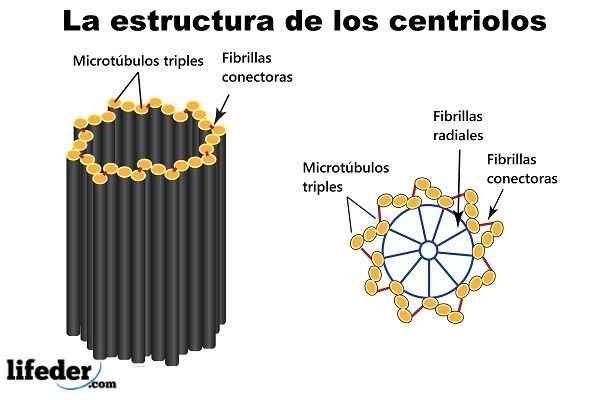
Yhdeksän mikrotubuluksen kolminkertaista kehälle järjestettyä (muodostaa lyhyt onton sylinteri) ympärille) ovat "rakennuslohkoja" ja keskipisteiden päärakenne.
Monien vuosien ajan keskipisteiden rakenne ja toiminta jätettiin huomiotta, vaikka 1880 -luvulla keskukset oli visualisoitu optisella mikroskopialla.
Theodor Boveri julkaisi vuonna 1888 perustetun teoksen, joka kuvaa siittiöiden keskuksen alkuperää hedelmöityksen jälkeen. Boveri kirjoitti lyhyessä viestinnässään vuonna 1887:
”Keskitys edustaa solun dynaamista keskustaa; Sen jakautuminen luo muodostettujen tytärsolujen keskukset, joiden ympärillä kaikki muut solukomponentit on järjestetty symmetrisesti ... keskukset ovat solun todellinen jakautumiselin, hän puolet ydin- ja solujen jakautumisesta ”(Scheer, 2014: 1). [Kirjoittajan käännös].
Pian vuosisadan puolivälin jälkeen Paul Schafer tutkittiin ja selitti elektronisen mikroskopian kehittymisen myötä elektronisen mikroskopian avulla.
Valitettavasti tätä työtä jätettiin huomiotta suurelta osin siitä, että tutkijoiden kiinnostus alkoi keskittyä Watsonin ja Krickin havaintoihin DNA: ssa.
Keskus

Pari keskipistettä, jotka sijaitsevat ytimen vieressä ja kohtisuorassa toisiinsa nähden, ovat "keskitys". Yksi keskipisteistä tunnetaan "isäksi" (tai äiti). Toinen tunnetaan "poika" (tai tytär; se on hiukan lyhyempi ja sen perusta on kiinnitetty äidin tukikohtaan).
Proksimaaliset päät (kahden keskipisteessä) on upotettu proteiinin "pilveen" (ehkä enintään 300 tai enemmän), joka tunnetaan nimellä MicroTubules Organisation Center (MTOC), koska se tarjoaa tarvittavan proteiinin rakentamiseen mikrotutkimukset.
Voi palvella sinua: tutkimuksen elinkelpoisuusMTOC tunnetaan myös nimellä "pericentriololaarinen materiaali", ja sillä on negatiivinen kuorma. Käänteisesti distaaliset päät (kaukana kahden keskipisteestä) on positiivisesti ladattu.
Centrioles -pari yhdessä ympäröivän MTOC: n kanssa tunnetaan nimellä "keskusta".
Keskusten päällekkäisyys
Kun keskipisteet alkavat kopioida, isä ja poika erottuvat hiukan ja sitten jokainen keskiosa alkaa muodostaa uuden Centriolon tukikohtaansa: isä uuden pojan kanssa ja poika uuden pojan kanssa ("pojanpoika", "pojanpoika" -A.
Vaikka keskiosan päällekkäisyys tapahtuu, ydin -DNA on myös kopioinut ja erotettu. Toisin sanoen nykyinen tutkimus osoittaa, että keskiosa ja DNA: n erottaminen ovat jotenkin linkitettyjä.
Päällekkäisyys ja solujen jako (mitoosi)

Mitoottinen prosessi kuvataan usein aloitusvaiheessa, joka tunnetaan nimellä "rajapinta", jota seuraa neljä kehitysvaihetta.
Rajapinnan aikana keskiosat kaksinkertaistuvat ja erottuvat kahteen pariin (yksi näistä ikätovereista alkaa liikkua ytimen vastakkaisella puolella) ja DNA on jaettu.
Centriolien päällekkäisyyden jälkeen keskipisteiden mikrotubulukset ulottuvat ja kohdistuvat ytimen pääakselia pitkin, muodostaen "mitoottisen karan".
Ensimmäisessä kehitysvaiheesta (vaihe I tai ”profas”) kromosomit tiivistyvät ja lähestymistapa, ja ydinkalvo alkaa heikentyä ja liukenemista. Samanaikaisesti mitoottinen kara muodostuu Centriol -parien kanssa, jotka sijaitsevat nyt karan päissä.
Toisessa vaiheessa (vaihe II tai "metafaasi") kromosomiketjut ovat linjassa mitoottisen karan akselin kanssa.
Kolmannessa vaiheessa (vaihe III tai "anafaasi") kromosomaaliketjut jaetaan ja siirtyvät kohti mitoottisen karan vastakkaisia päätä, nyt pitkänomaisia.
Lopuksi, neljännessä vaiheessa (vaihe IV tai ”telfaasi”) muodostuu uusia ydinkalvoja erillisten kromosomien ympärillä, mitoottinen kara on tekemättä ja soluerottelu alkaa valmistua puolella sytoplasmasta, joka kulkee jokaisen uuden ytimen kanssa.
Mitoottisen karan molemmissa päissä keskipistepareilla on tärkeä vaikutus (ilmeisesti liittyvät voimiin, jotka aiheuttavat sähkömagneettiset kentät, jotka ovat tuottaneet niiden proksimaalisten ja distaalisten päiden negatiiviset ja positiiviset kuormat) koko solun jakautumisen solussa.
Keskukset ja immuunivasteet
Stressi -altistuminen vaikuttaa organismin elämän toimintaan, laatuun ja kestoon. Esimerkiksi infektion aiheuttama syntynyt stressi voi johtaa tartunnan saaneiden kudosten tulehdukseen, aktivoimalla immuunivaste kehossa. Tämä vaste suojaa sairastua vartaloa, poistaen taudinaiheuttajan.
Monet immuunijärjestelmän toiminnallisuuden näkökohdat tunnetaan hyvin. Kuitenkin molekyyli-, rakenteelliset ja fysiologiset tapahtumat, joissa keskukset ovat edelleen arvoitus.
Voi palvella sinua: Koe -raporttiViimeaikaiset tutkimukset ovat löytäneet odottamattomia dynaamisia muutoksia keskuksien rakenteessa, sijainnissa ja toiminnassa stressiin liittyvissä olosuhteissa. Esimerkiksi infektion olosuhteiden jäljitelmän jälkeen on löydetty PCM -tuotannon ja mikrotubulusten lisääntyminen rajapintasoluissa.
Immuunisynapsissa olevat keskukset
Keskuksilla on erittäin tärkeä rooli immuunisynapsien rakenteessa ja toiminnassa (SI). Tämä rakenne muodostuu erikoistuneilla vuorovaikutuksilla T -solun ja antigeenin välillä, joka esittelee solua (CPA). Tämä solu-soluvuorovaikutus alkaa keskittyä kohti SI: tä ja sen myöhempää kytkemistä plasmamembraaniin.
Keskikytkentä Si: ssä on samanlainen kuin sylogeneesin aikana havaittu. Tässä tapauksessa se ei kuitenkaan aloita silian kokoonpanoa, vaan osallistuu SI: n organisointiin ja sytotoksisten rakkuloiden eritystä kohdesolujen lisariin.
Keski- ja lämpörasitus
Keskustat ovat "chaperonas -molekyyli" (proteiinisarja, jonka tehtävänä on auttaa kokoonpanoa ja muiden proteiinien solujen kuljetusta), jotka tarjoavat suojaa altistumiselta lämpöiskun ja stressin suhteen.
Keskuksiin vaikuttavien stressitekijöiden joukossa mukana on DNA: n ja lämmön vauriot (kuten kuumeiset potilassolut). DNA -vaurio alkaa DNA: n korjausreiteistä, jotka voivat vaikuttaa keskuksien ja proteiinikoostumuksen toimintaan.
Lämmön aiheuttama stressi aiheuttaa keskipisteiden rakenteen, keskuksien häiriöiden ja sen kyvyn muodostamisen kokonaisen inaktivoinnin muuttamisen, mitoottisen karan muodostumisen muuttaminen ja myitoosin estäminen.
Keskusten toiminnan keskeyttäminen kuumeessa voisi olla adaptiivinen reaktio karan pylväiden inaktivoimiseksi ja DNA: n epänormaalin jakautumisen estämiseksi mitoosin aikana, etenkin kun otetaan huomioon useiden proteiinien mahdolliset toimintahäiriö.
Se voisi myös tarjota solun takaisin funktionaalisen proteiinipoolin palauttamiseksi ennen solunjaon uudelleen aloittamista.
Toinen seuraus keskittymisen inaktivoinnista kuumeessa on sen kyvyttömyys siirtyä siihen, että se on organisoida ja osallistua sytotoksisten rakkuloiden eritykseen.
Centrioles -epänormaali kehitys
Centriolon kehitys on prosessi.
Jos proteiinien osuudessa on epätasapaino, Centriolon lapsi voi olla viallinen, sen geometria voidaan vääristää, parin akselit voivat poiketa kohtisuorisuudesta, useita lapsia voi kehittyä, Centriole -poika voi saavuttaa koko pituuden ennen aikaa, aikaa,, tai irrotusparit voivat viivästyä.
Se voi palvella sinua: luonnollinen ja sosiaalinen ympäristö ihmisen tarpeiden tyydyttämisessäKun keskipisteitä on väärä tai virheellinen päällekkäisyys (geometrisillä vikoilla ja / tai useilla päällekkäisyyksillä), DNA: n replikaatio muuttuu, esitetään kromosomaalinen epävakaus (CIN) (CIN).
Samoin keskuksen keskukset (esimerkiksi laajentunut tai laajennettu keskitys) johtavat CIN: hen ja edistävät useiden centrioles -lasten kehitystä.
Nämä kehitysvirheet aiheuttavat vaurioita soluille, jotka voivat jopa johtaa pahanlaatuiseen.
Epänormaalit keskipisteet ja pahanlaatuiset solut
Sääntelyproteiinien intervention ansiosta, kun poikkeavuuksia havaitaan keskittymisessä ja/tai keskittämisessä, solut voivat toteuttaa poikkeavuuksien itsekorjauksen.
Jos poikkeavuuden, epänormaalien keskipisteiden tai useiden lasten kanssa ("ylimääräiset keskipisteet" voidaan saavuttaa) itsekorjaus voi kuitenkin johtaa kasvaimien ("tuumorigeneesi") tai solukuoleman luomiseen.
Ylimääräiset keskipisteet yleensä kokoontuvat, mikä johtaa keskuksien ryhmittelyyn ("keskukset monistus", syöpäsoluille), muuttamaan solujen napaisuutta ja mitoosin normaalia kehitystä, mikä johtaa kasvainten esiintymiseen.
Soluilla, joilla on ylimääräisiä keskipisteitä.
On ehdotettu, että syöpäsolujen keskipisteiden tai keskuksien klusterit voisivat toimia "biomarkkerina" terapeuttisten ja mielikuvituksen agenttien, kuten superparamagneettisten nanohiukkasten, käytössä.
Viitteet
- Borisy, g., Heald, r., Howard, J., Janke, c., Musacchio, a., & Nogales, ja. (2016). Mikrotubulukset: 50 vuotta tubuliinin löytämisestä. Luontokatsaukset Molecular Cell Biology, 17 (5), 322-328.
- Buchwalter, r. -Lla., Chen, J. V., Zheng, ja., & Megraw, t. Lens. Solujen jakautumisen, kehityksen ja sairauden keskukset. hols.
- Gambarotto, D., & Basto, R. (2016). Numeeristen keskuksien käsitteet kehityksen ja sairauden puutteet. Mikrotubuluskystoskeleton (PP. 117-149). Springer Wien.
- Huston, R. Lens. (2016). Katsaus centriolia aktiivisuuteen ja laittomaan aktiivisuuteen solun jakautumisen aikana. Biotieteen ja biotekniikan edistysaskeleet, 7 (03), 169.
- Inaba, k., & Mizuno, K. (2016). Siittiöiden toimintahäiriöt ja siliopatia. Lisääntymislääketiede ja biologia, 15 (2), 77-94.
- Keeling, j., Tsiokas, L., & Maskey, D. (2016). Siliaarin pituuden hallinnan solumekanismit. Solut, 5 (1), 6.
- Loodish, h., Berk, a., Kaiser, c. -Lla., Krieger, m., Bretscher, a., Ploegh, H., AMON, a., Martin, k. C. (2016). Molekyylisolubiologia. New York: W. H. Freeman ja yritys.
- Matamoros, a. J -., & Baas, P. W -. (2016). Hermoston terveyden ja rappeuttavan sairauden mikrotubulit. Brain Research Bulletin, 126, 217-225.
- Pellegrini, L., Wetzel, a., Grannó, S., Heaton, G., & Harvey, k. (2016). Takaisin putkiin: Mikrotubulusten dynamiikka Parkinsonin taudissa. Solu- ja molekyylieläintieteet, 1-26.
- Scheer, u. (2014). Keskustutkimuksen historialliset juuret: Boverin mikroskoopin liukujen löytäminen Würzburgissa. Phil. Trans. R -. Soc. B, 369 (1650), 20130469.

