Ytimen elektroninen konfiguraatiorakenne, esimerkkejä
- 4743
- 1057
- Arthur Terry II
Se Ytimen elektroninen kokoonpano tai kompakti on se, joiden kvanttimerkinnät elektronien lukumäärästä ja niiden energia -ala -tasot lyhenevät jalokaasujen symboleissa. Se on erittäin hyödyllinen kirjoittaessasi tietyn elementin sähköisiä kokoonpanoja, koska se on yksinkertainen ja nopea.
Sana 'ydin' viittaa yleensä atomin elektronisiin sisäkerroksiin; Toisin sanoen ne, joissa heidän elektronit eivät ole Valenciasta, eivätkä siksi osallistu kemialliseen sidokseen, vaikka ne määrittelevät elementin ominaisuudet. Metaforisesti ottaen ydin olisi sipulin sisustus, ja sen kerrokset koostuvat kasvavista kiertoradaista energiassa.
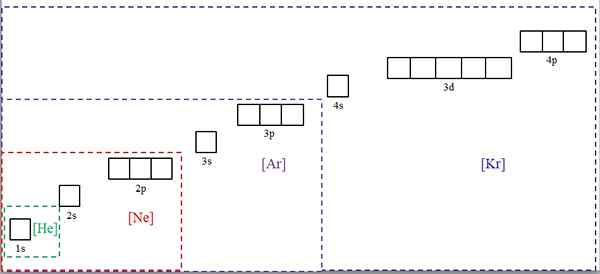
 Elektroniset kokoonpanot lyhennettynä jalokaasujen symboleilla. Lähde: Gabriel Bolívar.
Elektroniset kokoonpanot lyhennettynä jalokaasujen symboleilla. Lähde: Gabriel Bolívar. Ylivoimainen kuva näyttää kemialliset symbolit neljälle jalokaasulle neliömäisissä sidoksissa ja eri väreillä: [he] (vihreä), [ne] (punainen), [ar] (violetti) ja [kr] (sininen) (sininen) (sininen).
Jokainen sen katkoviiva sisältää ruutuja, jotka edustavat kiertorataa. Mitä suurempi, sitä suurempi on sisältävien elektronien lukumäärä; mikä puolestaan tarkoittaa, että useamman elementtien elektroniset kokoonpanot voidaan yksinkertaistaa näillä symboleilla. Tämä säästää aikaa ja energiaa kirjoittamalla kaikki merkinnät.
[TOC]
Rakennustilaus
Ennen ytimen elektronisten kokoonpanojen käyttöä on kätevää tarkistaa oikea järjestys näiden kokoonpanojen rakentamiseksi tai kirjoittamiseksi. Tätä säätelee diagonaalisen säännön tai Moeller -kaavion mukaan (kutsutaan sateen joihinkin osiin). Kun tämä kaavio on käsillä, kvanttimerkinnät pysyvät seuraavasti:
1S 2S 2P 3S 3P 4S 3D 4P 5S 4D 5P 6S 4F 5D 6P 7S 5F 6D 7P
Voi palvella sinua: perussuolat: kaava, ominaisuudet, nimikkeistö, esimerkitTämä kvanttimerkintöjen rivi näyttää uupuneelta; Ja olisi vieläkin enemmän, jos joudut kirjoittamaan sen kaikkien aikojen edustamiseksi minkä tahansa ajanjakson 5 alkaen elementtien elektronisen kokoonpanon. Huomaa, että rivi on tyhjä elektroneista; Korkeamman oikeuksien oikeuksissa ei ole numeroita (1s22s22 p6…).
On muistettava, että kiertoradat s voi "isännöidä" kahta elektronia (NS2-A. Orbitaalit p Kaikkia on kolme (katso kolmea yllä olevaa laatikkoa), joten ne voivat isännöidä kuusi elektronia (NP6-A. Ja lopuksi, kiertoradat d -d Niitä on viisi, ja F seitsemän, jolla on yhteensä kymmenen (nd10) ja neljätoista (NF14) vastaavasti elektronit.
Elektroninen konfiguraation lyhenne
Tästä huolimatta kvanttimerkintöjen eturivi on täynnä elektroneja:
1s2 2s2 2 p6 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Kuinka monta elektronia on yhteensä? 118. Ja mikä elementti vastaa niin massiivista määrää elektroneja sen atomiin? Noble Oganese Gas, OG.
Oletetaan. Sitten sen Valencia -elektroninen kokoonpano olisi 8s1; Mutta mikä olisi sen täydellinen sähköinen kokoonpano?
1s2 2s2 2 p6 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6 8s1
Ja mikä olisi ytimen elektroninen kokoonpanosi, kompakti? Tämä:
[OG] 8s1
Huomaa ilmeinen yksinkertaistaminen tai lyhenne. Symbolissa [OG] Kaikki edellä kirjoitetut 118 elektronia lasketaan, joten tässä epävarmassa elementissä on 119 elektronia, joista vain yksi on Valenciasta (se sijaitsee francion alla jaksollisessa taulukossa).
Voi palvella sinua: mikä on tyydyttynyt ratkaisu? (Esimerkkejä)Esimerkit
Yleinen
Oletetaan nyt, että haluat suorittaa lyhenteen asteittain:
[He] 2s2 2 p6 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Huomaa, että 1s2 Se korvattiin [hän]. Seuraava jalokaasu on neon, jossa on 10 elektronia. Tietäen tämän, lyhenne jatkuu:
[Ne] 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Seuraa sitten argonia 18 elektronilla:
[AR] 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Koska seuraava jalokaasu on Kripton, vielä 36 elektronia on edistynyt:
[KR] 5s2 4D10 5 p6 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Ksenonilla on 54 elektronia, ja siksi siirrämme lyhenteen 5P: n kiertoradalle:
[Xe] 6s2 4F14 5 D10 6P6 7s2 5F14 6D10 7P6
Tässä vaiheessa elektroninen kokoonpano lyhennetään aina NP -kiertoradalle; Eli jalokaasuilla on nämä orbitaalit täynnä elektroneja. Ja seuraa lopuksi radonia 86 elektronilla, joten lyhentemme 6p -kiertoradan:
[RN] 7s2 5F14 6D10 7P6
Happi
Happella on kahdeksan elektronia, jotka ovat sen täydellinen elektroninen kokoonpano:
1s22s22 p4
Ainoa lyhenne, jota voimme käyttää, on [hän] 1: llä2. Siten sen ytimen elektroninen kokoonpano on:
[He] 2s22 p4
Kalium
Kaliumissa on yhdeksäntoista elektronia, jotka ovat sen täydellinen elektroninen kokoonpano:
Voi palvella sinua: mistä muovi tulee? Historia ja tyypit1s2 2s2 2 p6 3s2 3P6 4S1
Huomaa, että voimme käyttää symbolia [hän] lyhentääksesi tätä kokoonpanoa; samoin kuin [ne] ja [ar]. Jälkimmäinen on mitä käytetään, koska argon on jalo kaasu, joka edeltää sitä lähinnä kaliumia. Siksi sen ytimen elektroninen kokoonpano on edelleen:
[AR] 4S1
intialainen
Intialaisella on neljäkymmentä -naista elektronia, jotka ovat sen täydellinen elektroninen kokoonpano:
1s2 2s2 2 p6 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p1
Koska Kripton on lähin jalokaasu, joka edeltää intialaista, käytetään lyhenteen [KR] -symbolia, ja sen ytimen elektroninen kokoonpano on:
[KR] 5s2 4D10 5 p1
Vaikka 4D -orbitaalit eivät kuulu virallisesti Intian ytimeen, niiden elektronit eivät puutu (aina.
Volframi
Volframissa (tai Wolframio) on 74 elektronia ja sen täydellinen elektroninen kokoonpano on:
1s2 2s2 2 p6 3s2 3P6 4S2 3D10 4P6 5s2 4D10 5 p6 6s2 4F14 5 D4
Etsimme jälleen lähintä jalokaasua. Hänen tapauksessaan se vastaa Xenónia, jonka 5p -kiertoradalla on valmis. Siten korvaamme kvanttimerkintöjen rivin symbolilla [xe], ja meillä on vihdoin sen ytimen elektroninen kokoonpano:
[Xe] 6s2 4F14 5 D4
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Pat Thayer. (2016). Elektronien kokoonpanokaaviot. Palautettu: ChemistryApp.org
- Helmestine, Anne Marie, PH.D -d. (5. joulukuuta 2018). Jalokaasun ytimen määritelmä. Toipunut: Admingco.com/
- Wikipedia. (2019). Elektroninen kokoonpano. Palautettu: on.Wikipedia.org
- « Uraanin diskohistoria ja laulajat, jotka ovat voittaneet sen
- Tuskegeen kokeiluhistoria, motiivit ja kritiikki »

