Erityiset viat
- 2535
- 277
- Shawn Stanton II
Mitkä ovat erityiset viat?
Täsmälliset viat ovat epätäydellisyyksiä tai epäsäännöllisyyksiä, jotka on esitetty kiinteän kiteisessä retikulumissa ja jotka poikkeavat sen täydellisen tilan kiteistä rakennetta. Sanotaan, että heillä ei ole ulottuvuutta (0), koska ne ovat vain kiteisen retikulumin pisteitä; Tämä kohta voi olla atomi, ioni, molekyyli, klusterit jne.
Kiinteät aineet lämpötilassa 0 K (absoluuttinen nolla) on täydellisiä rakenteita, koska teoriassa sen komponentit immobilisoidaan, jäädytetään. Atomeja on kuitenkin tuskin ladattu, sanoen, ne alkavat värähtyä, mikä päätyy ennemmin tai myöhemmin liikkumaan vastaavien sivustojensa ulkopuolelle.
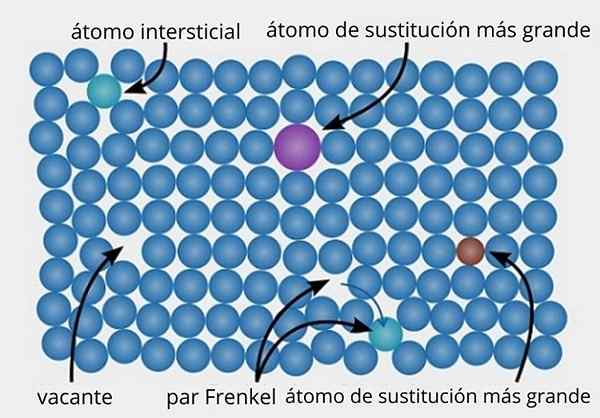
 Erityyppisten spesifisten vikojen esitys, jota löytyy kiteistä kiinteistä aineista. Lähde: Daniferi, CC BY-Sa 3.0, Wikimedia Commons
Erityyppisten spesifisten vikojen esitys, jota löytyy kiteistä kiinteistä aineista. Lähde: Daniferi, CC BY-Sa 3.0, Wikimedia Commons Katsotaanpa ylempi kuva esimerkkinä. Kaikki sinertävät kohdat tulisi kohdistaa järjestetyssä ja täydellisessä kiteisessä rakenteessa. Jotkut sinertävät pisteitä voi kuitenkin puuttua, mikä havaitaan tyhjän tilan tai avoimuuden läsnäololla.
Jos mainitun avoimen työpaikan muodostuminen johtuu sen alkuperäisen sivuston sinertävän pisteen siirtämisestä, meillä on pari Frenkel, yksi olemassa olevien tiettyjen vikojen tyypistä. Mobilisoitu sinertävä kohta on nyt interstitiaalisessa (vihreässä) asennossa.
Toisaalta spesifiset viat voivat johtua myös substituutioista, joko suuremmista (violetista) atomeista tai pienemmistä (ruskeista) atomeista (ruskea). Puhumme korvaavista erityisvaurioista, jotka tapahtuvat monta kertaa, kun epäpuhtaudet otetaan käyttöön tarkoituksella (dopped) metalli- ja keraamisissa materiaaleissa.
Täsmälliset viat ovat välttämättömiä muihin lasin mitoihin projisoidut muut viat.
Luontaiset spesifiset viat
Kun kiteinen rakenne on aina määritelty, se tehdään aina ihanteesta. Mutta luonnossa viat ovat väistämättömiä, riippumatta siitä, kuinka pienet ne ovat. Siten kiinteiden aineiden taipumus on luonnollinen taipumus esiintyä rakenteissaan olevia spesifisiä vikoja, joiden vuorovaikutus ja summaus vaikuttaa niiden kemiallisiin ja fysikaalisiin ominaisuuksiin. SO -nostetut luontaiset spesifiset viat tapahtuvat "puhtaissa" materiaaleissa.
Tämä luonnollinen taipumus johtuu termodynaamisista ja kineettisistä tekijöistä. Vian aiheuttaminen lisää kiinteän aineen entropiaa, mikä puolestaan kasvaa lämpötilan kanssa. Sitten tietyssä lämpötilassa millä tahansa kiinteällä tavalla on tila, jolla on minimi tiettyjen vikojen kokoonpano.
Lämpötilan noustessa on vielä enemmän vikoja, sillä se on suurin mahdollinen määrä sulamispisteen läheisyydessä. Kaikki tämä on järkevää, jos ajatellaan, että suuremmille lämpövärähtelyille suurempi on mahdollisuudet, että atomit luopuvat heidän vastaavista retikulaarisista asemistaan.
Pisteen ulkoiset viat
Toisin kuin luontaiset spesifiset viat, ulkoiset virheet tapahtuvat epäpuhtauksien sisällyttämisen vuoksi. Mikään luonteeltaan kiinteä kiinteä ei ole 100% puhdasta, joten tämäntyyppiset viat ilmenevät aina luontaisen lisäksi.
Voi palvella sinua: glukonihappo: rakenne, ominaisuudet, synteesi, käyttöNe kuitenkin veloittavat ainutlaatuisen merkityksen ja kiinnostuksen, kun epäpuhtauksia lisätään tarkoituksellisesti laiminlyönnissä; Puhumme materiaalista tyhmä.
Doponten ja valitun materiaalin ominaisuuksista riippuen viat sisällytetään kiinteään aineeseen ennakoidulla tavalla, jolla on vaikutusta sen kemiallisiin ja fysikaalisiin ominaisuuksiin. Näin on puolijohdeformulaation, esimerkiksi GAAS.
Toisaalta ulkoiset spesifiset viat viittaavat myös niihin, jotka muokkaavat materiaalien tai kiinteiden aineiden koostumusta. Eli he menettävät stökiometriansa tullakseen ei -stoikiometriksi kiinteiksi aineiksi.
Täsmälliset metallivirheet
Metalleissa meillä on kiteitä, joilla periaatteessa puuttuu sähkömaksu; Eli läsnä ei ole kationeja tai anioneja, vaan vain metalli -neutraaliatomeja. Joten metalleissa olevat puutteet eivät vaikuta niiden puolueettomuuteen, joten mikään mekanismi ei olisi mekanismia, joka kompensoi tällaisia vikoja.
 Sisäiset spesifiset viat hypoteettisen metallin kiteissä. Lähde: Gabriel Bolívar.
Sisäiset spesifiset viat hypoteettisen metallin kiteissä. Lähde: Gabriel Bolívar. Yllä olevassa kuvassa meillä on täydellinen kristalli ja kaksi muuta vikoista. Atomit voivat sijaita interstitiaalisissa asennoissa, jotka häiriöt naapuriatomien asemat ja tunnetaan itsehallintovirheeksi (alla keskellä). Samaan aikaan jotkut atomit kykenevät luopumaan kiteisen järjestelyn kohteista avoimien työpaikkojen tuottamiseksi (oikealla).
Siksi puhtaissa metalleissa avoimien työpaikkojen ja itsehallintojen luontaisten vikojen olemassaolo on mahdollista. Mitä enemmän avointa työpaikkaa siellä aineen tiheys vähenee; tosiasia, joka on linjassa lämpötilan vikojen määrän lisääntymisen kanssa.
Kun toisaalta annetaan metalli, jolla on toisen elementin atomit, ne aiheuttavat korvauksia tai pyrkivät sijoittamaan itsensä väliin. Tällaisissa tapauksissa metallitiheys nousee maksimiarvoon, josta se alkaa laskea rajusti.
Kiteisten rakenteiden spesifiset viat
Kiteisissä rakenteissa, jotka peittävät muita kiinteitä aineita edellä mainittujen metallien lisäksi, meillä on kahta päätyyppiä erityisiä vikoja: Frenkel ja Schottky. Molemmat voivat esiintyä samoilla kristallin alueilla, ja on myös täysin mahdollista, että niitä esiintyy yhdessä avoimien vaurioiden tai interstitiaalisten ammattien kanssa.
Kun puhumme suoloista, oksideista, sulfaateista jne., Siellä on kationien ja anionit, jotka määrittelevät kide sen sähköstaattisista vuorovaikutuksista. Siksi, jos poistamme kationin, anionien negatiiviset kuormat ovat vallitsevia, ja lasi ladataan negatiivisesti. Tätä on mahdotonta esiintyä, koska se rikkoisi elektroneutraation periaatetta.
Siten tämän tyyppisten kiteiden puutteet tuottavat sähkövarauksia, jotka mekanismin avulla on sovittava uudelleen. Frenkelin ja Schottkyn puutteet eivät kuitenkaan tuota tätä sähkömaksujen epätasapainoa.
Voi palvella sinua: vastaavuuspisteFrenkel
 Frenkelin täsmällinen vikaesitys. Lähde: Gabriel Bolívar.
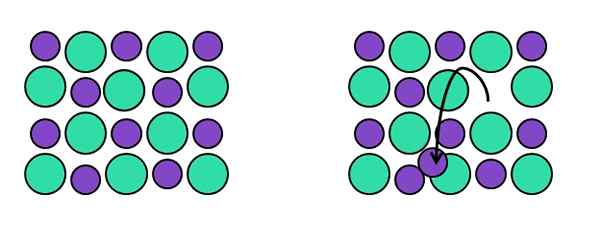
Frenkelin täsmällinen vikaesitys. Lähde: Gabriel Bolívar. Farm -Ran -Time Frenkel, Yakov Frenkelin kunniaksi, retikulaarinen piste jättää alkuperäisen asemaansa päättyä interstitiumissa. Eli atomi, molekyyli tai ioni siirtyy interstitiaaliseen asemaan jättäen avoimen työpaikan.
Katso yllä olevasta kuvasta. Vasemmalla puolella meillä on täydellinen kide, joka koostuu kahdesta ionista: yksi vihreä, joka on ordinarit anionille (enemmän tilaa vievä) ja violetti, josta tulee kationi (pienempi).
Kun yksi violetista kationeista jättää kiteisen järjestelyn sijainnin, jättää avoimen työpaikan taaksepäin. Huomaa vasemmalla suuntaan, johon musta nuolipiste on osoittanut, että kationi sijaitsee nyt interstitiumissa.
Koska Frenkelin vika koostuu kationin siirtymistä (tai anioneista), lasi pysyy neutraalina. Myös lasin koostumus pysyy vakiona, koska retikulumissa ionit muuttavat asentoja: ne eivät hylkää sitä, eivätkä muut lisää siihen.
Schottky
 Schottky -vian esitys. Lähde: Gabriel Bolívar.
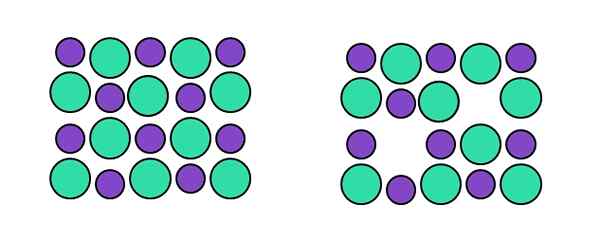
Schottky -vian esitys. Lähde: Gabriel Bolívar. Erityisessä schoottky -tyypissä meillä on kaksi samanaikaista avointa työpaikkaa: toinen vastaa kationia ja toinen vastaa anionia vastaava. Esimerkiksi, kyse ei ole kationista interstitiaalisen aseman brinquen, vaan että se "katoaa" anionin mukana (ylemmän kuvan oikealla).
Jälleen kerran, kun kaksi avointa työpaikkaa luodaan samanaikaisesti, kationinen (joka käyttäytyy kuin anionia) ja anioninen (joka käyttäytyy kuin kationi), kiteen koostumus pysyy muuttumattomana. Tämä on niin kauan kuin tämäntyyppinen vika puhuu, eikä ulkoisten tai sisäisten tekijöiden aiheuttamat mielivaltaiset avoimet työpaikat.
Kaikista edellä mainituista on päätelty, että Frenkelin ja Shottkyn viat ovat luontaisia pisteitä -stökiometrisiä vikoja, koska ne eivät muuta kiinteiden aineiden koostumusta tai stökiometriaa.
Keraamisten materiaalien täsmälliset viat
Keramiikka on materiaaleja, joiden ioninen luonne on hyvin värähtelevä. Jotkut esittävät huomattavan kovalenttisen hahmon, kuten piidioksidissa, sit2, tai alumiinin nitrolla, alnalla.
Siksi meidän on tarkasteltava kahta muun tyyppistä erityistä virhettä, joita voi tapahtua keramiikan kovalenttisen luonteen tuotena: antitium ja tyydyttymätön linkki.
Antisitium
Kuten nimensä päättelee, virhe, joka tapahtuu, kun kaksi atomia muuttavat heidän sivustonsa, ollessaan alkuperäisen kiteisen retikulumin vastaisesti. Esimerkiksi SIC: ssä voi tapahtua, että on C-C tai Si-If, missä ei pitäisi. Tämäntyyppinen täsmällinen vika on myös hyvin yleinen seoksissa:
Voi palvella sinua: Alumiinifosfuro (AIP): rakenne, ominaisuudet, käytöt, riskit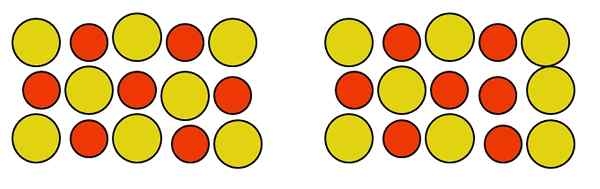 Täsmällinen antisitiumvika au-cu-seoksessa. Lähde: Gabriel Bolívar.
Täsmällinen antisitiumvika au-cu-seoksessa. Lähde: Gabriel Bolívar. Huomaa, että kupari- ja kultatomit Au-How-seoksessa ovat neutraaleja. Riippumatta siitä, kuinka ne liikkuvat, lasin puolueettomuutta ei häiritä. Siksi kaksi atomia vaihtavat lasin kohtaa, kuten yllä olevan kuvan oikealla puolella, se ei vaikuta seoksen puolueettomuuteen.
Keramiikassa, jossa on useampi kuin yksi kationi, kuten spiners, kaksi kationilla, joilla on yhtä suuri valenssi voi vaihtaa sivustoa (esimerkiksi3+ ja cr3+) ilman sähkömaksujen epätasapainoa.
Tyydyttymätön linkki
Tyydyttämätön linkki (roikkuva sidos englanniksi) keskeyttää kovalenttisen keramiikan kiteissä järjestyksen, koska linkin muodostava atomi on puuttuva, jättäen pari vapaata elektronia.
Keramiikassa annetaan antitium- ja ei -tyydyttymättömien linkkien viat, vaan myös kaikki sisäiset ja ulkoiset viat, joten on monimutkaista analysoida niiden todellisia, ei täydellisiä rakenteita.
Esimerkkejä tietyistä virheistä
Koko artikkelissa on mainittu esimerkkejä materiaaleista ja niiden erityisistä virheistä. Seuraavaksi ja lopuksi, muut materiaalit luetellaan, liitteenä niistä tyypistä, jota ne yleensä esiintyvät.
Hopeahalidesia
Hopeahalidesit, kuten AGCL tai AGBR, esiintyvät Frenkel -virheet missä agkaatio+ Se siirtyy interstitiaalisiin asentoihin.
Emäksinen haluros
Alkaliset halogenidit, kuten NaCl, ilmenevät Schottky -vikoja, joiden anioniset avoimet työpaikat täytetään elektroneilla, kun niiden kiteitä kuumennetaan natriumin tai metallisten kaliumhöyryjen läsnä ollessa.
Torio -dioksidi
Tho2 Kation th4+ on enemmän tilaa vievää kuin anionia tai2-. Siksi tällä oksidilla on frenkel -vika, missä se on2- joka siirtyy interstitiaalisiin asentoihin.
Paladio Sponge
Paladium kykenee absorboimaan vetyä käyttäytymällä kuin sieni, joka pitää ne kiteidensä interstitiaalisiin asentoihin.
Teräkset
Samoin kuin paladiumin ja vedyn välillä, rauta voi sisällyttää hiiliatomeja sen väliintuloihin, mikä johtaa terästen muodostumiseen.
Titaaniseokset
Korvaava täsmällinen vika, vaikka sitä ei ole selitetty muina vikoina, ei ole muuta kuin yhden atomin korvaaminen toiselle, joka rikkoutuu kristallin asettamalla järjestyksellä.
Siten esimerkiksi titaanikiteisen atomit voidaan korvata muilla atomilla (metalli) aiheuttamaan titaaniseosten perheen.
Viitteet
- Barry Carter & M. Grant Norton. (2007). Keraamiset materiaalitieteet ja tekniikka. Jousto.
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- B -.S.H. Royce. (S.F.-A. Pistehuutot. Toipunut: Princeton.Edu
- Wikipedia. (2020). Kristallografinen vika. Haettu: vuonna.Wikipedia.org
- Nayak, s.K -k -., Ripustettu, c.J -., Sharma, V. et al. (2018). Näkemys pistehuonteista ja epäpuhtauksista titaanissa ensimmäisistä periaatteista.NPJ Computer Ma 4.11. doi.org/10.1038/S41524-018-0068-9
- Byju. (2020). Pistehuutot. Toipunut: byjus.com

