Deuterium
- 4250
- 213
- Gustavo Runte DVM
Mikä on deuterium?
Hän deuterium Se on yksi isotooppisista vetylajeista, joka on esitetty d tai 2H. Lisäksi raskaan vedyn nimi on annettu, koska sen massa on kahdesti protonin nimi. Isotooppi on laji, joka tulee samasta kemiallisesta elementistä, mutta jonka massamäärä on erilainen kuin tämä.
Tämä ero johtuu sen neutronien lukumäärän eroista. Deuteriumia pidetään stabiilina isotooppina, ja sitä voidaan löytää yhdisteistä, jotka muodostuu luonnollisesta vedystä, vaikkakin melko pienessä osassa (alle 0,02 %).
Ottaen huomioon sen ominaisuudet, jotka ovat hyvin samanlaisia kuin tavallisen vedyn ominaisuudet, se voi korvata vedyn kaikissa reaktioissa, joihin se osallistuu, ja niistä tulee vastaavia aineita.
Tästä ja muista syistä tällä isotoopilla on paljon sovelluksia eri tieteen aloilla, ja siitä tulee yksi tärkeimmistä.
Deuteriumrakenne
Deuteriumin rakenne muodostuu pääasiassa ytimestä, jossa on protoni ja neutroni, jonka atomipaino tai massa on noin 2 014 g.
Samoin tämä isotooppi velkaa havainnon Harold C: lle. Urey, kemisti Yhdysvalloista ja sen yhteistyökumppanit Ferdinand Brickwedde ja George Murphy, vuonna 1931.

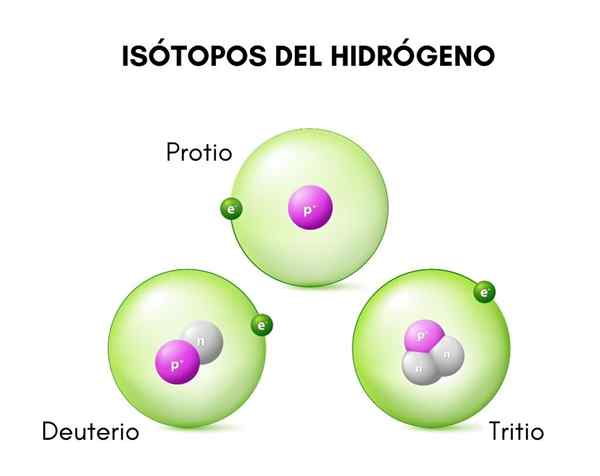
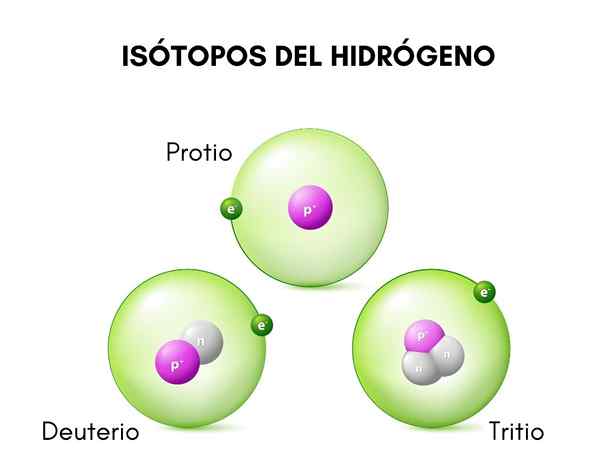
Yläkuvassa voit nähdä vertailun vety -isotooppien rakenteiden välillä, joita esiintyy protiomuodossa (sen runsain isotooppi), deuterium ja tritium, tilattu vasemmalta oikealle.
Deuteriumin valmistus puhtaaseen tilaan suoritettiin onnistuneesti ensimmäistä kertaa vuonna 1933, mutta 1950 -luvulta lähtien on käytetty kiinteän faasiaineen ja se on osoittanut stabiilisuutta, jota kutsutaan litium deuteridiksi (LID), deuteriumin ja tritiumin korvaamiseksi In Stauteriumissa ja tritiumissa in Stauterium ja tritium suuri määrä kemiallisia reaktioita.
Voi palvella sinua: kloorioksidi (III): Ominaisuudet, rakenne, käyttöTässä mielessä tämän isotoopin runsautta on tutkittu ja on havaittu, että sen osuus vedessä voi vaihdella hieman riippuen siitä, mistä näyte otetaan.
Lisäksi spektroskopiatutkimusten avulla tämän galaksin muihin planeettoja on määritetty tämän isotooppin olemassaolo.
Joitain tietoja deuteriumista
Perusero vetyjen isotooppien välillä (jotka ovat ainoat, jotka on nimetty eri tavoin) on niiden rakenteessa, koska lajin protonien ja neutronien määrä antaa sen kemialliset ominaisuudet.
Toisaalta tähtimarjojen sisällä oleva olemassa oleva deuterium poistetaan nopeammalla nopeudella kuin on peräisin.
Lisäksi katsotaan, että muut luonnon ilmiöt muodostavat vain hyvin pienen määrän sitä, joten sen tuotanto jatkaa kiinnostusta nykyään.
Samoin tutkimussarja on paljastanut, että suurin osa tästä lajista muodostuneista atomeista on peräisin isosta räjähdyksestä; Tästä syystä sen läsnäolo suurilla planeetoilla, kuten Jupiter.
Yleisin tapa saavuttaa tämä laji luonnossa on, kun se yhdistetään vedyn kanssa proto -muodossa, tiedeyhteisön kiinnostusta herättää edelleen molempien lajien osuuden välinen suhde eri tieteenaloilla, sellainen tähtitiede tai sää.
Voi palvella sinua: Renio: Löytö, ominaisuudet, rakenne, käyttötarkoituksetDeuterium -ominaisuudet
- Se on isotooppi, josta puuttuu radioaktiiviset ominaisuudet; eli se on luonteeltaan melko vakaa.
- Sitä voidaan käyttää vetyatomin korvaamiseen kemiallisissa reaktioissa.
- Tämä laji ilmenee muun käyttäytymisen kuin tavallisen vedyn biokemiallisissa reaktioissa.
- Kun kaksi vetyatomia korvataan vedessä, D saadaan2Tai hankkimalla raskaan veden nimen.
- Deuteriumin muodossa oleva valtameressä läsnä oleva vety on suhteessa 0,016 % suhteessa ProTioon.
- Tähteissä tällä isotoopilla on taipumus sulauttaa nopeasti heliumin aiheuttamiseksi.
- D -d2Tai muodostaa myrkyllisiä lajeja, vaikka sen kemialliset ominaisuudet ovat hyvin samanlaisia kuin H2
- Kun deuterium -atomeja altistetaan ydinfuusioprosessilla korkeissa lämpötiloissa, saadaan suurten energiamäärien irrottaminen.
- Fysikaalisilla ominaisuuksilla, kuten kiehumispiste, tiheys, höyrystymislämpö, kolminkertainen piste, on muun muassa suuria suuruuksia deuteriummolekyyleissä (D2) että vedyssä (H2-A.
- Yleisin tapa, jolla se löytyy.
Käyttää/sovelluksia
Ominaisuuksiensa vuoksi deuteriumia käytetään monenlaisissa sovelluksissa, joissa vetyä on mukana. Joitakin näistä käyttötarkoituksista on kuvattu alla:
- Biokemian alalla sitä käytetään isotooppisessa merkinnässä, joka koostuu "merkitsemisestä" näytteestä, jonka isotooppi on valittu seuraamaan sitä läpi tietyn järjestelmän läpi.
Voi palvella sinua: vahva happo- Fuusioreaktioita toteuttavissa ydinreaktoreissa sitä käytetään vähentämään neutronien liikkuvan nopeutta ilman näiden suurta imeytymistä, joita tavallinen vety esittelee.
- Ydinmagneettiresonanssin (NMR) alueella käytetään deuteriumiin perustuvia liuottimia, jotka saavat tämän tyyppisen spektroskopian näytteitä ilman häiriöitä, jotka tuotetaan käyttämällä hydratettuja liuottimia.
- Biologian alalla makromolekyylejä tutkitaan neutronidispersiotekniikoiden avulla, joissa käytetään deuteriumilla toimitettuja näytteitä vähentämään merkittävästi näissä kontrastiominaisuuksissa.
- Farmakologia -alueella deuterium käyttää vedyn korvaamista kineettisen isotooppisen vaikutuksen kanssa, joka syntyy ja antaa näille lääkkeille pidemmän puolen ajanjakson.