Energiakaavio
- 1834
- 112
- Edgar VonRueden
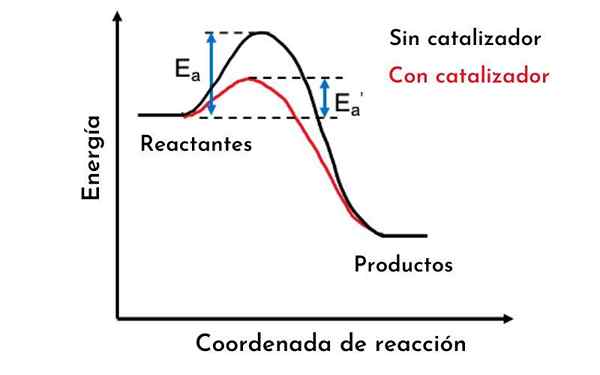
 Energiakaavio, joka osoittaa aktivointienergian vähenemisen katalyyttillä. Lähde: Emma Ambrogi, CC BY-SA 4.0, Wikimedia Commons
Energiakaavio, joka osoittaa aktivointienergian vähenemisen katalyyttillä. Lähde: Emma Ambrogi, CC BY-SA 4.0, Wikimedia Commons Mikä on energiakaavio?
Eräs energiakaavio Se on energiakaavio, joka kuvaa prosessia, joka tapahtuu koko reaktion ajan. Energiakaaviot määritellään myös orbitaalien elektronisen kokoonpanon visualisoinniksi: jokainen esitys on orbitaalin elektroni nuolella.
Esimerkiksi energiakaaviossa nuolet, jotka pisteet ylemmässä suunnassa, edustavat elektronia, jolla on positiivinen käännös. Päältä alaspäin olevat nuolet ovat vastuussa elektronin edustamisesta negatiivisella käännöksellä.
Energiakaavioita on kahta tyyppiä. Termodynaamiset tai orgaaniset kemiakaaviot, jotka osoittavat reaktiota tuotetun tai käytetyn energian määrän, alkaen, koska elementit löytyvät reagensseista siirtymätilan kautta tuotteisiin.
Ja epäorgaaniset kemian kaaviot, jotka osoittavat molekyyliorbitaalit, riippuen atomien energian tasosta.
Energiakaavioiden ominaisuudet
- Ne ovat erikoistuneita kaavioita, jotka vaativat valmistelua.
- Jokainen kaaviossa esiintyvä esitys on orbitaalin elektroni nuolella.
- Niiden on mitattava aineen erilaisia energiatiloja (termodynamiikka), kuten tilavuus ja paine.
- Niitä voidaan käyttää lääketieteellisellä alueella, kuten sydän- ja verisuonifysiologia, hengitysfysiologia tai termodynaaminen fysiologia.
- Ne muodostavat apua elementin tuottaman energian mittaamiseen, ja siksi niillä on sovellus kvanttimekaniikassa, koska ne osoittavat atomienergiatasoja.
Energiakaaviotyypit
Termodynaamiset kaaviot
Termodynaamisia kaavioita käytetään edustamaan aineen termodynaamisia tiloja (tyypillisesti nesteitä) ja tämän materiaalin manipuloinnin seurauksia.
Voi palvella sinua: kuinka kauan Red Bullin vaikutus viimeksi?Esimerkiksi entrooppista lämpötilakaaviota voidaan käyttää nesteen käyttäytymisen osoittamiseen, kun se muuttuu kompressoriksi.
Sankey -kaaviot ovat energiakaavioita, joissa nuolien paksuus esitetään suhteessa virtauksen määrään.
Tämä kaavio edustaa tehtaan koko ensisijaista energiavirtausta. Kaistan paksuus on suoraan verrannollinen tuotannon, käytön ja tappioiden energiaan.
Primaarienergialähteet ovat kaasu, sähkö ja hiili/öljy, ja ne edustavat energian pääsyä kaavion vasemmalle puolelle.
Energiakulut, materiaalin virtaus alueellisella tai kansallisella tasolla ja elementin tai palvelujen kustannusten hajoaminen voidaan myös visualisoida.
Nämä kaaviot korostavat visuaalisesti suuria energiasiirtoja tai virtauksia järjestelmässä.
Ja ne ovat erittäin hyödyllisiä, kun sijoitetaan hallitseva panos yleisessä virtauksessa. Usein nämä kaaviot osoittavat säilyneitä määriä määritellyn järjestelmän rajoissa.
P-V-kaavio
Sitä käytetään kuvaamaan järjestelmän tilavuus- ja painemittauksia vastaavia muutoksia. Niitä käytetään yleisesti termodynamiikassa, sydän- ja verisuonifysiologiassa ja hengitysfysiologiassa.
P-V-kaavioita kutsuttiin alun perin indikaattoreiksi. Niitä kehitettiin 1800 -luvulla työkaluina höyrykoneiden tehokkuuden ymmärtämiseksi.
P-V-kaavio näyttää paineen P muutoksen suhteessa joidenkin prosessien tai prosessien V: n määrän suhteen.
Termodynamiikassa nämä prosessit muodostavat syklin siten, että syklin kulkulla järjestelmän tilassa ei tapahdu muutosta, kuten laitteessa, joka palaa sen alkuperäiseen paineeseen ja tilavuuteen.
Voi palvella sinua: ihminenT-S-kaavio
Sitä käytetään termodynamiikassa spesifisen lämpötilan ja entropian muutoksen visualisoimiseksi termodynaamisen prosessin tai syklin aikana.
Se on erittäin hyödyllinen ja erittäin yleinen työkalu alueella, etenkin siksi, että se auttaa visualisoimaan lämmönsiirtoa prosessin aikana.
Palautuvien tai ihanteellisten prosessien kohdalla prosessin T-S-käyrän alla oleva alue on järjestelmälle siirretty lämpö prosessin aikana.
Isentrooppinen prosessi on graafinen kuin pystysuora viiva T-S-kaaviossa, kun taas isoterminen prosessi on graafinen vaakasuora viiva.
Epäorgaaniset kemian kaaviot
Ne edustavat atomiin ja niiden energiatasoon liittyviä molekyyliorbitaaleja tai shematiloida.
Potentiaalinen energiakaavio ETA: sta
Etaanin eri konformaatioilla ei ole samaa energiaa, koska niillä on erilainen elektroninen torjunta hydrogenien välillä.
Kun molekyyli kääntyy, alkaen jo vuorottelevasta konformaatiosta, tietyn metyyliryhmien vetyatomien välinen etäisyys alkaa vähentää. Järjestelmän potentiaalinen energia kasvaa, kunnes se saavuttaa varjostetun konformaation.
Erityyppisiä energiatyyppejä voidaan esittää graafisesti eri konformaatioiden keskuudessa. Etaanikaaviossa havaitaan, kuinka varjostetut konformaatiot ovat maksimaalisia energiaa. Toisaalta varajäsenet olisivat minimi.
Esimerkkejä energiakaavioista
T-S-kaavio
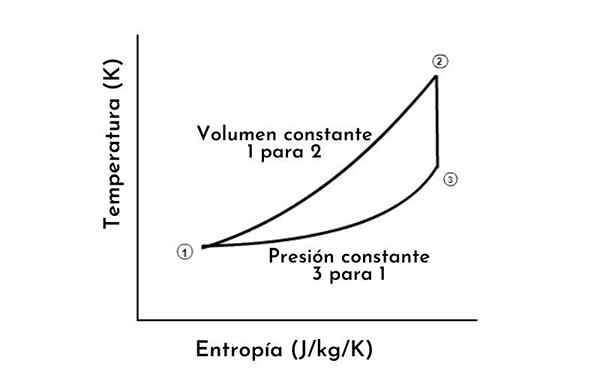 T-S-kaavio
T-S-kaavio P-V-kaavio
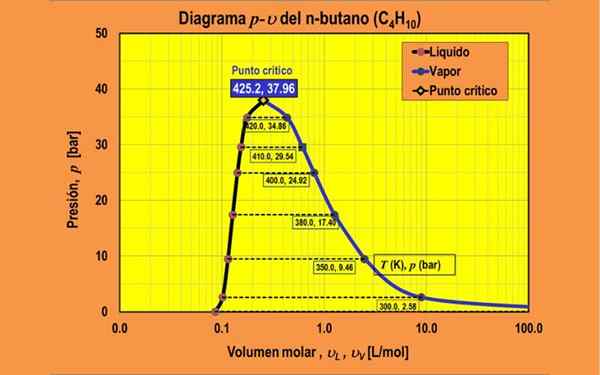 P-V-kaavio. Lähde: Josearortino, CC BY-SA 4.0, Wikimedia Commons
P-V-kaavio. Lähde: Josearortino, CC BY-SA 4.0, Wikimedia Commons Se on n-butaani P-V-kaavio.
Etan -kaavio
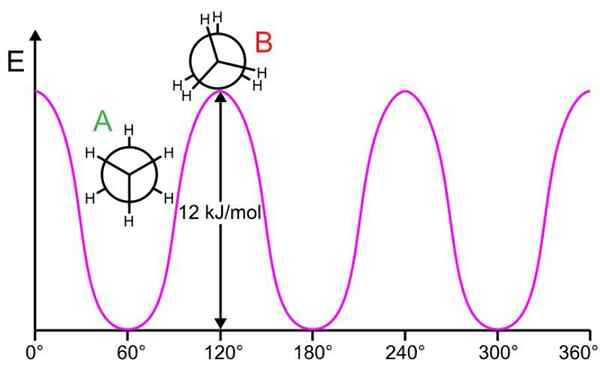 Etan -kaavio. Lähde: Kministi, Wikimedia Commons
Etan -kaavio. Lähde: Kministi, Wikimedia Commons Tämä kaavio osoittaa Newmanin ennusteet ETA: n konformaatioista ja niiden suhteellisista energiaeroista (ei kokonaisenergiat). Kun etaani kiertää yhden kovalenttisen sidoksensa ympärillä, nämä konformaatiot muodostuvat. Vääntö-/diedral kulma on esitetty x -akselilla.
Se voi palvella sinua: tsunamin kaksi pääasiallista syytäV: Escoado / B: Pimennys
Viitteet
- T-S-kaavio. Haettu jstk.Wikipedia.org
- Sankey -kaavio. Haettu jstk.Wikipedia.org

