Elektrodialyysi miten toimii, edut, haitat, käyttää
- 898
- 37
- Mr. Clifford Kshlerin
Se Elektrodialyysi Se on ionin liike jälkiversiokelpoisen kalvon läpi, jota ohjaa sähköpotentiaaliero. Elektrodialyysissä käytetyillä kalvoilla on ominaisuus olla ioninvaihtimia kationeille tai anioneille.
Kationinvaihtokalvoilla on negatiiviset kuormat: ne antavat kationien ohittaa ja hylätä anionit. Sillä välin anionisilla vaihtokalvoilla on positiivinen varaus: ne antavat anionit ja hylkäävät kationit.
 Viiden elektrodialyysisolujen pakkauksen kaavio. Lähde: Commonshelper2 Wikipedian kautta.
Viiden elektrodialyysisolujen pakkauksen kaavio. Lähde: Commonshelper2 Wikipedian kautta. Elektrodialyysikamerat tai solut on järjestetty pakkauksiin, joissa on useita anioni- ja kationisia vaihtokalvoja, jotka vuorotellen toistensa kanssa. Anioniset ja kationiset vaihtamiskalvot rajaavat tilat, joissa nesteiden laimennus- ja pitoisuusprosessit suoritetaan.
Elektrodialyysisolujen kalvojen ylittävien ionisten virtausten käyttövoima on ero katodin ja anodin välissä sähköpotentiaalissa.
Samaan aikaan käänteisosmoosissa veden virtaus osastosta suurimmalla osmolaarisuudella alempaan osmolaarisuusosastoon johtuu hydrostaattisen paineen noususta, joka johtuu pumpun vaikutuksesta.
[TOC]
Miten toimii veden laimennuksessa?
Kuvaus viiden elektrodialyysisolujen pakkauksesta
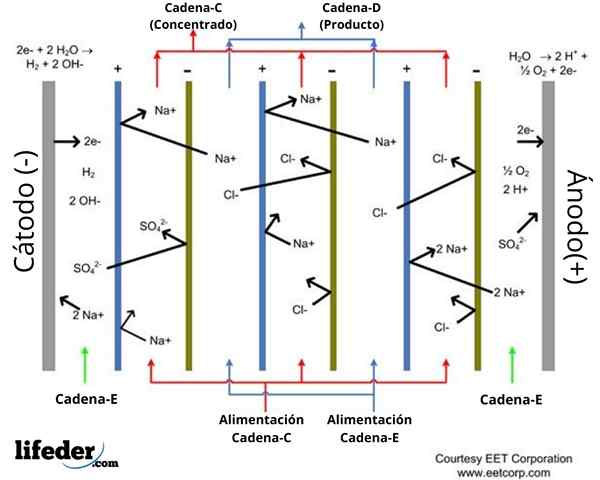
Esitetyssä järjestelmässä (ylivoimainen kuva) kuuden ioninvaihtokalvon sijainti on osoitettu: kolme kationinvaihtoa ja kolme anioninvaihtoa, jotka ovat välissä toistensa kanssa. Nämä kalvot rajaavat viisi osastoa, joissa elektrodialyysiin osallistuvat nesteet kiertävät (katso punaiset ja sinertävät nuolet).
Anioniset vaihtokalvot ladataan positiivisesti, ja ne esiintyvät sinisenvärisessä järjestelmässä. Ne antavat anionien kulkea ja torjuvat kationit sähköstaattisen torjuntaa varten.
Kationinvaihtokalvoilla on negatiivinen kuorma, joka osoittaa vihreän kaavion. Kationit ylittävät ne, mutta hylkäävät anionit.
Se voi palvella sinua: Testi: Ominaisuudet, tyypit, esimerkit käytöstäMolemmat kalvotyypit ovat vedenpitäviä veteen. Kaaviossa on kaksi tilaa, joissa tapahtuu veden suolaliuospitoisuuden laimennus. Kaaviossa näiden tilojen pääsyn ja poistumisen vesipitoiset virtaukset on merkitty sinisellä, tunnistettu nykyiseksi D.
Samaan aikaan on kolme tilaa, joissa vesi kiertää korkealla suolaliuoksella, ja se on tunnistettu punaiseksi. Tulot ja poistumisvirrat näihin osastoihin on ilmoitettu järjestelmässä nykyisenä C.
Samoin anodi (+) ja katodi (-) -osastot on merkitty kaaviossa, jonka kautta virta ja.
Elektrodialyysioperaatio
Kationit houkuttelevat katodin (-) kuorma, kun taas hylättiin anodi (+). Anodin (+) kuorma houkuttelee anodit ja katodin kuormitus (-).
Esimerkiksi kolmen, neljän ja viiden solujen havainto osoittaa seuraavat: soluissa kolme ja viisi kiertää konsentroitua nestettä, kun taas solussa neljä nestettä kiertää.
Ion cl- osastosta neljä houkutellaan anodin kuorma ja ylittää anionisen vaihtokalvon, joka erottaa sen osastosta viisi.
Samaan aikaan Na -ioni+ osastosta viisi hylätään anodin positiivinen kuorma, mutta se ei pääse osastoon neljää. Tämä johtuu siitä, että neljäs ja viisi osastoja erottava kalvo on anionista vaihtoa, joten se hylkää kationit.
Toisaalta na+ Anodi (+) hylkää neljän osaston neljä ja ylittää kationinvaihtokalvon (-), joka erottaa sen osastosta kolme.
Yhteenveto: NA -pitoisuus+ ja cl- Neljä osastoa pyrkii vähentymään. Sitten suolaliuospitoisuus vähenee laimennusosastoissa ja lisääntyy pitoisuusosastoissa.
Se voi palvella sinua: Sovellettu kemia: Opiskelua, oksat, merkitys, esimerkitHyödyt ja haitat
Edut
-Elektrodialyysi on yksinkertaista ja jatkuvaa toimintaa.
-Kemiallista käsittelyä ei vaadita vaihtokalvojen uudistamiseen.
-Käyttö- ja ylläpitokustannukset ovat alhaiset, mikä vaatii vähän tilaa sen toimintaan.
Haitat
-Hiukkaset, joiden halkaisija on yli 1 um, voivat estää ioninvaihtokalvoja.
-Vettä ei suositella käyttämään suurempaa kovuutta, koska kalsiumkarbonaatti luo kuoren konsentraattisoluihin.
-Vaatii hiilidioksidin eliminointikäsittelyä (CO2), koska tämä dissosioitumisen yhteydessä voi muokata veden johtavuutta.
Ero dialyysin ja elektrodialyysin välillä
Dialyysi on veden virtaus pienemmän osmolaarisuuslokeron puolijalkaisen kalvon läpi suurempaan osmolaarisuuslokeroon. Osastolla, jolla on vähemmän osmolaarisuus, on suurempi vesimolekyylipitoisuus.
Tästä syystä vesi virtaa osaston pitoisuusgradientin hyväksi vähemmän osmolaarisuuteen osastoon suuremmalla osmolaarisuudella.
Elektrodialyysi puolestaan on ionien virtaus ioninvaihtokalvon kautta, joka antaa tai ei siirtyä ioneihin, sen sähkövarauksesta riippuen. Ioniliikkeen liikkeellepaneva voima on ero sähköpotentiaalissa.
Toisin kuin dialyysi, elektrodialyysissä ei ole veden virtausta kalvojen läpi ja ionivirtausta on vain.
Elektrodialyysisovellukset
Veden demineralisaatio
On elektrodialyysikasveja, jotka käsittelevät vettä korkeilla suoloilla juomaveden tuottamiseksi. Elektrodialyysiä käytetään myös kotimaisen ja teollisuuden käytön jäteveden käsittelemiseen, jotta ne sopivat seuraaviin kulutuksiin.
Se voi palvella sinua: Erlenmeyer -pullo: ominaisuudet, käytöt, käyttötavatTarkemmin. Sitä käytetään myös suolojen ja happoliuosten poistamiseen sekä neutraalien molekyylien ionisten yhdisteiden erottamiseen.
Ruokateollisuus
Vaikka elektrodialyysiä käytetään lääketeollisuudessa, kosmetiikassa ja muilla aloilla, sen laajin käyttö on elintarviketeollisuudessa. Minkä tahansa sovelluksen joukossa voimme mainita seuraavat:
-Seerumin ja melassin smineralisaatio
-Viinihapon stabilointi
-Hedelmämehujen happamuuden väheneminen
-Eristettyjen vihannesproteiinien tuotanto
-Seerumin proteiinien epäonnistuminen
-Soija- ja kalaöljyjen demineralisaatio
-Juurikkaiden emäksisten ionien ja sokeriruo'on melassin eliminointi
-Äyriäiset jätteenkäsittely
-Rypäleen demineralisaatio ja perunamehu
-Orgaanisten happojen pitoisuus ja talteenotto
-Soijaproteiinin tuotanto
-Antioksidantin rikastuminen
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Wikipedia. (2020). Elektrodialyysi. Haettu: vuonna.Wikipedia.org
- Lentech b.V. (2020). Mikä on EDI? Toipunut: lentech.com
- Mondor m., Ipperiel d., Lamarche f. (2012) Elektrodialyysi elintarvikkeiden jalostuksessa. Julkaisussa: boye j., Arcand ja. (toim.) Vihreät tekniikat elintarvikkeiden tuotannossa ja jalostuksessa. Elintarviketosarja. Springer, Boston, MA. doi.org/10.1007/978-1-4614-1587-9_12
- Akhter M, Habib G, Qamar His (2018) Elektrodiasiksen levitys jätevedenkäsittelyssä ja likaantumisen vaikutus prosessin suorituskykyyn. J Memb Sci Technol 8: 182. Doi: 10.4172/2155-9589.1000182
- H. Strathmann. (6. joulukuuta 2006). Elektrodiasis ja sen soveltaminen kemian prosessiteollisuudessa. Taylor & Francis verkossa. doi.org/10.1080/03602548508068411
- « Kolmannen henkilön piirtämisominaisuudet ja esimerkit
- 8 esimerkkiä merkityksellisimmistä graafisista resursseista »

