Glykosidi -linkki mikä on, ominaisuudet, tyypit, nimikkeistö
- 4819
- 243
- Edgar VonRueden
Se Glykosidiset linkit Ne ovat kovalenttisia sidoksia, joita esiintyy sokerien (hiilihydraattien) ja muiden molekyylien välillä, jotka voivat olla muita monosakkarideja tai muita monipuolisia molekyylejä.
Nämä yhteydet tekevät mahdolliseksi useiden perustavanlaatuisten komponenttien olemassaolon paitsi varantopolttoaineiden ja rakenneosien muodostumisessa, myös olennaisten tietojen kuljetusmolekyylien kanssa soluviestinnässä.
Polysakkaridien muodostuminen riippuu pohjimmiltaan glykosidisten sidosten muodostumisesta alkoholien tai yksittäisten monosakkaridiyksiköiden vapaiden hydroksyyliryhmien välillä.
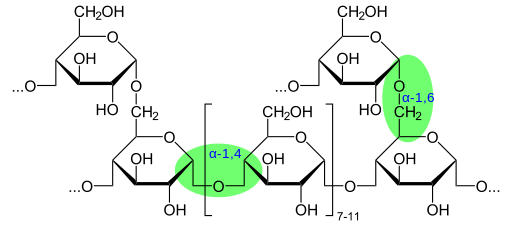 Glykosidinen sidosesimerkki glykogeenissä (lähde: Glykogen.SVG-neurotkerrivatiivi-työ-Marek-M-Public-Domeen Wikimedia Commons -sovelluksen kautta)
Glykosidinen sidosesimerkki glykogeenissä (lähde: Glykogen.SVG-neurotkerrivatiivi-työ-Marek-M-Public-Domeen Wikimedia Commons -sovelluksen kautta) Glykosidiset yhteydet esiintyvät useissa soluympäristöissä, mukaan lukien joidenkin sfingolipidien polaarisen pään ryhmän liitokset, monien organismien solukalvojen välttämättömät aineosat sekä glykoproteiinien ja proteoglykaanien muodostuminen.
Tärkeät polysakkaridit, kuten selluloosa, kitiini, agar, glykogeeni ja tärkkelys, eivät olisi mahdollisia ilman glukosidisia sidoksia. Samoin proteiinien glykosylaatio, joka tapahtuu endoplasmisessa retikulumissa ja Golgi -kompleksissa, on erittäin tärkeää monien proteiinien aktiivisuudelle.
Ominaisuudet
Glykosidiset sidokset ovat paljon monimuotoisempia kuin niiden analogit proteiineissa ja nukleiinihapoissa, koska periaatteessa kaksi sokerimolekyyliä voivat liittyä toisiinsa monin tavoin, koska niillä on useita ryhmiä -OH, jotka voivat osallistua linkin muodostumiseen.
Lisäksi monosakkaridien isomeerit, toisin sanoen yksi kahdesta suuntauksesta, joka hydroksyyliryhmällä voi olla syklisessä rakenteessa anomeerisen hiilen suhteen, tarjoavat ylimääräisen monimuotoisuuden tason.
Isomeereilla on erilaiset kolme dimensionaalista rakennetta sekä erilaisia biologisia aktiivisuuksia. Selluloosa ja glykogeeni koostuvat toistuvista D-glukoosin yksiköistä, mutta eroavat glukosidisidoksen tyypistä (α1-4 glykogeenille ja β1-4 selluloosille), ja siksi niillä on erilaiset ominaisuudet ja toiminnot.
Aivan kuten polypeptideillä on polaarisuus toisella päällä N- ja toisella c- ja polynukleotideilla on 5 'ja 3' päätä, oligo-tai polysakkaridit on polaarisuus määritelty vähentämällä päätä ja eivät vähennä.
Pelkistävässä päässä on vapaa anomerinen keskus, joka ei muodosta glykosidista yhteyttä toiseen molekyyliin, joten se säilyttää aldehydin kemiallisen reaktiivisuuden.
Voi palvella sinua: ulkoinen hedelmöitysGlukosidinen sidos on oligo-tai polysakkarin joustavin alue.
Glykosidinen sidosmuodostus
Glukosidinen sidos voi liittyä kahteen monosakkaridimolekyyliin yhden ja toisen hydroksyyliryhmän kautta. Toisin sanoen yhden sokerin hemiasetaaliryhmä reagoi toisen alkoholiryhmän kanssa asetaalin muodostamiseksi.
Yleensä näiden linkkien muodostuminen tapahtuu kondensaatioreaktioilla, joissa vesimolekyyli vapautuu jokaisella muodostetulla linkillä.
Joissakin reaktioissa happi ei kuitenkaan hylkää sokerimolekyyliä vetenä, vaan osana difosfaattiryhmän difosfaattiryhmää.
Reaktioita, jotka aiheuttavat glukosidisia yhteyksiä. Ne muodostuvat kovalenttisesti modifioidun sokerin välillä lisäämällä fosfaattiryhmää tai nukleotidia (esimerkiksi 6-fosfaattiglukoosi, UDP-galaktoosi), joka sitoutuu kasvuketjuun kasvavassa polymeerissä.
Glykosidisidoksen hydrolyysi
Glykosidiset sidokset voivat helposti hydrolysoitua hiukan happamissa ympäristöissä, mutta ne kestävät melko alkalisia ympäristöjä.
Glukosidisten sidosten entsymaattista hydrolyysiä välittyy glykosidaasina tunnetuilla entsyymeillä. Monilla nisäkkäillä ei ole näitä entsyymejä selluloosan hajoamiseksi, joten ne eivät pysty purkamaan energiaa tästä polysakkaridista huolimatta siitä, että ne ovat välttämättömiä kuitulähteitä.
Esimerkiksi märehtijöillä, kuten lehmillä, on bakteereja, jotka liittyvät niiden suoliin, jotka tuottavat entsyymejä, jotka kykenevät hajottamaan syömänsä selluloosaa, mikä tekee heistä kykenevän hyödyntämään kasvikudoksissa säilytettyä energiaa.
Silmän kyynelissä ja joidenkin bakteerivirusten kyynelissä tuotettu sileä entsyymi kykenee tuhoamaan bakteerit hydrolyyttisen aktiivisuuden ansiosta, joka rikkoo glukosidisen sidoksen N-asetyyliglukosamiinin ja N-asetyylimuramihapon välillä soluseinämän soluseinämän välillä bakteerit.
Monimuotoisuus
Oligosakkaridit, polysakkaridit tai glykaanit ovat hyvin monimuotoisia molekyylejä, ja tämä johtuu monosakkaridista, joilla monosakkaridit voivat liittyä yhteen muodostamalla korkeamman asteen rakenteet.
Tämä monimuotoisuus alkaa tosiasiasta, kuten edellä mainittiin, että sokereissa on hydroksyyliryhmiä, jotka sallivat eri ammattiliittoalueet ja että sidokset voivat tapahtua kahden mahdollisen stereoisomeerin välillä sokerin anomeerisen hiilen (α tai β) välillä.
Voi palvella sinua: BlastozoosGlykosidiset yhteydet voidaan muodostaa sokerin ja minkä tahansa hydroksyloidun yhdisteen, kuten alkoholin tai aminohapon, väliin.
Lisäksi monosakkaridi voi muodostaa kaksi glukosidista sidosta, joten se voi toimia haarapisteenä, tuottaen potentiaalisen monimutkaisuuden glykaanien tai polysakkaridien rakenteessa soluissa.
Kaverit
Mitä tulee glukosidisidoksien tyyppeihin, kaksi luokkaa voidaan erottaa: glukosidiset sidokset monosakkaridien välillä, jotka muodostavat oligo- ja polysakkaridit, ja glukosidisia sidoksia, jotka esiintyvät gluktorotiineissa tai glukolipideissä, jotka ovat proteiineja tai lipidejä karbohydraattien kanssa.
O-glukosidi-linkit
Monosakkaridien välillä esiintyy O-glykosidisia yhteyksiä, muodostuu reaktiolla sokerimolekyylin hydroksyyliryhmän ja toisen anomeerisen hiilen välillä.
Disakkaridit ovat yleisimmistä oligosakkarideista. Polysakkaridit ovat yli 20 yksikköä monosakkarideja, jotka on liitetty lineaarisesti, ja joskus niissä on useita seurauksia.
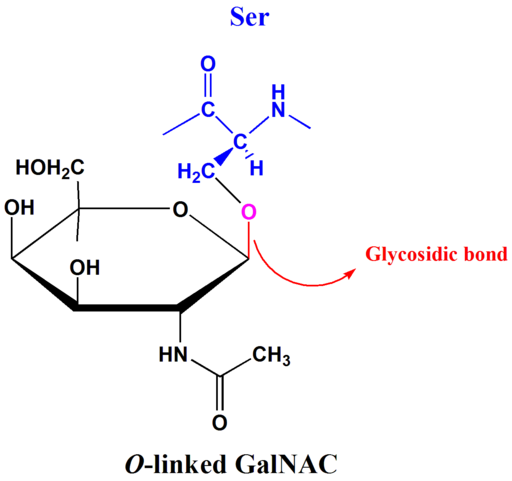 O-glukosidi-linkkiesimerkki (lähde: tpirojsi [julkinen alue] Wikimedia Commonsin kautta)
O-glukosidi-linkkiesimerkki (lähde: tpirojsi [julkinen alue] Wikimedia Commonsin kautta) Disakkaridit, kuten maltoosi, laktoosi ja sakkaroosi, yleisin glukosidinen sidos on O-glykosidinen tyyppi. Nämä yhteydet voivat esiintyä hiilihiilien ja isomeeristen muotojen α tai β -OH: n välillä.
Glukosidisidosten muodostuminen oligo- ja polysakkarideihin riippuu liitettyjen sokerien stereokemiallisesta luonteesta ja niiden hiiliatomien lukumäärästä. Yleensä 6 hiilihiilisidoksia, joissa on 6 hiilihiiliä, hiilihiilien välillä 1 - 4 tai 1 ja 6.
O -tyyppejä on kahta tyyppiä-Glykosidit, jotka nimikkeistöstä riippuen, määritellään α ja β tai 1.2-IVY ja 1,2-trans-glykosidit.
Jätteet 1,2-IVY Glykosyloituneet, a-glykosidit D-glykoosille, D-galaktoosille, L-fucosalle, D-xilosalle tai β-glykosideille D-manosalle, L-yarabinosalle; samoin kuin 1,2-trans (β-glykosidit D-glukoosille, D-galaktoosille ja a-glykosideille D-manylle jne.), ovat erittäin tärkeitä monille luonnollisille komponenteille.
O-glykosylaatio
Yksi yleisimmistä translaation jälkeisistä modifikaatioista on glykosylaatio, joka koostuu glukidiosan lisäämisestä kasvavaan peptidiin tai proteiiniin. Muciinit, eritysproteiinit, voivat sisältää suuria määriä oligosakkaridiketjuja, jotka on kytketty O-glukosidisidoksilla.
O -glykosylaatioprosessi tapahtuu eukaryootien Golgi -kompleksissa ja koostuu proteiinien liitoksesta glukidiaaliseen osaan glukosidisidoksen kautta seriinin tai treoniinin aminohapparin jäännöksen ja sokerin anomeerisen hiilen välillä,.
Voi palvella sinua: glukolipidit: mitä ovat, luokittelu, rakenne, toiminnotNäiden sidosten muodostuminen hiilihydraattien ja hydroksylisiinin ja hydroksilisiinin välillä sekä tyrosiinijätteiden fenoliryhmää on myös havaittu.
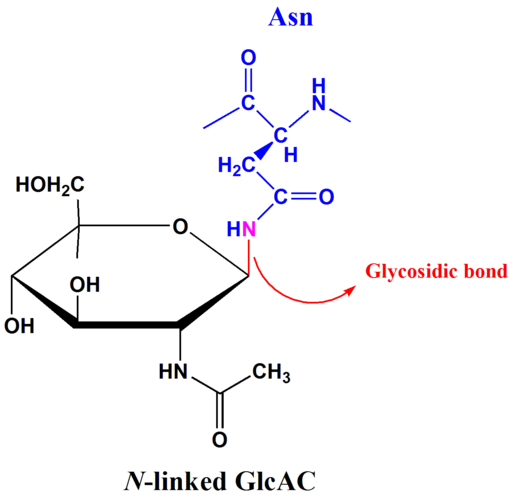
N-glukosidi-linkit
N-glykosikosidiset yhteydet ovat yleisimpiä glykosyloiduissa proteiineissa. N-glykosylaatio tapahtuu pääasiassa eukaryootien endoplasmisessa retikulumissa, seuraavilla modifikaatioilla, joita voi esiintyä Golgi-kompleksissa.
 N-Glucosidic Link -esimerkki (lähde: tpirojsi [julkinen verkkotunnus], Wikimedia Commonsin kautta)
N-Glucosidic Link -esimerkki (lähde: tpirojsi [julkinen verkkotunnus], Wikimedia Commonsin kautta) N-glykosylaatio riippuu ASN-XXX-Series/THR: n konsensussarjan läsnäolosta. Glykosidinen sidos tapahtuu aspeptidiketjuun sitovan asparagiinin sivuketjun ja anomeerisen hiilen välisen typen välillä.
Näiden sidosten muodostuminen glykosylaation aikana riippuu oligosakariltransferaasiksi tunnetusta entsyymistä, joka siirtää oligosakkaridit fosfaattidolikolista asparagiinijätteen keskellä olevaan typpiin.
Muun tyyppisiä glukosidisia linkkejä
S-glukosidi-linkit
Niitä esiintyy myös proteiinien ja hiilihydraattien välillä, on havaittu peptidien välillä N-terminaalisten kysteiinien ja oligosakkaridien kanssa. Peptidit, joilla oli tämän tyyppiset yhteydet.
C-glukosidi-linkit
Niitä havaittiin ensin translaation jälkeisenä modifikaationa (glykosylaatio) tryptofaanitähteessä RNASA 2: ssa, joka on läsnä ihmisen virtsassa ja punasoluissa 2. Käsi sitoutuu hiileen aminohappo-ytimen asennosta 2 c-glukosidisidoksen avulla.
Nimikkeistö
Termiä glykosidia käytetään kuvaamaan mitä tahansa sokeria, jonka anomeerinen ryhmä korvataan ryhmä -tai o- (o -glykosidit), -sr (tioglykosidit), -ser (selenoglukosidit), -nr (n -glykosidit tai glucosamiinit) tai jopa -cr (C-glukosidit).
Ne voidaan nimetä kolmella eri tavalla:
(1) Monosakkaridin vastaavan syklisen muodon "-o" -pääte "-ido" ja kirjoittamalla aiemmin, eri sanana korvaavan ryhmän R-ryhmän nimi.
(2) käyttämällä termiä "glykosyyloxi" monosakkaridin nimen etuliitteenä.
(3) Termin käyttäminen JOMPIKUMPI-glykosili, N-glykosili, S-glykosili tai C-glykosili etuliitteenä hydroksyloituneen yhdisteen nimelle.
Viitteet
- Nelson, D. Lens., & Cox, M. M. (2009). Lehninger -biokemian periaatteet. Omega -versiot (5. ed.-A.
- Hiilihydraattien nimikkeistö (suositukset 1996). (1996). Haettu www.Qmul.Ac.Yhdistynyt kuningaskunta
- « Branchiopoda mikä on, ominaisuudet, lisääntyminen, ruoka
- Tyynenmeren autiomaa mikä on, ominaisuudet, ilmasto, kasvisto, eläimistö »

