Pellit
- 2358
- 657
- Edgar VonRueden
 Epimeerin rakenne. Lähde: Gabriel Bolívar
Epimeerin rakenne. Lähde: Gabriel Bolívar Mitkä ovat epigrafit?
Se Pellit Ne ovat diaiaisomeerejä, joissa vain yksi sen vesikeskuksista eroaa alueellisesta kokoonpanosta, toisin kuin enantiomeereihin, joissa kaikilla vesikeskuksilla on erilaisia kokoonpanoja ja edustavat pari spekulaarista kuvaa, jotka eivät voi päällekkäin toiseen.
Muilla diasteroisomeereillä (esimerkiksi geometriset isomeerit) voi olla enemmän kuin kaksi keskuksia, joilla on erilaiset kokoonpanot. Siksi suuri osa stereoisomeereistä on diaestoisomeerejä.
Epmerit esiintyvät usein hiilihydraateissa: esimerkiksi D-glykoosi ja D-manosa eroavat C2: ssa, mikä on ensimmäinen kiraalinen hiiliatomi.
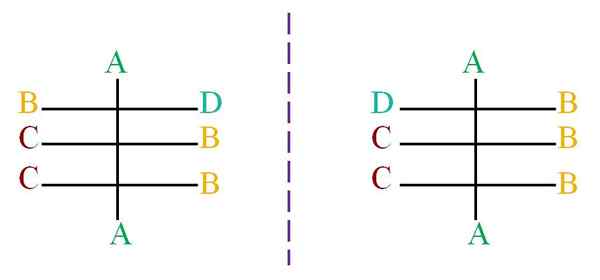
Oletetaan, että rakenne, jossa on mustia atomeja, jotka on kytketty kirjaimiin A, B, C ja D (ylivoimainen kuva).
Katkoviiva edustaa peiliä, joka osoittaa, että yllä olevien molekyylien vääntömomentti ei ole enantiomeerejä, koska kaikilla sen kiraalikeskuksilla on sama kokoonpano, paitsi ensimmäinen keskusta, joka on linkitetty kirjaimiin B ja D.
Vasemmalla puolella olevalla molekyylillä on kirjain D oikealle puolelle, kun taas oikean molekyylin kirjain D, katsoo vasemmalle puolelle. Tietääksesi, mitä kunkin kokoonpanoa on käytettävä Cahn-ingold-prelogin järjestelmään (R-S).
Epigmerien ominaisuudet
- Epigmerien pääominaisuus sijaitsee vain vesikeskuksessa (tai stereogeenisessä).
D: n ja B: n alueellisen suunnan muuttaminen voi aiheuttaa vakaampia tai epävakaampia konformereja, ts. Yksinkertaisten linkkien kiertoa aiheuttavat kaksi atomia tai tilaa vieviä atomien ryhmää tai siirtymään pois.
Siten epimer voi olla paljon vakaampi kuin toinen. Se, joka kiertää linkkinsä, tuottaa vakaampia rakenteita, on Epimerus, jolla on suurin taipumus muodostua tasapainossa.
Voi palvella sinua: Epäselvä järjestelmäPaluu kirjaimiin, D ja B voivat olla erittäin tilaa vieviä, kun taas C on pieni atomi. Joten oikean epimerinä oleminen on vakaampaa, koska kahden ensimmäisen keskuksen vasemmalla puolella löydetyt D ja C kärsivät vähemmän steerisestä esteestä.
- Mikroskooppisesti tästä tulee ominaispiirteitä otetuille epiteeliparille.
- Makroskooppisesti erot korostetaan, ja loppuvat esimerkiksi sulamispisteet, taitekertoimet, erilaiset NMR -spektrit (monien muiden ominaisuuksien lisäksi).
- Entsyymien katalysoimien biologian ja reaktioiden alalla epiteemit eroavat vielä enemmän. Ruumiin metaboloida yksi, kun taas toinen ei.
Koulutus
Epmerit muodostetaan kemiallisella reaktiolla, jota kutsutaan epimerisaatioksi. Jos molemmat epitakerit eivät eroa suuressa vakauden suhteen, perustetaan epimerisoitumisen tasapaino, mikä ei ole muuta kuin käännös:
EPB EPA
Missä EPA on epimer A, ja EPB EPIMER. Jos jokin heistä on paljon vakaampi kuin toinen, sillä on suurempi pitoisuus ja se aiheuttaa sen, mitä tunnetaan muuttajaksi. Toisin sanoen hän pystyy muuttamaan polarisoidun valon säteen suuntaa.
Epimerisaatio ei välttämättä ole tasapaino, ja siksi se on peruuttamaton. Näissä tapauksissa saadaan EPA/EPB -diasteroisomeerien rannekerma sekoitus.
Epitarnien synteettinen reitti vaihtelee riippuen siitä, mitkä ovat reagenssit, reaktio tarkoittaa ja prosessimuuttujia (katalyyttien käyttö, paine, lämpötila jne.-A.
Tästä syystä kunkin epitariparin muodostumista on tutkittava erikseen muilta, jokaisella on omat kemialliset mekanismit ja järjestelmät.
Se voi palvella sinua: Agentin vähentäminen: Konsepti, vahvin, esimerkitTautomerointi
Kaikista epitsemerien muodostumisprosesseista kahden päivän kahden päivän tautomerointi voidaan pitää yleisenä esimerkkinä.
Tämä koostuu tasapainosta, jossa molekyyli käyttää ketonimuotoa (C = O) tai enlicus (C-OH). Kun ketoninen muoto on muunnettu, karbonyyliryhmän (jos se on kiraalinen) vieressä oleva hiilikokoonpano muuttuu, jolloin pari epitsääjää tuottaa.
Esimerkki edellä mainitusta on cis-dekaloni- ja trans-dekaloni-vääntömomentti.
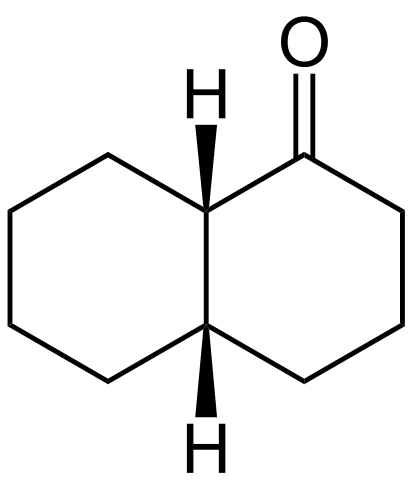 Cis-Decalona-rakenne. Lähde: Wikimedia Commons
Cis-Decalona-rakenne. Lähde: Wikimedia Commons Cis-dekalonan rakenne on esitetty yllä. H-atomit sijaitsevat kahden renkaan yläosassa, kun taas trans-dekalonissa toinen on renkaiden yläpuolella ja toinen on alla.
Hiili ryhmän C = O vasemmalla puolella on quiraalikeskus, ja siksi se, joka erottaa epitchit.
Esimerkit
Glukoosin anomerit
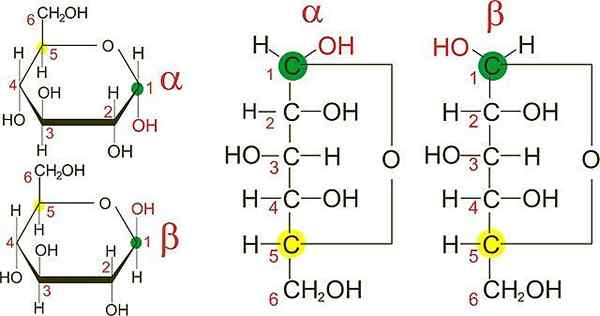 D-glukoosi-anomerit. Lähde: Wikimedia Commons
D-glukoosi-anomerit. Lähde: Wikimedia Commons Ylemmässä kuvassa sinulla on kahden D-glykoosin anomeerin furaanirenkaat: α ja β. Renkaista voidaan nähdä, että hiilen 1 OH -ryhmät löytyvät joko viereisen OH: n samaan suuntaan, a -anomeerissä tai vastakkaisiin suuntiin, kuten β -anomeerissä.
Molempien anomereiden (kuvan oikealla puolella) kalastajaprojektiot tekevät eron molempien epitseiden välillä vielä selkeämmäksi, jotka puolestaan ovat anomeerejä.
Kahdella α -anomerilla voi kuitenkin olla erilaisia alueellisia kokoonpanoja yhdessä muissa hiilissä, ja siten epiteerit.
Fisherin α-anomeerin projisoinnin C-1: ssä OH-ryhmä "näyttää" oikealta, kun taas β "näyttää" β-anomeeri.
Voi palvella sinua: Faraday ConstantMentolisarit
 Mentolin stereoisomeerit. Lähde: Wikimedia Commons
Mentolin stereoisomeerit. Lähde: Wikimedia Commons Kuvassa sinulla on kaikki mentolimolekyylin stereoisomeerit. Jokainen sarake edustaa enantiomeerien paria (tarkkaile huolellisesti), kun taas rivit vastaavat diastereoisomeerejä.
Joten epitaarien on oltava ne, jotka tuskin erottelevat muuta kuin hiilen alueellisessa asemassa.
(+)-mentol ja (-)-neoisomentol ovat epäröitä ja myös diabetereoisomeerejä (ne eivät ole samassa sarakkeessa).
Jos sitä havaitaan yksityiskohtaisesti, molemmissa ryhmissä -OH ja -CH3 He jättävät lentokoneen (renkaan yläpuolella), mutta (-)-neoisomentol-isopropiliryhmä osoittaa myös tasosta.
Ei vain (+)-mentol on (-)-neoisomentolin, mutta myös (+)-neomentol. Jälkimmäinen eroaa vain siitä, että ryhmä -CH3 osoittaa lentokonetta. Muita epähkisiä ovat:
- (-)-isomentol ja (-)-neomentol
- (+)-isomentol ja (+)-neomentol
- (+)-neoisomentol ja (-)-neomentol
- (+)-neomentol ja (-)-neoisomentol
Nämä stereoisomeerit edustavat käytännöllistä esimerkkiä epitemerien käsitteen selventämiseksi, ja voidaan nähdä, että useista diastereoisomeereistä monet voidaan erottaa vain yhdessä epäsymmetrisessä tai kiraalisessa hiilessä.
Viitteet
- Carey f. (2008). Orgaaninen kemia. MC Graw Hill.
- Pellit. Haettu luokkahuoneista.Uruguayeduca.Edu.vai niin

