Fucosa -ominaisuudet, rakenne, toiminnot
- 3559
- 331
- Louis Moen
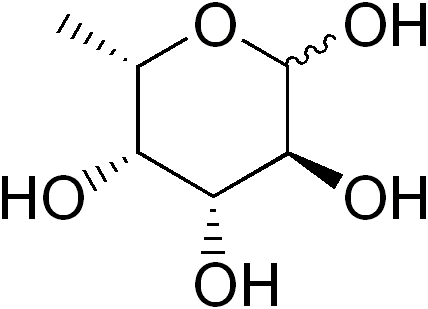
Se Fukosa (lyhennetty FUC) tai 6-L-DEXI-galaktoosi, se on osittain deoksigenado (deoksizúcar) monosakkaridi kuudesta hiilestä, jonka empiirinen kaava on C IS C IS6H12JOMPIKUMPI5. Kuten muutkin monosakkaridit, se on polyhydroksyloitu sokeri.
Kun hydroksyyliryhmä korvataan vedyn atomilla, johdetaan deoksiazúcar. Vaikka teoreettisesti tämä korvaus voi vaikuttaa mihin tahansa monosakkaridin hydroksyyliryhmään, luonnossa on vähän erilaisia deksiazúcús.
 Lähde: Edgar181 [julkinen verkkotunnus]
Lähde: Edgar181 [julkinen verkkotunnus] Jotkut deoksiaazúces ovat: 1) deoksiribosa (2-disoxxi-d-libose), johdettu DNA: ta, joka on osa DNA: ta; 2) Ramnosa (6-D-Dexxi-Marso), johdettu D-manosasta; 3) Fucosa, johdettu L-galaktoosista. Jälkimmäinen on yleisempi kuin D-fukosa, johdettu D-galaktoosista.
[TOC]
Ominaisuudet ja rakenne
Fucosa tunnetaan myös 6-disoxxi-scalact-heksoosi-, fukopiraanisilla, galactometyyli- ja rodeous-nimillä.
Vaikka se muodostaa normaalisti polysakkaridit ja glykoproteiinit, eristetty monosakkaridina on makeampaa kuin galaktoosi. Tämä johtuu siitä, että hydroksyyliryhmän korvaaminen vetyatomilla lisää hydrofobista luonnetta ja siksi molekyylin makeutta.
Fucosa -hydroksyyliryhmät voivat kokea samat reaktiot kuin muilla sokereilla, jotka tuottavat monenlaisia asetaaleja, glykosideja, eetteriä ja estereitä.
Fukosiloitu biomolekyyli on sellainen, johon fukosyylitransferaasin vaikutuksella he ovat liittyneet glykosidisidoksilla, fucosa -molekyylit. Kun glykosidisten sidosten hydrolyysi tapahtuu fukosidaasin vaikutuksella, mikä erottaa fukot.
Kun glucanos fukosyyli, fucanos -nimisiä monimutkaisempia glucaaneja syntyy, mikä voi olla osa glykoproteiineja. Sulfaattifukans määritellään niiksi, jotka ovat polysakkarideja, jotka sisältävät L-fucosan sulfaattijäämiä. Ne ovat tyypillisiä ruskealle levälle. Esimerkkeinä ne voidaan nimittää Ascophilano, Sargasano ja Pelvetano.
Yksi parhaiten tutkituista fucanosista on fucoidano, joka on saatu ruskeasta levästä Fucus vesiculosus, jota on markkinoitu (Sigma-Aldrich Chemical Company) vuosikymmenien ajan.
Voi palvella sinua: mikä on virheeneo?Jakautuminen luonnossa
D-fukoosia esiintyy mikrobien tuottamissa antibioottisissa aineissa ja vihannesglykosideissa, kuten Convoling, Charrtreusine, Ledienosida ja Queirotoksiini.
L-fukoosi on levien polysakkaridien, luumujen, liinavaatteiden, soijan ja rypäleiden, tragakakantokumin, perunan seinämien, kassavan, kiivihedelmien, kiivihedelmien, hedelmien, kassavan, soijan ja rypsin levyjen aineosa, kiwi-heinät, kiwi-soluseinät, kivit, soija, kiwi-hedelmät, Ceiban aivokuori ja maissin kaliftran mucgel, samoin kuin muut kasvit.
L-fukosaa esiintyy myös merisiilimunissa ja hyytelössä, joka suojaa sammakon munia.
Nisäkkäissä fucaanit L-fukosassa muodostavat ligandit, jotka toimivat Selectin-välitteisessä leukosyytti-endoteelin tarttuvuudessa, ja osallistuvat lukuisiin ontogeneettisiin tapahtumiin.
L-fucosa on runsaasti maha-suolikanavan epiteelin ja luuytimen fukoesfingolipideissä, ja se esiintyy pieninä mittasuhteissa rusto- ja keratiinirakenteissa.
Ihmisillä fucanot L-fukosassa ovat osa syljen glykoproteiineja ja mahalaukun mehuja. Ne ovat myös osa antigeenejä, jotka määrittelevät ABO -veriryhmät. Niitä esiintyy useissa oligosakkarideissa rintamaitoa.
Fucosa -aineenvaihdunta
Fukosyylitransferaasit käyttävät BKT-fukoosia, fucosa-muodon aktivoituna nukleotideilla fukosan luovuttajana fukosyloitujen oligosakkaridien rakentamisessa.
BKT-fukosa on johdettu BKT-manosasta kahden entsyymin peräkkäiseen toimintaan: BKT-Manasea 4.6-Dehydratasa ja BKT-4-Zo-6-Desoximanosa 3.5-Epimerasa-4-Reduktaasi.
Ensimmäinen entsyymi katalysoi NADP+-kofaktoria, joka katalysoi BKT-monen kuivumista. Aseman 6 vähentäminen ja aseman 4 hapettuminen tuottaa BKT-6-Desoxi-4-keto-koamingin (reaktion aikana hybridi siirretään sokerin asemasta 4-6)).
Toinen entsyymi, joka on NADPH-riippuvainen, katalysoi BKT-6-desoxi-4-Ecto-Mamosan asemien 3 ja 5 epimerisointia ja ryhmän 4-ZO: n verkkoa.
Bakteerit voivat kasvaa käyttämällä fukosaa yhtenä hiilen ja energian lähteenä fukosan indusoitavan oponin kautta, joka koodaa tämän sokerin katabolisia entsyymejä.
Voi palvella sinua: karboksyylihappoAikaisempi prosessi sisältää: 1) vapaa fukosa -pääsy soluseinän läpi väliaikaisesti permeaasin välityksellä; 2) fucosa -isomerointi (aldosa), joka muodostaa räikeän (zea); 3) epämääräisen fosforylaatio muodostaa fucous-1-fosfaattia; 4) Aldolaasireaktio laktadehydin ja dihydroksiasetonin fosfaatin muodostamiseksi fucousus-1-fosfaatista.
Funktiot
Syöpäpaperi
Monen tyyppisten syöpää aiheuttavien kasvaimen oireiden joukossa ovat glukaanilinnoitusproteiinien läsnäolo, jotka erotetaan muuttuneesta oligosakkaridikoostumuksesta,. Näiden epänormaalien glucanien läsnäolo, joista fucanot erottuvat, liittyy näiden kasvainten pahanlaatuisuuteen ja metastaattiseen potentiaaliin.
Rintasyöpään kasvainsolut sisältävät fukosan glykoproteiineihin ja glykolipideihin. Fucosa edistää tämän syövän etenemistä, suosimalla syövän kantasolujen aktivointia, hematogeenistä etäpesäkkeitä ja kasvainten tunkeutumista solunulkoisten matriisien kautta.
Keuhkokarsinoomassa ja hepatokarsinogeneesissä fucosan lisätty ekspressio liittyy suureen metastaattiseen potentiaaliin ja alhaisella eloonjäämisen todennäköisyydellä.
Vastapuolena jotkut sulfatoidut fucanot ovat lupaavia aineita syövän hoidossa, sellaisena kuin se on määritetty.
Paperi muissa sairauksissa
Fucanosin lisätty ilmentyminen seerumin immunoglobuliineissa on liittynyt nuorten ja aikuisten nivelreumaan ja aikuisiin.
Leukosyyttien tarttumisen II puute on harvinainen synnynnäinen sairaus, joka johtuu mutaatioista, jotka muuttavat Golgi-laitteessa sijaitsevan FDP-fukoosin kuljettajan aktiivisuutta.
Potilaat kärsivät henkisestä ja psykomotorisesta viivästyksestä ja kärsivät toistuvista bakteeri -infektioista. Tämä tauti reagoi suotuisasti suun kautta otettaviin fukosiannoksiin.
Biolääketieteellinen potentiaali
Ruskeasta levästä saadut sulfaattifucanot ovat tärkeitä yhdisteiden säiliöitä, joilla on terapeuttinen potentiaali.
Se voi palvella sinua: itiTrium: rakenne, ominaisuudet, käytöt, hankkiminenHeillä on anti -inflammatorisia ja antioksidantti -ominaisuuksia, estäen lymfosyyttien migraatiota infektiokohdissa ja suosimalla sytokiinien vapautumista. Lisää immuunivastetta aktivoimalla lymfosyytit ja makrofagit.
Heillä on antikoagulanttien ominaisuuksia. Se on todistettu ihmispotilailla, jotka estävät suun kautta verihiutaleiden aggregaatiota.
Heillä on antibiootti- ja antiparasiittinen potentiaali ja ne estävät mahalaukun patogeenisten bakteerien kasvua Helicobacter pylori. Tappaa loiset Plasmodium SPP. (Malarian syy -aine) ja Leishmania Donovani (Amerikkalaisen viskeotrooppisen leishmaniaasin syy -agentti).
Lopuksi niillä on voimakkaita viruslääkkeitä, jotka estävät pääsyä useiden virusten soluun, joka on erittäin tärkeä ihmisten terveydelle, myös Areenavirus, Sytomegalovirus, Hantavirus, Hepadnavirus, HIV-, herpes simplex -virus ja influenssavirus.
Viitteet
- Becker, D. J -., Lowe, J. B -. 2003. Fukoosi: Biosynteesi ja biologinen toiminta nisäkkäissä. Glykobiologia, 13, 41R-53R.
- Deniaud-bouët, e., Hardouin, k., Potin, P., Kloareg, b., Hervé, c. 2017. Katsaus ruskeista leväsolujen seinämistä ja fukoosia sisältävistä sulfatoituneista polysakkarideista: soluseinämäympäristö, biolääketieteelliset ominaisuudet ja keskeiset tutkimushaasteet.Hiilihydraattipolymeerit, http: // dx.doi.org/10.1016/j.Karboli.2017.07.082.
- Kukkia h. M. 1981. D-ja L-fukoosin kemia ja biokemia. Hiilihydraattikemian ja biokemian edistysaskeleet, 39, 279-345.
- Linkinsky, J. J -., Siegal, G. P., Linkinsky, c. M. 2011. Syntyvä merkitys α-L-fukoosi ihmisen rintasyövässä: Katsaus. OLEN. J -. Kääntää. Naudanliha., 3, 292-322.
- Murray, r. K -k -., et al. 2003. Harperin kuvitettu biokemia. McGraw-Hill, New York.
- Pereira, l. 2018. Levien terapeuttinen ja ravitsemuksellinen käyttö. CRC Press, Boca Raton.
- Staudacher, E., Altmann, f., Wilson, I. B -. H., März, l. 1999. Fukoosi N-Glykaanissa: Kasvista ihmiselle. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, W., Loewus, f. -Lla. 1981. Kasvihiilihydraatit II. Solunulkoiset hiilihydraatit. Springer, New York.
- Vanhooren, P. T., Vandamme, E. J -. 1999. L-fukoosi: esiintyminen, fysiologinen rooli, kemiallinen, entsymaattinen ja mikrobisynteesi. Journal of Chemical Technology and Biotechnology, 74, 479-497.
- « Etelämantereen napapiirin sijainti, ominaisuudet, kasvisto ja eläimistö
- Kemosynteesifaasit, organismit, erot fotosynteesin kanssa »

