Galvanoplastia

- 3012
- 140
- Louis Moen
Selitämme, mitä galvanoplastia koostuu, nimeltään myös elektrodepositio, miten sen prosessi, käytännölliset esimerkit ja sen sovellukset ovat.
 Lusikan galvanoplastia
Lusikan galvanoplastia Mikä on galvanoplastia?
Galvanoplastia tai elektrodepositio on sähkökemiallinen tekniikka, joka koostuu, kuten sen nimi viittaa, metallikerrosten tallettamiseen objektien vastaanottamiseen; Toisin sanoen niiden peittäminen metallikannasta, jonka paksuus vaihtelee välillä 5-20 μm.
Tätä tekniikkaa tunnetaan myös nimellä Electrochapado tai elektrolyyttinen päällystetty, koska elektrolyyttinen väliaine, joka koostuu metallin metalli -ioneista, joita halutaan tallettaa, on välttämätöntä sen toteuttamiselle. Siksi, jos haluamme kuparia (kuparia), tarvitsemme kupariliukoisia suoloja, kuten kuparisulfaattia, liuennut veteen.
Aikaisempi päättely koskee mitä tahansa muuta metallia: kultaelektrolyyttinen päällystetty vaatii kultasuoloja, yleensä kultaisyanideja, joista voi tulla erittäin myrkyllisiä. Siten jotkut esineet, kuten syömisvälineet, voidaan päällittää kullalla suuremman arvon ja aatelisen osoittamiseksi.
Mutta galvanoplastia ylittää estetiikan: ne annetaan. Se sallii myös luonnonvarojen säästämisen, koska ei ole välttämätöntä käyttää suuria määriä metallia päällysteisiin.
Galvanoplastiaprosessi
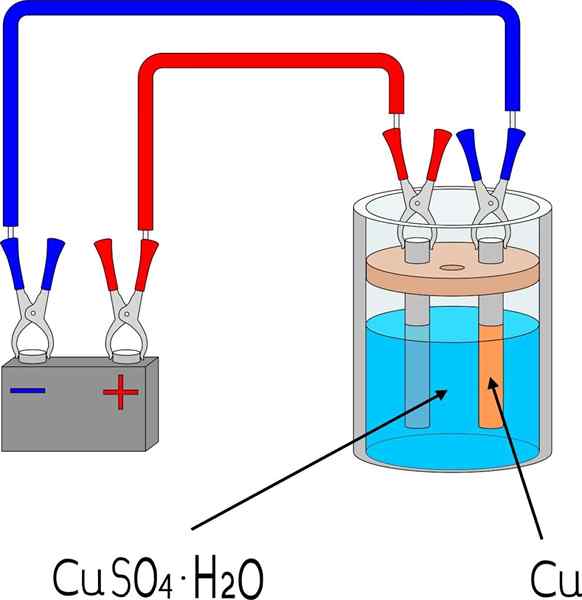 Kuparielektrodipositio kuparisulfaattihuoneessa
Kuparielektrodipositio kuparisulfaattihuoneessa Kohteet
Metallin elektrodeposeiden pinnalla tarvitaan joitain peruselementtejä, joiden mitat ja tila vaihtelevat peitettävien esineiden erän mukaan.
Esimerkiksi ylemmässä kuvassa on esitetty pieni -asukas kuparin elektrodi, toistettavissa missä tahansa laboratoriossa tai tilassa.
Elektrolyyttinen väliaine
Ensinnäkin tarvitaan metallin elektrodepositod -elektrolyyttiväliaine. Kuparisulfaattisuola, cuo4, Se on hyvin liukoinen veteen, joten se tuo ionit cu2+ joka sitten pelkistetään atomeiksi cu0 -. Nämä atomit ovat niitä, jotka kootaan vastaanottopinnalle metallikiteiden aiheuttamiseksi.
Elektrolyyttinen väliaine on välttämätön piirin toimimiseksi ja ioniset kuormat voivat liikkua tai mobilisoida kohti aluetta, jolla elektrodepositio tapahtuu.
Elektrodit
Elektrodit ovat pintoja, joilla elektrodepositio tapahtuu sen kemiallisesta emäksestä. Yksinkertaisesti sanottuna on kaksi elektrodia: katodi, jossa metalli on elektrodepos; Ja anodi, jossa tapahtuu kemiallinen reaktio, joka luovuttaa elektroneja metalli -ioneihin, jotka peittävät katodin.
Se voi palvella sinua: uretaani: rakenne, ominaisuudet, hankkiminen, käyttöEli katodista tulee haluamasta kappaleesta. Samaan aikaan anodi on mikä tahansa pinta, jolla laji hapettaa ja lahjoittaa elektronit katodiin. Monta kertaa anodi on valmistettu samasta metallista, joka on liuennut elektrolyyttiseen ympäristöön. Jos keskellä on kupari -ionista, tässä tapauksessa anodi on metallinen kupari.
Ulkopiiri
Ulkoinen piiri on akku, joka tarjoaa alkuperäiset elektronit, jotka edistävät elektrodepositiota. Sen läsnäolo tarkoittaa, että reaktio ei ole spontaani: Kemiallisen muutoksen tuottamiseksi tarvitaan sähköä, mikä on liuennettujen metalli -ionien vähentäminen.
Elektrodin puhdistus
Palattavan kappaleen on oltava täysin puhdas. Muuten päällystetty tai pinnoite on viallinen.
Tätä varten sinun on varmistettava, että sen pinta on täysin hydrofiilinen, ts. Siinä ei ole rasvaa tai likaa. Yksi tapa varmistaa tämä kemiallisen pesun jälkeen on kastea pala vedellä, ja jos havaitaan vesipisaroita tai epäyhtenäistä nestemäistä pudotusta, se tarkoittaa, että elektrodi ei ole vielä puhdas.
Elektronien reaktiot ja merkitys
Galvanoplastia on redox -reaktio. Siksi: Yksi laji on vähennettävä, kun taas toinen hapettunut tai päinvastoin. Kuparissa meillä on kuparista valmistettu anodi ja metalli -Meistä valmistettu katodi (rauta, sinkki, tina jne.-A.
Kun kytkemme akun päälle, ne virtaavat elektroneja katodiin, joka alkaa latautua negatiivisesti.
Katodin negatiivinen kuorma houkuttelee kationeja cu2+ elektrolyyttisen ympäristön suhteen vähentäminen:
Cu2+(AC) +2e- → Cu (s)
Se voi palvella sinua: Maillard -reaktioAkun on palautettava lahjoitetut elektronit, ja myös ionit Cu on palautettava2+ pelkistetty ylläpitämään elektrolyyttisen ympäristön puolueettomuutta. Tällöin anodi tulee toiminnassa: kupariatomit hapettuu:
Cu (s) → cu2+(AC) +2e-
Ja vapautetut elektronit on suunnattu takaisin akkuun, mikä puolestaan mobilisoi niitä kohti katodia jatkaakseen elektrodepositiota.
Anodi on saanut positiivista kuormaa, mikä houkuttelee SO -ioneja42- elektrolyyttisen väliaineen (katso kuva jälleen kerran).
Toisin sanoen esiintyvät reaktiot ovat kuparin, metallin, joka on elektrodeposin, pelkistäminen ja hapettuminen:
Cu2+(AC) +2e- → Cu (s)
Cu (s) → cu2+(AC) +2e-
Kuparin anodi menettää taikinaa, kun taas toisen metallin katodi on peitetty hienolla kuparikerroksella.
Esimerkkejä galvanoplastiasta
Hopea
Metallit voivat olla "elektrolaatti", joka peittää ne hopeakerroksesta. Tämä on erityisen hyödyllistä sähköisissä komponenteissa, joiden on suoritettava sähkö. Hopea voi olla elektrodeposita teräksellä, kuparilla, nikkelillä ja muilla metalleilla.
Tina-
Tinner on tinan elektrodepositio. Se on erittäin hyödyllinen rauta tölkkien tuotannossa, jotka on peitetty tinalla, jotta ne olisivat korroosion kestäviä, eivätkä siten vahingoita varastoita ruokaa tai tuotteita, jotka.
Latinalainen tai ruskea
Vaikka messinki ja pronssi voi olla hiukan yksityiskohtaisempi, ne voivat olla myös elektrodeposja joillakin metalleilla heidän ulkonäkönsä parantamiseksi.
Sinkado
Sinkki- tai sinkki -galvanoplastiaa (ei sekava termisen galvanoituun) käytetään enimmäkseen raudankestävyyden myöntämiseen korroosiolle ja kirkkaammille ja houkuttelevammalle pinnalle. Siten sen toiminta on esteettinen ja samalla toiminnallinen, ja sitä löytyy kehon osista, kuten pyörät.
Metallimuovia
Muovit, jotka on aiemmin käsitelty johtavalla pinnalla, voidaan peittää myös metallilla, mikä on kuin ne kiinnitetään alumiinifolion arkkiin.
Voi palvella sinua: Kitasato -pulloGalvanoplastikkisovellukset
Galvanoplastian tai elektrodepositiosovellukset voidaan jakaa funktionaalisiin tai esteettisiin.
Funktionaalinen
 Ohut kullan elektrodipos astronautien tapausten katsojissa antaa heille mahdollisuuden suojata silmänsä auringonvalolta
Ohut kullan elektrodipos astronautien tapausten katsojissa antaa heille mahdollisuuden suojata silmänsä auringonvalolta Pala tai esineen päällyste on tarjota pintaansa ominaisuuksilla, joilla yksin puuttuu. Esimerkiksi kupari- tai kultaelektroditio tekee heidän kappaleidensa, joten elektronisissa piireissä on ihanteellista hyödyntää näiden metallien ominaisuuksia ilman tarvetta käyttää tonnia kultaa kokonaisten ja kiinteiden kappaleiden valmistukseen.
Kulta puolestaan suojaa lämpöä ja säteilypintoja. Tästä syystä sitä käytetään laajasti satelliitteissa ja astronautien kypärissä, koska se heijastaa auringonvaloa siten, että heidän silmänsä tai nopeasti kuuma.
Kromi- tai nickeled -teräkset ovat erittäin resistenttejä korroosiolle tarkasti näiden metallikerrosten ansiosta. Siksi teollisuudessa käytetään galvanoplastiaa suojaamaan metalleja, jotka ovat herkkiä Corrodille.
Estetiikka
Metalli viilut loistavat. Sinkkiä, nikkeliä ja kromia käytetään paljon tähän tarkoitukseen. Myös kulta ja hopea ovat elektrodepos renkaissa, ketjuissa, rannekkeissa, tukehtuneissa, rinteissä jne., Ja siksi sen galvanoplastia löytää monia sovelluksia korukaupoista ja koristeista, näiden vaatteiden kuvan ja arvonomistuksen parantamiseksi.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Wikipedia. (2021). Elektropanoiva. Haettu: vuonna.Wikipedia.org
- Chris Woodford. (28. heinäkuuta 2020). Kuinka elektrolanointi toimii. Haettu osoitteesta: SelftinTatstuff.com
- Rob Snyder. (S.F.-A. Nanomittakaavan elektrodepositio. STEM Education Institute. [PDF]. Toipunut: nanomittakaava.Unta.Edu
- Elsevier B.V. (2021). Elektrodepositio. Tiede. Haettu: ScienEdirect.com
- Vaishali Mittal. (10. joulukuuta 2020). Elektropanoiva. Kemian librettexts. Palautettu: Chem.Librettexts.org
- Singh Davneet. (9. kesäkuuta 2020). Erityyppiset sähkökäytöt. Toipunut: Teachoo.com
- Helmestine, Anne Marie, PH.D -d. (26. elokuuta 2020). Mikä on sähköpuhelinta ja miten se toimii? Toipunut: Admingco.com

