Gilbert Newton Lewis
- 2195
- 378
- Kelly Kilback
 Gilbert Newton Lewis
Gilbert Newton Lewis Gilbert Newton Lewis (1875-1946) oli yksi 2000-luvun tärkeimmistä amerikkalaisista tutkijoista. Hänen työnsä tuotti rakenteellisen vallankumouksen kemiallisissa tutkimuksissa monien panosten ansiosta, joita hän antoi koko elämänsä tieteen kehityksen kannalta.
Tämän fysikaalis -kemiallisen panoksen joukossa erottuu hänen nimensä kantavan kaavan, jolla elektroniparit ovat graafisesti esitettyjä. Lewisin tutkimustyö oli erittäin laaja, vaikka hänen maine johtui periaatteessa kemiallisten sidosten teoriasta ja happo-emäshapon määritelmästä vuonna 1923.
Lewisilla oli suuri vaikutus Yhdysvaltojen tieteelliseen ja akateemiseen maailmaan, etenkin Harvardin yliopistossa, missä puheenjohtaja perustettiin ja saneltiin. Hänen työnsä Yhdysvaltain armeijalle ensimmäisen maailmansodan aikana ansaitsin hänelle suurimman tunnustuksen ja korkeimman kunnianosoituksen.
Se muodostettiin Nebraskan, Harvardin, Leipzigin ja Gontingan yliopistoissa Saksassa. Hän työskenteli Massachusetts Institute (MIT) Harvardin yliopistossa ja Kalifornian yliopistossa, missä hän kuoli työskentelyssä.
Koko elämänsä ajan hän sai lukemattoman tunnustuksen ja palkinnot, joista useat Chicagon, Madridin, Liverpoolin, Wisconsinin ja Pennsylvanian kunniatohtorit erottuvat. Hän oli useiden tieteellisten instituutioiden kunniajäsen Englannissa, Intiassa, Ruotsissa, Tanskassa ja Yhdysvalloissa.
Elämäkerta
Syntymä ja varhaiset vuodet
Gilbert Newton Lewis syntyi Weymouthissa, Massachusettsissa, 23. lokakuuta 1875. Hänen vanhempansa olivat Frank Wesley Lewis ja Mary Burr White Lewis. Varhaisvuosiensa aikana hän sai opetuksia omassa kodissaan ja 10 -vuotiaana hän tuli julkiseen kouluun, missä hän valmistui vuonna 1889.
Vuonna 1884 Lewisin piti asettua perheensä kanssa Lincolnissa, Nebraskassa. 13 -vuotiaana hänet otettiin Nebraskan yliopiston lukioon.
Voi palvella sinua: beryllium -hydridi (beh2)Opinnot
Valmistuttuaan hän jatkoi yliopisto -opintojaan kaksi vuotta ja ilmoittautui sitten Harvardin yliopistoon vuonna 1893.
Alun perin hän oli kiinnostunut taloudesta, mutta lopulta valitsi fysiikan ja kemian. Gilbert sai kemian tittelinsä vuonna 1896 ja vuodeksi hän opetti Phillips Academyssa, joka on yksityinen Andoverin koulu.
Hän palasi Harvardiin suorittamaan jatkotyötä ja hankkimaan maisterin tutkinnon vuonna 1898 hänen opinnäytetyönsä päällä Elektroni ja molekyyli. Vuotta myöhemmin tohtori ja hänen opinnäyte olivat nimeltään Jotkut sinkki- ja kadmiumamalgaamien sähkökemialliset ja lämpökemialliset suhteet".
Harvardissa hän toimi ohjaajana vuoden ajan ja matkusti sitten Eurooppaan stipendillä. Hän opiskeli ajan suuria fysikaalis -kemikaaleja.
Vuonna 1899 hän matkusti Saksaan opiskelemaan Wilhelm Ostwald Leipzigin kanssa ja sitten Walter Nernstin kanssa Gontingin yliopistossa; Sitten hän työskenteli filippiiniläisen hallituksessa.
Akateeminen työ ja osallistuminen sotaan
Vuosina 1999–1906 hän antoi kemian tuolin Harvardin yliopistossa ja palkkasi sitten Massachusettsin tekniikan instituutin, missä hän oli vuosina 1907 - 1912.
Myöhemmin hänestä tuli fyysisen kemian professori Kalifornian yliopistossa (Berkeley), missä hän sai kemian koulun dekaanin tutkinnon.
Vuonna 1908 hän julkaisi ensimmäisen artikkelinsa relatiivisuusteoriasta rinnakkain Albert Einsteinin kanssa. Tässä se toteaa, että energia-masan välillä on yhteys, mutta muuhun suuntaan kuin Einsteinin käyttämä.
Lewis meni 21. kesäkuuta 1912 Mary Fanckley Sheldonin kanssa, jonka kanssa hänellä oli kolme lasta: Margery S. Lewis, Edward S. Lewis ja Richard Newton Lewis.
Se voi palvella sinua: Giberélihappo: Ominaisuudet, synteesi, toiminnotHänen työnsä Kaliforniassa keskeytti ensimmäisen maailmansodan puhkeamisen. Vuonna 1917 hänet valtuutettiin työskentelemään Yhdysvaltain armeijassa, missä hänestä tuli kemiallisen sotapalvelun puolustajan jaoston päällikkö.
Lewisin toimitus ja työkapasiteetti sallivat armeijan. Sodan lopussa hänet myönnettiin palveluistaan korkeimmalla kunnianosoituksella.
Kuolema laboratoriossa
Gilbert n. Lewis kuoli 70 -vuotiaana sydänkohtausta, kun hän työskenteli laboratoriossaan Berkeleyn yliopistossa 23. maaliskuuta 1946.
Ehkä introvertin persoonallisuutensa vuoksi tämä merkittävä tiedemies ei koskaan saanut Nobel -palkintoa. Melkein uransa lopussa hän onnistui todistamaan, että orgaanisten molekyylien fosforesenssia säätelee innostunut kolminkertainen tila, jopa laskemalla sen magneettiset ominaisuudet.
Osallistuminen tieteeseen
Jotkut Gilbert Newton Lewisin tärkeimmistä panoksista tieteeseen ovat seuraavat:
Lewis -rakenteet
Ne ovat useita menetelmiä, jotka edustavat molekyylin rakennetta. Näissä elementtien symbolit edustavat atomeja, kun taas pisteet edustavat niitä ympäröivät elektronit. Esimerkki tästä on vedyn, heliumin ja hiilen esitys:
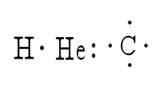
Lewis ehdotti ensimmäisenä ajatusta, että atomit voisivat pysyä yhtenäisinä vertaamalla elektronipareja; Siksi hän loi rakenteiden symbolismin.
Lewisin ehdottama laaja linkkiteoria ajoi ryhmään yhdeksi konseptille kaiken tyyppiset kemialliset yhteydet. Tällä tavoin osoitettiin ionisten, molekyyli-, kovalenttien ja metallisten aineiden väliset suhteet. Siihen asti näillä elementeillä ei ollut ollut käsitteellistä yhteyttä.
Voi palvella sinua: 02 -linkin tyyppiKovalenttisidos
Käsittelee kovalenttisen sidoksen, joka muodostuu kahden atomin välillä, kun ne liittyvät saavuttamaan stabiili oktetti ja jakavat viimeisen tason elektronit, paitsi vety, joka onnistuu stabiilisuuteen saamalla 2 elektronia.
Oktettiteoria
Lewis totesi sen vuonna 1916. Tämä osoittaa, että jaksollisen järjestelmän elementteihin kuuluvat ionit yleensä täydentää useita 8 elektronia niiden viimeisimmät energiatasot. Tämän avulla he voivat hankkia erittäin vakaan kokoonpanon.
Fotoni
Se oli termin fotonin luoja vuonna 1926, joka määritteli pienimman valon energian yksikön. Tämä energiahiukkas välittää kaikki olemassa olevat sähkömagneettisen säteilyn muodot (x -säteily, infrapuna, gamma, ultravioletti, mikroaallot, radioaallot jne.-A.
Kemiallinen vetovoima ja Valencia
Yhdessä kemiallisen kollegansa Irwing Langmirin kanssa hän kehitti vetovoiman ja kemiallisen valenssin teorian, joka tunnetaan nimellä Langmuir-Lewis -teoria. Tätä varten se perustui aineiden atomirakenteeseen.
Raskas vesi
Lewis oli myös ensimmäinen tutkija, joka tutki ja tuotti raskasta vettä (deuterium) puhtaimmassa muodossaan. Hän oli myös ensimmäinen, joka sovelsi termodynamiikan periaatteita kemiallisten ongelmien tutkimuksessa.
Liukenemisteoria
Samoin Lewis tunnustetaan hänen työnsä ratkaisuteoriasta; toisin sanoen homogeeniset seokset, jotka on saatu atomien, molekyylien tai ionien interpositiosta, läsnä kahdessa tai useammassa aineessa. Nämä aineet, joita kutsutaan komponenteiksi, puuttuvat mittasuhteisiin, jotka vaihtelevat.

