Glyseraldehydi 3-fosfaatti (G3P) -rakenne, toiminnot
- 1437
- 127
- Alonzo Kirlin
Hän Glyseraldehydi 3-fosfaatti (aukko) Se on glykolyysin metaboliitti (sen nimi tulee kreikasta; glykos = makea tai sokeri; hajotus = repeämä), joka on metabolinen reitti, joka muuntaa glukoosimolekyylin kahteen pyruvaattimolekyyliin energian tuottamiseksi adenosiinin tryfosfaatin muodossa (ATP -A.
Soluissa glyseraldehydi 3-fosfaatti yhdistää glykolyysin glukoneogeneesiin ja pentoosifosfaattireitille. Fotosynteettisissä organismeissa glyseraldehydi 3-fosfaatti hiilidioksidin kiinnitystä käytetään sokeribiosynteesiin. Maksassa fruktoosimetabolia tuottaa aukon, joka sisällytetään glykolyysiin.
 Lähde: Benjah-BMM27 [julkinen alue]
Lähde: Benjah-BMM27 [julkinen alue] [TOC]
Rakenne
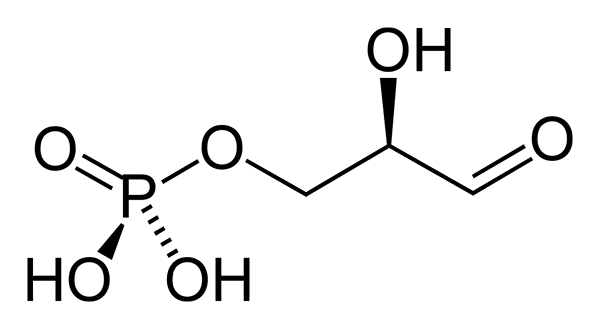
3-fosfaatti-glyseraldehydi on fosforyloitu sokeri, jolla on kolme hiilyä. Sen empiirinen kaava on c3H7JOMPIKUMPI6P. Aldehydiryhmä (-CHO) on Carbon 1 (C-1), hydroksimetyleeniryhmä (-CHAH) on hiili 2 (C-2) ja hydroksimetyyliryhmä (-CH2OH) on hiili 3 (c3). Tämä viimeksi muodostaa yhteyden fosfaattiryhmään (Fosfoester Link).
3-fosfaatti-glyseraldehydi-konfiguraatio C-2-quiraalissa on D. Yleissopimuksen mukaan fischerin projisoinnin suhteen aldehydiryhmä on esitetty ylöspäin, hydroksimetyylifosfaattiryhmä alaspäin, hydroksyyliryhmä oikealle ja vetyatomi vasemmalle.
Ominaisuudet
3-fosfaattiglyseraldehydillä on molekyylimassa 170,06 g/mol. Gibbs -vapaan energianmuutos (ΔGº) mitä tahansa reaktiota varten on laskettava lisäämällä tuotteiden vapaan energian variaatio ja vähentämällä reagenssien vapaan energian variaation summa.
Se voi palvella sinua: Metazoa: Ominaisuudet, tyypit, elinympäristö ja sairaudetTällä tavoin vapaan energian vaihtelun (ΔGº) määritetään glyseraldehydi 3 -fosfaatista, joka on -1 285 kJ × mol-1. Valmistelukunnan mukaan tavanomaisessa tilassa 25 ºC ja 1 atm, puhtaiden elementtien vapaa energia on nolla.
Funktiot
Glykolyysi ja glukoneogeneesi
Glykolyysiä on läsnä kaikissa soluissa. Se on jaettu kahteen vaiheeseen: 1) energiainvestointivaihe ja metaboliittien synteesi korkealla fosfaattiryhmän siirtopotentiaalilla, kuten glyseraldehydi 3-fosfaatti (GAP); 2) ATP -synteesivaihe molekyyleistä, joilla on korkea siirtopotentiaali fosfaattiryhmään.
3-fosfaattiglyseraldehydi ja dihydroksiasetonifosfaatti. 3-fosfaattiglyseraldehydi muuttuu 1,3-bifosfoglyseraatiksi (1,3 bpg) entsyymirokojen dehydrogenaasin katalysoimalla reaktiolla, joka on katalysoitu.
Dehydrogenaasiroko katalysoi aldehydihiiliatomin hapettumista ja siirtää fosfaattiryhmän. Siten muodostetaan sekoitettu happoanhydridi (1,3bpg), jossa happoryhmä ja fosforiatomi ovat alttiita nukleofiiliselle hyökkäysreaktiolle.
Sitten 3-fosfoglysereraattikinaasin katalysoima reaktiossa 1,3 bpg siirtää fosfaattiryhmän hiilestä 1 ADP: hen, muodostaen ATP: n.
Koska aldolaasin katalysoimat reaktiot, dehydrogenaasiroko ja 3-fosfoglyseraattikinaasi ovat tasapainossa (ΔGº ~ 0), ovat palautuvia, joten ne ovat osa glukoneogeneesin polkua (tai uuden glukoosin synteesiä) polkua).
Vía de la Pentosa -fosfaatti- ja Calvin -sykli
Pentoosifosfaattitiellä 3-fosfaatti (GAP) glyseraldehydi ja 6-fosfaattifruktoosi (F6P) muodostetaan C-C-sidosten leikkaamisella ja muodostumisreaktioilla pentoosista, ksyluloosasta 5-fosfaatista ja riboosi 5 -fosfaatista.
Voi palvella sinua: Hyracoterium: Ominaisuudet, ravitsemus, lajit, lisääntyminen3-fosfaattiglyseraldehydi voi seurata glukoneogeneesin reittiä ja muodostaa 6-fosfaattiglukoosin, joka jatkaa pentoosifosfaatin reittiä. Glukoosi voidaan hapettaa kokonaan tuottamalla kuusi Co -molekyyliä2 Pontosa -fosfaattitien oksidatiivisen vaiheen läpi.
Calvin -syklissä CO2 Se on asetettu 3-fosfoglyseraatioksi, reaktiossa, jota katalysoidaan kylkiluun bifosfaattikarboksylaasi. Sitten 3-fosfoglyseraatio vähenee NADH: lla vaikutuksella entsyymin, jota kutsutaan aukkojen dehydrogenaasiksi.
2 rako -molekyyliä heksaosin biosynteesiä varten, kuten glukoosi, joka palvelee tärkkelystä tai selluloosan biosynteesiä kasveissa kasveissa.
Fruktoosin aineenvaihdunta
Fruktokinaasientsyymi katalysoi fruktoosin fosforylaatiota ATP: llä C-1: ssä, muodostaen 1-fosfaattifruktoosin. Aldolaasi A, joka löytyy lihaksesta, on spesifinen fruktoosille 1,6-bifosfaatille substraattina. Aldolaasi B löytyy maksasta ja se on spesifinen 1-fosfaattifruktoosille substraattina.
B-aldolaasi katalysoi fruktoosi 1-fosfaatin aldoolista repeämää ja tuottaa dihydroksiasetonin fosfaattia ja glyseraldehydia. Glyseraldehydi-kinaasi katalysoi glyseraldehydin fosforylaatiota ATP: n kautta muodostaen glykolyyttisen välittäjän, 3-fosfaatin glyseraldehydin (GAP).
Eri reitillä glyseraldehydi transformoi glyseroliksi alkoholidehydrogenaasilla, jota NADH käyttää elektronien luovuttajien substraattina. Sitten glyserolifosforylaattikinaasiglyseroli ATP: llä muodostaen glyserolifosfaatin. Tämä viimeinen metaboliitti on reoksi, muodostaen dihydroksiasetonin fosfaatin (DHAP) ja NADH: n.
DHAP muunnetaan rakoksi kolmella isomeasefosfaattientsyymillä. Tällä tavoin fruktoosi muunnetaan glykolyysimetaboliitteiksi. Laskimonsisäisesti toimitetut fruktoosi voi kuitenkin aiheuttaa vakavia vaurioita, jotka koostuvat solunsisäisen fosfaatin ja ATP: n dramaattisesta laskusta. Jopa maitohappoasidoosi tapahtuu.
Se voi palvella sinua: Chihuahua Flora ja eläimistö: Erinomainen lajiFruktoosivaurio johtuu siitä, että sillä ei ole säätelypisteitä. Ensinnäkin fruktoosi tulee lihaksiin GLUT5: n kautta, joka on riippumaton insuliinista.
Toiseksi fruktoosi muunnetaan suoraan rakoksi ja tällä tavoin se ei käy läpi fosfofuto -kinaasi (PFK) -entsyymin säätelyä glykolyysin alussa.
Entner-Doudoroffin kautta
Glykolyysi on universaali reitti glukoosikatabolismiin. Jotkut bakteerit käyttävät kuitenkin vuorotellen Entner-Doudoroff-tietä. Tämä reitti merkitsee kuusi askelta, joita entsyymit katalysoivat, joissa glukoosi muuttuu rakoksi ja pyruvatoksi, jotka ovat tämän tien kaksi lopputuotteita.
Gap ja pyruvaatti muuttuu etanoliksi alkoholisfermentointireaktioilla.
Viitteet
- Berg, J. M., Tymoczco, J. Lens., Stryer, l. 2015. Biokemia. Lyhyt kurssi. W -. H. Freeman, New York.
- Miesfeld, r. Lens., Mcevoy, m. M. 2017. Biokemia. W -. W -. Norton, New York.
- Nelson, D. Lens., Cox, m. M. 2017. Lehninger -biokemian periaatteet. W -. H. Freeman, New York.
- Saway J. G. 2004. Aineenvaihdunta yhdellä silmäyksellä. Blackwell, Malden.
- Voet, D., Voet, J. G., Pratt, c. W -. 2008. Biokemian perusteet: Elämä molekyylitasolla. Wiley, Hoboken.
- « Elohopeahydroksidirakenne, ominaisuudet, käytöt, riskit
- Traibitavoitteet ja kerrosten muodostuminen »

