Hydroksiapatiitti

- 701
- 79
- Dr. Travis Reichert
Selitämme, mikä on hydroksylapatiitti, sen rakenne, miten se syntetisoidaan, sen käyttö ja fysikaaliset ja kemialliset ominaisuudet
 Hydroksiapatiitti. Lähde: Rob Lavinsky, Irocks.com-cc-by-sa-3.0, CC BY-SA 3.0, Wikimedia Commons
Hydroksiapatiitti. Lähde: Rob Lavinsky, Irocks.com-cc-by-sa-3.0, CC BY-SA 3.0, Wikimedia Commons Mikä on hydroksiapatiitti?
Se Hydroksiapatiitti Se on kalsiumfosfaatti -mineraali, jonka kemiallinen kaava on CA10(PO4-A6(VAI NIIN)2. Yhdessä muiden mineraalien ja orgaanisten ja tiivistettyjen orgaanisten aineiden kanssa se muodostaa raaka -aineen, joka tunnetaan nimellä fosforikivi. Termi hydroxi viittaa anioniin OH-.
Jos anionin sijasta olisi fluoridia, mineraalia kutsutaan fluorapatitaksi (CA10(PO4-A6(F)2; Ja niin muiden anionien kanssa (Cl-, Br-, Yhteistyö32-, jne.-A. Samoin hydroksiapatiitti on luiden ja hammaskemelin pääasiallinen epäorgaaninen komponentti, pääasiassa kiteinen.
Joten, se on elintärkeä elementti elävien olentojen luukudoksissa. Hänen suuri stabiilisuus muita kalsiumfosfaatteja vastaan antaa hänelle tukea fysiologisia olosuhteita, jolloin luille on ominaista kovuus. Hydroksiapatiitti ei ole yksin: se täyttää sen toiminnan, johon liittyy kollageeni, konjunktiivisten kudosten kuituproteiini.
Hydroksiapatiitti (tai hydroksylapatiitti) sisältää Ca -ionit2+, Mutta muut kationit voivat myös olla sen rakenteessaan (MG2+, Naa+), epäpuhtaudet, jotka liittyvät luiden muihin biokemiallisiin prosesseihin (kuten niiden uusinta).
Hydroksiapatiittirakenne
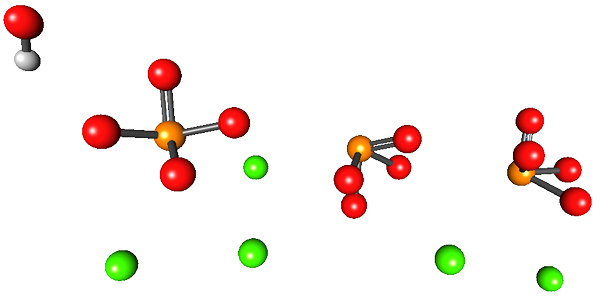
Ylivoimainen kuva kuvaa kalsiumhydroksiapatiitin rakennetta. Kaikki pallot miehittävät kuusikulmaisen "laatikon" puolet, missä toinen puoli on identtinen ensimmäisen kanssa.
Tässä rakenteessa vihreät pallot vastaavat Ca -kationeja2+, Vaikka punaiset pallot happiatomeihin, oranssi fosforiatomeihin ja valkoinen OH -vetyatomiin-.
Tämän kuvan fosfaatti -ioneilla on vika, että ei näytetä tetraedrista geometriaa; Sen sijaan ne näyttävät neliönpohjalta pyramidilta.
Voi palvella sinua: lasimainen tilaVAI NIIN- antaa vaikutelman, että se sijaitsee kaukana CA: sta2+. Kiteinen yksikkö voi kuitenkin toistaa itsensä ensimmäisen katolla, mikä osoittaa molempien ionien läheisen läheisyyden. Lisäksi nämä ionit voidaan korvata muilla (Na+ ja f-, Esimerkiksi).
Hydroksylapatiittisynteesi
Hydroksylapatiitti voidaan syntetisoida reaktiolla kalsiumhydroksidilla fosforihapon kanssa:
10 ca (OH)2 + 6 h3Poikki4 => CA10(PO4-A6(VAI NIIN)2 + 18 tuntia2JOMPIKUMPI
Hydroksiapatita (CA10(PO4-A6(VAI NIIN)2) ilmaistaan kahdella Formula CA -yksiköllä5(PO4-A3vai niin.
Samoin hydroksiapatiitti voidaan syntetisoida seuraavan reaktion avulla:
10 ca (ei3-A2.4H2O + 6 NH4H2Poikki4 => CA10(PO4-A6(VAI NIIN)2 + 20 NH4EI3 + 52 h2JOMPIKUMPI
Sademääränopeuden hallinta antaa tämän reaktion tuottaa hydroksiapatiitti -nanohiukkasia.
Hydroksiapatiittikiteitä

Ionit ovat tiivistettyjä ja kasvavat muodostaen jäykän ja resistentin biokriittisen. Tätä käytetään luun mineralisaation biomateriaalina.
Se tarvitsee kuitenkin kollageenia, orgaanista tukea, joka toimii kasvun muotina. Nämä kiteet ja niiden monimutkaiset muodostumisprosessit riippuvat luusta (tai hampaasta).
Nämä kiteet kasvavat impregnoituna orgaanisella aineella, ja elektronisten mikroskopiatekniikoiden levittäminen yksityiskohtaisesti hampaissa aggregaateina sauvamuodoilla, joita kutsutaan prismiksi.
Hydroksylapatiitti käyttää
Lääketieteellinen ja hammaslääketiede
Nanohydroksiapatiitti on houkutteleva käyttää sen samankaltaisuuttaan koon, kristallografian ja koostumuksen kanssa kovan ihmisen kudoksen kanssa, nanohydroksiapatiitti. Myös nanohydroksiapatiitti on bioyhteensopiva, bioaktiivinen ja luonnollista, sen lisäksi, että se ei ole myrkyllinen tai tulehduksellinen.
Tämän seurauksena nanohydroksiapatiittikeramiikassa on erilaisia sovelluksia, joihin sisältyy:
- Bone Tejido -leikkauksessa sitä käytetään onteloiden täyttämisessä ortopedisissa, traumatologisissa, maxillofacial- ja hammasleikkauksissa.
- Sitä käytetään ortopedisen ja hammasimplantin pinnoitteena. Se on desensibilisoiva aine, jota käytetään hampaiden valkaisuun. Häntä käytetään myös remineralisoivana aineena hammaspastassa ja varhaisessa karieshoidossa.
- Ruostumattomasta teräksestä valmistettu ja titaani -implantit peitetään usein hydroksiapatiittia niiden hylkäämisen nopeuden vähentämiseksi.
- Se on vaihtoehto luiden alogeenisille ja ksenogeenisille siirteille. Paranemisaika on lyhyempi hydroksiapatiitin läsnä ollessa kuin sen puuttuessa.
- Nanohidroksiapatiitti synteettinen jäljittely hydroksiapatiitiksi, joka on luonnollisesti dentiini ja apatiitti enmaltti, joten sen käyttö emalin korjaamisessa ja hammaslääketieteen liittäminen on edullista, samoin kuin suussa.
Muut hydroksiapatiitin käyttötarkoitukset
- Hydroksiapatiittia käytetään moottoriajoneuvojen ilmansuodattimissa niiden tehokkuuden lisäämiseksi hiilimonoksidin (CO) absorptiossa ja hajoamisessa. Tämä vähentää ympäristön pilaantumista.
- Alginaatti-hydroksiapatiittikompleksi on syntetisoitu, että kenttäkokeet ovat osoittaneet, että se kykenee absorboimaan fluoridia ioninvaihtomekanismin kautta.
- Hydroksiapatiittia käytetään kromatografisena väliaineena proteiineille. Tällä on positiivisia maksuja (CA++) ja negatiivinen (PO4-3), joten se voi olla vuorovaikutuksessa sähköisesti varautuneiden proteiinien kanssa ja sallia sen erottelun ioninvaihdoilla.
- Hydroksiapatiittia on käytetty myös tukena elektrofoottisille nukleiinihapoille. DNA: ta on mahdollista erottaa RNA: sta, samoin kuin kahden säikeiden DNA: n yksinkertaisen juosteen DNA.
Fysikaaliset ja kemialliset ominaisuudet
Hydroksiapatiitti on valkoinen kiinteä aine, joka voi hankkia harmaata, keltaista ja vihertäviä sävyjä. Kuten kiteinen kiinteä kiinteä kiinteä, se aiheuttaa korkeat fuusiopisteet, mikä osoittaa voimakkaita sähköstaattisia vuorovaikutuksia; Hydroksiapatiitissa tämä on 1100 ºC.
Se on tiheämpi kuin vesi, tiheys on 3,05 - 3,15 g/cm3. Lisäksi se on käytännössä liukenematon veteen (0,3 mg/ml), mikä johtuu fosfaatti -ioneista.
Happamassa väliaineessa (kuten HCL: ssä) se on kuitenkin liukoinen. Tämä liukoisuus johtuu CACL: n muodostumisesta2, Erittäin liukoinen vesisuola. Samoin fosfaatit ovat protonia (HPO42- ja h2Poikki4-) ja vuorovaikutuksessa paremmin vedellä.
Happaman hydroksiapatiitin liukoisuus on tärkeä karieksen patofysiologiassa. Suun ontelon bakteerit erittävät maitohappoa, glukoosin käymisen tuotetta, mikä vähentää hammaspinnan pH: ta alle 5: een, joten hydroksiapatiitti alkaa liukenemista.
Voi palvella sinua: sublimointi: käsite, prosessi ja esimerkitFluori (f-) Voit korvata OH -ionit- Kiteisessä rakenteessa. Kun tämä tapahtuu, se tarjoaa vastustuskyvyn hammaskemalien hydroksiapatiittia happojen edessä.
Mahdollisesti tämä vastus voi johtua CAF: n liukenemattomuudesta2 muodostettu kieltäytymällä "jättämästä" lasia.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs Ed., p. 349, 627). MC Graw Hill.
- Fluidinova. (2017). Hydroksylapatiitti. Haettu Fluidinovasta.com
- Gaiabulbanix. (5. marraskuuta 2015). Hydroksiapatiitti. [Kuva]. Commons.Wikimedia.org
- Martin.Neitov. (25. marraskuuta 2015). Hüroksüapatiidi Kristallid. [Kuva]. Commons.Wikimedia.org
- Wikipedia. (2018). Hydroksylapatiitti. Haettu jstk.Wikipedia.org
- Fiona Petchey. Luu. C14Dating toipunut.com

