Berylliumhydroksidi (BE (OH) 2)
- 4536
- 926
- Arthur Terry II
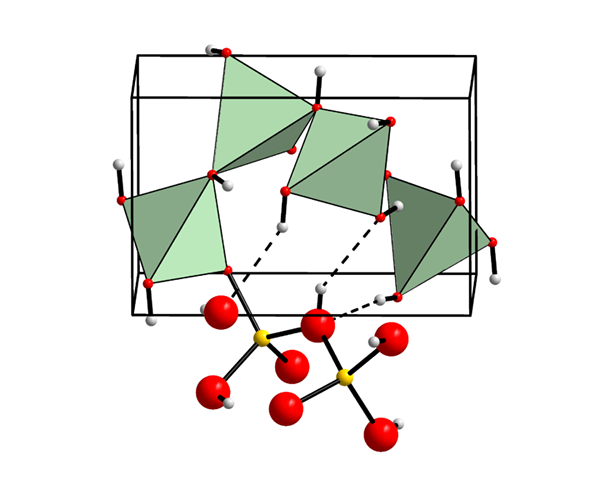
 Beryylihydroksidin kemiallinen rakenne. Lähde: Wikimedia Commons
Beryylihydroksidin kemiallinen rakenne. Lähde: Wikimedia Commons Mikä on berylhydroksidi?
Hän berylliumhydroksidi Se on kemiallinen yhdiste, joka on muodostanut kaksi hydroksidimolekyyliä (OH) ja berylliummolekyyli (BE). Sen kemiallinen kaava on (OH)2 Ja sille on ominaista amfotaattilaji. Yleensä se voidaan saada berylliumin ja vesimonoksidin välisestä reaktiosta seuraavan kemiallisen reaktion mukaan:
Beeo + H2O → Be (OH)2
Toisaalta tämä amfotaattiaine esittelee lineaarisen tyyppisen molekyylin kokoonpanon. Beryl -hydroksidin rakenteita voidaan kuitenkin saada: alfa- ja beetamuoto, kuten mineraali- ja höyryfaasi, käytetystä menetelmästä riippuen.
Beryylihydroksidin kemiallinen rakenne
Tätä kemiallista yhdistettä löytyy neljällä eri tavalla:
Beryl -alfa -hydroksidi
Lisäämällä kaikki emäksiset reagenssi. Esimerkki on esitetty alla:
2NAOH (laimennettu) + Becl2 → Ole (OH)2↓ + 2nacl
2NAOH (laimennettu) + suudelma4 → Ole (OH)2↓ + NA2Sw4
Beryyli Beeta -hydroksidi
Tämän alfatuotteen rappeutuminen muodostaa meta-stabiilin tetragonaalisen kiteisen rakenteen, joka on kulunut pitkäaikaisen ajanjakson jälkeen beryllium beeta-hydroksidiksi (β) nimeltään romomirakenne.
Tämä beetamuoto saadaan myös saostumana natriumberyllium liuoksesta hydrolyysillä olosuhteissa lähellä sulamispistettä.
Berilio -hydroksidi mineraaleissa
Vaikka se ei ole tavallista, beryylihydroksidi löytyy kiteisenä mineraalina, joka tunnetaan nimellä Behoite (jota kutsutaan tällä tavalla sen kemiallisen koostumuksen suhteen).
Se voi palvella sinua: Unforléninen happo: rakenne, ominaisuudet, synteesi, käyttääSitä esiintyy graniittisissa pegmatitaissa, jotka on muodostettu muuttamalla gadolinita (silikaattiryhmän mineraalit) vulkaanisissa fumaroleissa.
Tämä mineraali - heijastava uusi - löydettiin ensimmäisen kerran vuonna 1964, ja tällä hetkellä on löydetty vain Granite Pegmatitasista, jotka sijaitsevat Texasin ja Utahin osavaltioissa, Yhdysvalloissa.
Berylliumhydroksidihöyry
Yli 1.200 ° C (2.190 ° C), beryylihydroksidi on höyryvaiheessa. Se saadaan vesihöyryn ja beryylioksidin (BEEO) välisestä reaktiosta.
Samoin tuloksena olevan höyryn osittainen paine on 73 pA, mitattuna lämpötilassa 1.500 ° C.
Berilily -hydroksidiominaisuudet
Beryylihydroksidilla on molekyylimolekyylipaino tai likimääräinen molekyylipaino 43 0268 g/mol ja 1,92 g/cm tiheys3. Sen sulamispiste on lämpötilassa 1.000 ° C, jossa sen hajoaminen alkaa.
Mineraalina, BE (OH)2 (Beoita) on kovuus 4 ja sen tiheys vaihtelee välillä 1,91 g/cm3 ja 1,93 g/cm3.
Ulkomuoto
Berylliumhydroksidi on valkoinen kiinteä kiinteä, jolla alfa -muodossa on hyytelö ja amorfinen ulkonäkö. Toisaalta tämän yhdisteen beetamuoto muodostuu hyvin määriteltyyn, ortorromiseen ja stabiiliin kiteiseen rakenteeseen.
Voidaan sanoa, että mineraalin morfologia (OH)2 Se on monipuolinen, koska sitä voidaan löytää retikulaarisina, maarisarjoina tai pallomaisina aggregaattikiteinä. Samoin se esitetään valkoisella, vaaleanpunaisella, sinertävällä ja jopa värittömällä väreillä ja rasvaisella lasimaisella kiiltolla.
Lämpökemialliset ominaisuudet
Koulutuksen entalpia: -902,5 kJ/mol
Gibbs Energy: -815,0 kJ/mol
Voi palvella sinua: Kaasumainen kloori: Kaava, vaikutukset, käytöt ja riskitHarjoittelu entropia: 45,5 J/mol
Lämpökapasiteetti: 62,1 j/mol
Erityinen lämpökapasiteetti: 1 443 J/K
Vakioharjoittelu entalpia: -20,98 kJ/g
Liukoisuus
Berylliumhydroksidi on amfotilottu, joten se kykenee luovuttamaan tai hyväksymään protoneja ja liukenee sekä happo- että emäksisissä väliaineissa happo-emäsreaktiossa, tuottaen suolaa ja vettä.
Tässä mielessä BE (OH) liukoisuus2 Vedessä sitä rajoittaa liukoisuustuote KPS(H2O), joka on yhtä suuri kuin 6,92 × 10-22.
Altistumisriskit
Määritellyn beryylihydroksidiaineen laillinen sallittu ihmisen altistuminen (PEL tai OSHA) maksimipitoisuudella välillä 0,002 mg/m3 ja 0,005 mg/m3 Se on 8 tuntia ja pitoisuudelle 0,0225 mg/m3 korkeintaan 30 minuuttia.
Nämä rajoitukset johtuvat tosiasiasta, että beryllium on luetteloitu tyypin A1 syöpää aiheuttavana aineena (karsinogeeninen aine ihmisillä, jotka perustuvat epidemiologisten tutkimusten todisteisiin).
Bamey -hydroksidi käyttää
Se on hyvin rajallinen (ja epätavallinen) beryylihydroksidin käyttö raaka -aineena tuotteen käsittelyyn. Se on kuitenkin yhdiste, jota käytetään pääreagenssina muiden yhdisteiden synteesille ja metallin berylliumin saamiseksi.
Saada
Berylliumoksidi (BEEO) on kemiallinen yhdiste, jolla on korkea puhtaus beryllium, jota eniten käytetään teollisuudessa. Sille on tunnusomaista väritön kiinteä aine, jolla on sähköeristimen ominaisuudet ja korkea lämmönjohtavuus.
Tässä mielessä sen synteesin (teknisen laadun) prosessi suoritetaan seuraavasti:
- Beryl -hydroksidi liuotetaan rikkihapoon (H2Sw4-A.
- Suoritetaan reaktio, liuos suodatetaan siten, että oksidin tai sulfaatin liukenemattomat epäpuhtaudet eliminoidaan.
- Suodatus altistetaan haihtumiseen tuotteen keskittymiseksi, joka on jäähdytetty berylliumsulfaattikiteiden saamiseksi4.
- Suudelma4 Se kalsinoidaan tietyllä lämpötilassa välillä 1.100 ° C ja 1.400 ° C.
Lopputuotetta (BEEO) käytetään erityisten keraamisten osien valmistukseen teollisuuskäyttöön.
Metallisen berylliumin hankkiminen
Beryllium -mineraalien uuttamisen ja käsittelyn aikana syntyy epäpuhtauksia, kuten beryyli- ja berylihydroksidioksidi. Jälkimmäiseen kohdistuu muutossarjaa, kunnes metallinen beryllium.
Olla (oH) reagoi2 Ammoniumbifluori -liuoksella:
Ole (Voi)2 + 2 (NH4) Hf2 → (NH4-A2Bef4 + 2 h2JOMPIKUMPI
(NH4-A2Bef4 Se on lämpötilan nousu, kärsimystä lämpöhajoamisesta:
(NH4-A2Bef4 → 2NH3 + 2HF + BEF2
Lopuksi berylliumfluoridin vähentäminen lämpötilassa 1.300 ° C Magnesiumin (MG) kanssa johtaa metalliseen berylliumiin:
Bef2 + Mg → be + mgf2
Berylliumia käytetään metalliseoksissa, elektronisten komponenttien tuotanto, X -ray -laitteissa käytettyjen näytöiden ja säteilyikkunoiden valmistus.
Viitteet
- Wikipedia (S.F.-A. Berylliumhydroksidi. Haettu jstk.Wikipedia.org
- Holleman, a. F.; Wiberg, e. Ja Wiberg, N. (2001). Berylliumhydroksidi. Saatu kirjoista.Google.yhteistyö.mennä
- Julkaiseminen, m. D -d. (S.F.-A. Olla. Palautettu HandbookOfmineralogy.org
- Kaikki reaktiot (s.F.-A. Berylliumhydroksidi BE (OH)2. Saatu AllReactionista.com
- Pubchem (S.F.-A. Berylliumhydroksidi. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus
- Walsh, k. -Lla. ja Vidal, ja. JA. (2009). Beryllium -kemia ja prosessointi. Saatu kirjoista.Google.yhteistyö.mennä

