Inflamenooman aktivointi ja toiminnot
- 4202
- 1230
- Joshua Emmerich
Hän syttyjä Se on kompleksi, joka koostuu useista proteiinidomeeneista, jotka sijaitsevat solusytosolissa, jonka tehtävänä on toimia luontaisen immuunijärjestelmän reseptoreina ja anturina. Tämä alusta on puolustus Barrie.
Useat hiirien tutkimukset osoittavat tulehduksen roolin vakavien sairauksien esiintymisessä kansanterveydelle. Siksi on tutkittu huumeiden kehitystä, jotka vaikuttavat tulehduksellisten sairauksien parantamiseksi.
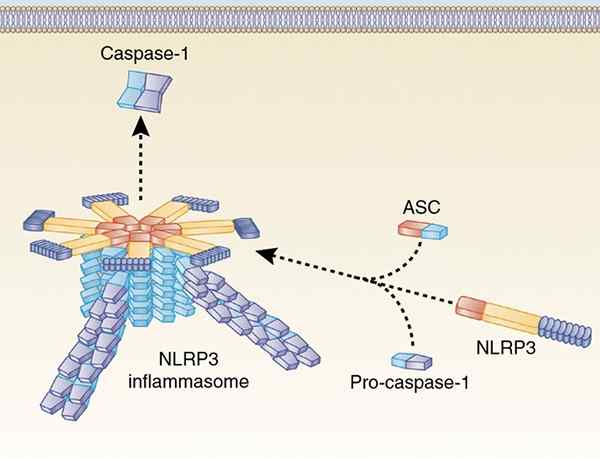 Tulehduksen rakenne. Kirjoittanut Haitao Guo [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by/4.0)], Wikimedia Commons.
Tulehduksen rakenne. Kirjoittanut Haitao Guo [CC BY-SA 4.0 (https: // creativecommons.Org/lisenssit/by/4.0)], Wikimedia Commons.
Tulehdukset indusoivat tulehduksellisia, autoimmuunisia ja neurodegeneratiivisia sairauksia, kuten multippeliskleroosi, Alzheimerin ja Parkinson Parkinson. Samoin kuin aineenvaihduntahäiriöt, kuten ateroskleroosi, tyypin 2 diabetes ja liikalihavuus.
Sen löytön teki joukko tutkijoita DR: n johdolla. Tschopp (Martinon 2002). Tämän rakenteen muodostuminen johtuu immuunivasteen induktiosta, jonka tarkoituksena on patogeenisten mikro -organismien eliminointi tai toiminta solujen tulehduksellisten prosessien anturina ja aktivaattorina.
Tämän alustan kokoonpano tuottaa Procaspaasi-1: n tai ProcasPA-11: n stimulaation, joka sitten aiheuttaa kaspaasi-1: n ja kaspaasi-11: n muodostumisen. Nämä tapahtumat ovat peräisin tyypin 1 interleusiini-1: n tulehduksellisten sytokiinien tuotannosta, nimeltään interleusiini-1 beeta (IL-1β) ja interleuciini-18 (IL-18), jotka ovat peräisin proil-1p: stä ja proil-18: sta.
Tulehdukset ovat tärkeitä rakenteita, jotka aktivoivat useat PAMP: t (patogeeniin liittyvät molekyylikuviot) ja kosteilla (vaurioihin liittyvät molekyylikuviot). Ne indusoivat interleukiini-1-beeta (IL-1β) ja interleukiini-18 (IL-18) proinflammatoristen sytokiinien (IL-18) (IL-18) leikkaus ja vapautuminen (IL-18) (IL-18). Ne muodostavat reseptori, jolla on nukleotidiyhdistysdomeeni (NLR) tai AIM2, ASC ja CASPASA-1.
Se voi palvella sinua: troofiset tasot ja sen muodostavat organismit (esimerkit)[TOC]
Tulehduksen aktivointi
Inflasoomat ovat sotilaita, jotka esiintyvät solusytosolissa. Tämäntyyppinen vaste johtuu epäilyttävien aineiden, kuten PAMP: ien ja patojen, läsnäolosta (Lamkanfi ym., 2014). Nukleotidiyhdistysdomeenin perheen (NLR) sytoplasmisten reseptorien aktivointi on peräisin kompleksista.
Joitakin esimerkkejä ovat NLRP1, NLRP3 ja NLRC4, samoin kuin muut reseptorit, kuten Melanooma 2: ssa puuttuvat niin kutsutut reseptorit (AIM2). Tässä ryhmässä tulehdus, jota on arvioitu suuremmassa määrin, on NLRP3, koska sen suuresta patofysiologisesta merkityksestä johtuu tartunta- ja tulehduksellisissa prosesseissa. Myös ASC-sovitin ja Caspasa-1-efektoriproteiini.
NLRP3: n syntymä
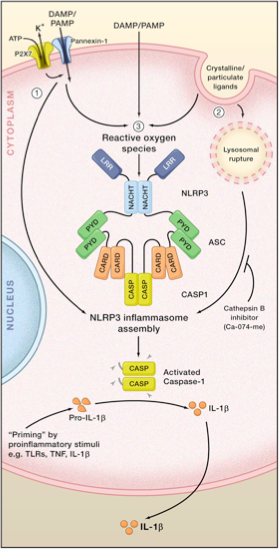
NLRP3 -tulensiirto syntyi vasteena signaaliryhmälle, joka voi olla bakteeri-, sieni-, alkueläin- tai viruskomponentit. Samoin kuin muut tekijät, kuten adenosiinitrifosfaatti (ATP), piidioksidi, virtsahappo, tietyt huokosinduktiiviset toksiinit, muun muassa (HALLE 2008). Kuvio 1 näyttää NLRP3 -rakenteen.
NLRP3 -flammasomi aktivoidaan monipuolisilla signaaleilla, jotka muistuttavat keinotekoista tulipaloa, joka osoittaa mainitulle rakenteelle, joka alkaa työskennellä. Esimerkkejä ovat solun kaliumin tuotos, reaktiivisten komponenttien tuottaminen happea mitokondrioista (ROS), kardiolipiinin, mitokondriaalisen DNA: n tai Catepsinan vapauttaminen.
Patogeenisiin mikro-organismeihin (PAMP) tai vaaran induktoreihin (kostea) ja tulehdusta edistäviin sytokiineihin (kuten TNF-a, IL-1β, IL-6, IL-18), heräävät NF-KB-KB. Tämä on signaali tulehduksen aktivoinnille NLRP3. Se indusoi NLRP3: n, Pro-IL1p: n ja Pro-IL-18: n ja tulehdusta edistävien sytokiinien, kuten IL-6, IL-8 ja TNF-a, tuotanto.
Seuraava signaali kertoo tulehdukselle NLRP3: lle, että se on koottu siten, että NLRP3/ASC/PRO-CASASA-1 -kompleksi ilmestyy, mikä ilmoittaa Caspasa-1: lle, joka on aktivoitava. Takaosan askel indusoi, että Pro-C-1β ja Pro-IL-18 kypsyvät ja ovat peräisin IL-1β: sta ja IL-18: sta niiden aktiivisissa muodoissa.
Se voi palvella sinua: Timolphthalein: Ominaisuudet, valmistelu ja sovelluksetIL-1β ja IL-18 ovat sytokiineja, jotka tukevat tulehduksellista prosessia. Myös näiden tapahtumien kanssa apoptoosi ja pyroptosi voivat ilmestyä.
 NLRP3 -aktivointimallit. Kirjoittanut RjOO317 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)], Wikimedia Commons.
NLRP3 -aktivointimallit. Kirjoittanut RjOO317 [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)], Wikimedia Commons.
Tulehduksen toiminnot
NLRP3 -infamosomi on makrofaageissa, monosyyteissä, dendriittisissä ja neutrofiileissä. Se voi olla enkeli, kun se hyökkää tarttuvia agentteja aktivoimalla tulehduksellinen prosessi. Tai päinvastoin, demoni, joka voi aiheuttaa useiden sairauksien etenemisen. Tämä on peräisin epäjärjestyksellisestä ja ilman kontrollin aktivointia, kun sen säätely vaikuttaa.
Inflamasoma on tärkein toimittaja joidenkin sairauksien fysiologian ja patologian tapahtumissa. On havaittu, että puuttuu tulehdukseen liittyviin vaivoihin. Esimerkiksi tyypin 2 diabetes ja ateroskleroosi (Duewell et ai, 2010).
Jotkut tutkimukset osoittavat, että itsetulehdukselliset oireyhtymät johtuvat NLPR3: n säätelyn ongelmista, jotka aiheuttavat erittäin syviä ja epäjärjestyksellisiä kroonisia tulehduksia, jotka ilmeisesti liittyvät IL-1p: n tuotantoon. Tämän sytosiinin antagonistien käytön myötä tauti vähentää sen haitallisia vaikutuksia kärsiviin yksilöihin (Meinzer ja Col, 2011).
Tulehduksen rooli sairauksien kehityksessä
Jotkut tutkimukset ovat osoittaneet, että tulehdukset ovat tärkeitä maksasairauksien aikana aiheutuneissa vaurioissa. Imaeda et ai. (2009) viittaavat siihen, että tulehduksellisella NLRP3: lla on asetaminofeenin hepatotoksisuus. Näissä tutkimuksissa havaitaan, että hiirillä, joilla on asetaminofeenilla ja NLRP3: n puute, on vähemmän kuolleisuutta.
NLRP3 -tulenpalkki toimii suoliston homeostaasisäätimenä moduloimalla immuunivastetta suoliston mikrobiotalle. Puutteellisissa hiirissä NLRP3: ssa mikrobiotan määrä ja tyyppi (Dupaul-Chicoine et ai., 2010) muutokset.
Yhteenvetona voidaan todeta, että tulehdukselliset voivat toimia hyvällä puolella molekyylialustana, joka hyökkää infektioita, samoin kuin tumma puolta, kuten Parkinsonin aktivaattori, Alzheimer, diabetes mellitus tyyppi 2 tai ateroskleroosi, mainitsemaan vain joitain.
Voi palvella sinua: Proteiinin denaturointi: Mikä on, tekijät, seurauksetViitteet
- Strowig, t., Henao-Mejia, J., Elinav, E. & Flavell, R. (2012). Terveyden ja sairauden tulehdukset. Nature 481, 278-286.
- Martinon F, Burns K, Tschopp J. (2002). InflammaMome: Molekyylialustalle, joka laukaisee tulehduksellisten kaspaasien aktivoitumisen ja proil-beetin käsittelyn. Moll Cell, 10: 417-426.
- Guo H, Callaway JB, Ting JP. (2015). Tulehdukset: toimintamekanismi, rooli sairauksissa ja terapeuttiset lääkkeet. Nat Med, 21 (7): 677-687.
- Lamkanfi, m. & Dixit, V.M. (2014). Tulehduksen mekanismit ja toiminnot. Solu, 157, 1013-1022.
- Falle A, Hornung V, Petzold GC, Stewart CR, Monks BG, Reinheckel T, Fitzgerald KA, Latz E, Moore KJ ja Golenbock DT. (2008). NALP3-inflammatoimi on mukana synnynnäisessä immuunivasteessa amyloidi-beetaan. Nat. Immunol, 9: 857-865.
- Duewell P, Kono H, Rayner KJ, Sirois CM, Vladimer G, Bauernifeind FG, et ai. (2010). NLRP3 -tulehdukset vaaditaan. Nature, 464 (7293): 1357-1361.
- Meinzer U, Quartier P, Alexandra J-F, Hentgen V, Execadez F, Koné-PAUT I. (2011). Interleukiini-1, joka kohdistuu lääkkeisiin Välimeren kuumeen: tapaussarja ja kirjallisuuskatsaus. Semin niveltulehdus Rheum, 41 (2): 265-271.
- Dupaul-Chicoinine J, Yeretsian G, Doiron K, Bergstrom KS, McIntire CR, LeBlanc PM, et ai. (2010). Suoliston homeostaasin, koliitin ja koliittien assosioituneen kolorektaalisyövän hallinta tulehduksellisten kaspaasien avulla. Immuniteetti, 32: 367-78. Doi: 10.1016/j.Imuni.2010.02.012

