Isomería
- 4701
- 68
- Ronald Reilly
Mikä on isomeria?
Isomería on kemiallinen ilmiö, joka on karakterisoitu, joissa molekyyleillä, joilla on sama määrä atomeja, on erilaiset kemialliset tai fysikaaliset ominaisuudet. Siten se esiintyy isomeereissä, jotka puolestaan ovat molekyylejä, joiden kemialliset kaavat ovat samat, mutta niiden rakenteet tai alueelliset säännökset eroavat huomattavasti toisistaan.
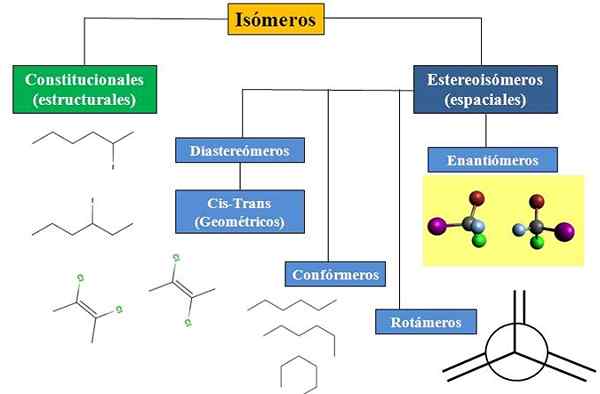
Meillä on perustuslaillinen tai rakenteellinen isomeria ja avaruus isomería, joka keskittää paljon huomiota stereokemiaan. Alemman kuvan virtauskaavio osoittaa, että isomeerit on jaettu pääasiassa mainituihin kahteen tyyppiin: perustuslailliset ja stereoisomeerit.
 Virtakaavio erityyppisille isomeereille orgaanisessa kemiassa. Lähde: Gabriel Bolívar.
Virtakaavio erityyppisille isomeereille orgaanisessa kemiassa. Lähde: Gabriel Bolívar. Kaikilla isomeereillä, tietylle yhdisteelle, on sama kemiallinen kaava. Mutta rakenteet, jotka voivat rakentaa näitä atomeja ja niiden mittasuhteita, ovat ainutlaatuisia jokaiselle molekyylille tai isomeerille. Lisäksi, vaikka rakenne itsessään olisi sama, atomit tai ryhmät voivat käyttää erilaisia alueellisia asemia.
Virtakaaviossa on esitetty esimerkkejä isomeereistä, joita käsitellään seuraavissa osissa.
Isomeerien tyypit
Perustuslaki
Perustuslailliset tai rakenteelliset isomeerit eroavat molekyylin luurankon järjestyksessä. Eli niiden atomeja ei ole kytketty samalla tavalla, joten kyseiset rakenteesta tai funktionaaliset ryhmät voivat tulla hyvin erilaisiksi.
Esimerkiksi samalle kemialliselle kaavalle C7H10Tai voi olla useita molekyylejä, jotka täyttävät atomien määrän; Kaikilla on yksi happiatomi, mutta muiden atomien rakenteellinen sijoitus on ainutlaatuinen jokaiselle isomerille.
Ja siksi kaikkien perustuslaillisten isomeerien kemialliset ja fysikaaliset ominaisuudet kaavalle C7H10Tai eroavat myös suuresti toisistaan.
Toisaalta perustuslailliset isomeerit voivat olla hyvin yksinkertaisia, vaihtelevat vain yhden atomin tai ryhmän suhteellisessa sijainnissa. Seuraavassa osassa näkyy esimerkki tästä ja yllä olevasta.
Stereoisomeerit
Stereoisomeerit ovat niitä, joilla on sama rakenteellinen järjestys, mutta eroavat atomien tai ryhmiensa alueellisissa asemissa ja suuntauksissa.
Voi palvella sinua: moduloitu amplitudiJotta niiden olemassaolo olisi mahdollista, molekyylien on sisällettävä stereogeenisiä keskuksia, jotka ovat orgaanisessa kemiassa tunnetuimpia epäsymmetrisiä tai kiraalisia hiiliatomeja; eli neljällä eri substituentilla.
Epäsymmetristen hiilien lisäksi pidetystä molekyylistä on puuttuva symmetriaelementit. Muuten alueellisen järjestelmän on mahdotonta kertyä stereoisomiin.
Enantiomeerit
Enantiomeerit ovat stereoisomeerejä, jotka koostuvat ei -superimentaalisista peilikuvista. Esimerkiksi oikeat ja vasen kädet eivät ole päällekkäisyyksiä, aivan kuten kengät tai käsineet. Seuraavassa osassa käsitellään Enantiomeían klassista esimerkkiä: bromokloreyodometaani: cbrcli.
Diastreomerit
Diastreomerit puolestaan ovat myös stereoisomeerejä, mutta eivät ole spekulaarisia kuvia. Toisin sanoen, joka asetetaan toisten eteen, ei ole itsestään heijastus. Tunnetuimmista diastomeereista meillä on cis-trans isomeria, jota kutsutaan myös geometrisiksi isomerioiksi, etenkin kun sitä sovelletaan alkeeniin.
Konformerot
Konformerit, vaikka he olisivat stereoisomin spektrissä, eivät oikeastaan ole isomeerejä. Nämä ovat avaruuskonfiguraatioita, joita molekyyli tietyssä vaiheessa tai energiatila hankkii useiden sen linkkien kiertämisen kautta. Esimerkki konformereista n-heksaani.
Rotámeros
Lopuksi meillä on rotarmerit, jotka muistuttavat konformereita siinä mielessä.
Yhden linkin kahden hiiliatomin välillä otetaan kuitenkin vertailuna, ja suhteellisia sijainteja verrataan, pimennettynä tai vaihdettuna, substituenteihin molemmille hiileille. Myöhemmin esimerkki propeenirotaartereista nähdään.
Esimerkkejä isomeereistä
Heksaani jodi
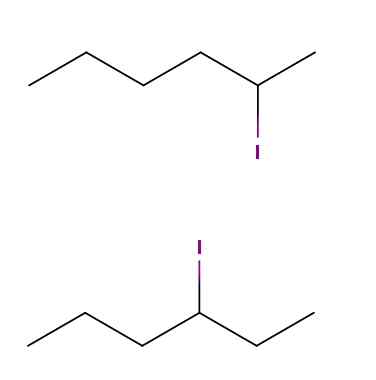 Heksaanin jodin perustuslailliset isomerit. Lähde: Gabriel Bolívar Molviewin kautta.
Heksaanin jodin perustuslailliset isomerit. Lähde: Gabriel Bolívar Molviewin kautta. Yllä on kaksi molekyyliä, joiden kemialliset kaavat ovat c6H13Yllyttää. Ensimmäisessä meillä on 2-jodhexan, kun taas toisessa 3-adhexan. Ne ovat paikallisia perustuslaillisia isomeerejä, koska luuranko on sama, erolla, että jodiatomin sijainti vaihtelee hiilestä toiseen.
Voi palvella sinua: Staattinen kitka: Kerroin, esimerkki, liikuntaC3H8JOMPIKUMPI
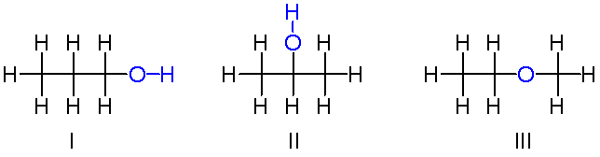 Lähde: V8RIK, CC BY-SA 3.0, Wikimedia Commons
Lähde: V8RIK, CC BY-SA 3.0, Wikimedia Commons Ylös meillä on toinen esimerkki kemiallisen kaavan C perustuslaillisista isomeereistä3H8JOMPIKUMPI. Molekyylit I ja II ovat vastaavasti 1-propanolia ja 2-propanolia. Molemmat ovat alkoholia. Sen sijaan molekyyli III on etyyli-metyyli.
Siksi puhumme toisesta toiminnallisesta ryhmästä. Huomaa, että kolmella molekyylillä on sama määrä atomeja, mutta niiden rakenteet ovat erilaisia.
2,3-deklooro-2-buteeni
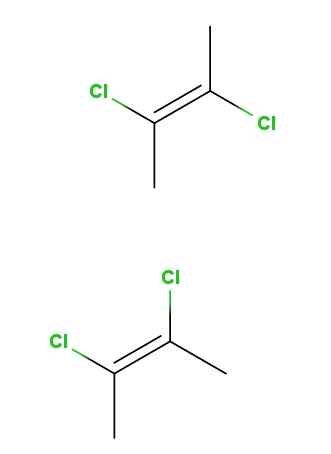 Geometriset isomeerit, joissa on 2,3-dekloro-2-buteenia. Lähde: Gabriel Bolívar Molviewin kautta.
Geometriset isomeerit, joissa on 2,3-dekloro-2-buteenia. Lähde: Gabriel Bolívar Molviewin kautta. Ylös meillä on Trans-22,3-Declolor-2-Butene-isomeeri ja CIS-2,3-dikloori-2-Butene-isomeerin alapuolella. Ensimmäisessä klooriatomeja löytyy vastakkaisissa asennoissa, jotka koskevat kaksoissidoksen suhteen, kun taas toisessa ne sijaitsevat kaksoisidon samalla puolella.
Molempien molekyylien luuranko on sama, mutta eroavat klooriatomien alueellisissa asemissa; Siksi he ovat stereoisomeerejä, eivätkä ne ole spekulaarisia kuvia, niistä tulee diamapereita.
3-flúor-2-metyylisikohexan
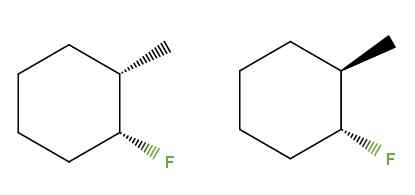 3-flúor-2-metyylisikoheksano-diastereomers. Lähde: Gabriel Bolívar Molviewin kautta.
3-flúor-2-metyylisikoheksano-diastereomers. Lähde: Gabriel Bolívar Molviewin kautta. Tällä kertaa kaksoissidoksen sijasta meillä on sykloheksinen rengas 3-flúor-2-metyylisilmohexan-yhdisteelle. Vasemmalla olevassa isomeerissä ryhmät3 ja F sijaitsevat rengastason alapuolella; Oikealla puolella, Cho3 on ylös ja f alla.
Siksi vasemmalla oleva vastaa cis -isomeeriä, ja oikealla puolella olisi trans -isomeeri. Siksi ne ovat diamaperomeerejä, koska ne eivät ole enää spekulaarisia kuvia.
Conformeros del n-heksaani
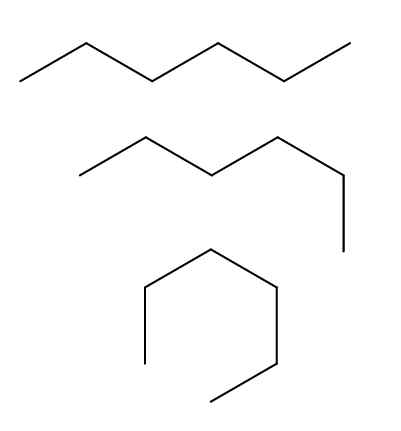 N-heksaanin konformerit. Lähde: Gabriel Bolívar Molviewin kautta.
N-heksaanin konformerit. Lähde: Gabriel Bolívar Molviewin kautta. Meillä on kolme konformeria n-Heksaano, joka johtuu hiilihapotetun ketjun kierroksista ja ”taitoksista” eri suunnissa. Kaikki vastaavat samaa molekyyliä n-Heksaani, jolla on erilaiset taitteet, mikä riippuu kunkin molekyylin ympäristöstä ja sisäisestä energiasta.
3-bromi-2-penoli
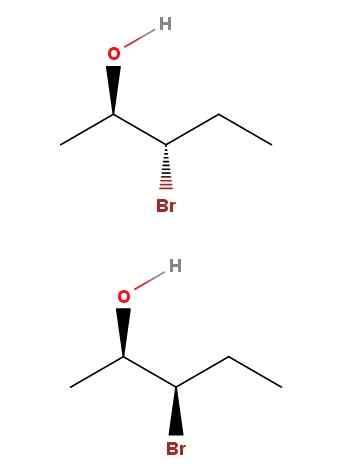 3-bromi-2-pentanolin diastreomeerit. Lähde: Gabriel Bolívar Molviewin kautta.
3-bromi-2-pentanolin diastreomeerit. Lähde: Gabriel Bolívar Molviewin kautta. 3-bromo-2-pantanolissa meillä on toinen esimerkki diastereomeereistä. Huomaa, että jälleen kerran, yllä olevassa isomeerissä meillä on OH ja BR osoittavat kohti ohjeita luurankon tason vastaisia; Alla olevassa isomeerissä molemmat ryhmät osoittavat lukijan suuntaan.
Se voi palvella sinua: termodynamiikan toinen laki: kaavat, yhtälöt, esimerkit1-bromi-3-kloori-5-etyylisikloheksan
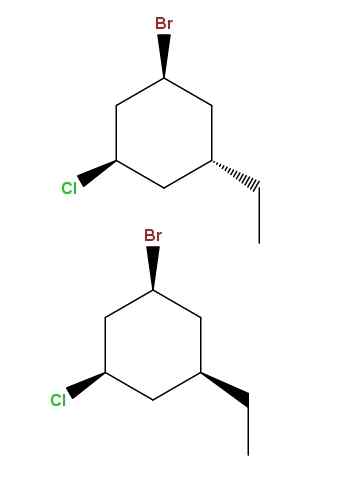 1-BROMO-3-Clor-5-etyylisikloheksanin diastreomeerit. Lähde: Gabriel Bolívar Molviewin kautta.
1-BROMO-3-Clor-5-etyylisikloheksanin diastreomeerit. Lähde: Gabriel Bolívar Molviewin kautta. Ja jälleen kerran, meillä on toinen pari diastereomeerejä, erolla, että ero on nyt yhden ryhmän alueellisessa asemassa: etyyli, -CH2CH3.
Tämäntyyppisillä isomeereillä on hyvin erityinen nimi: epigmerit, jotka ovat diastheomereita, joiden vaihtelua havaitaan vain yhden epäsymmetrisen hiilen alueellisessa kokoonpanossa; Tässä tapauksessa se, joka on kytketty -CH: hon2CH3.
Bromokloreyodometaani
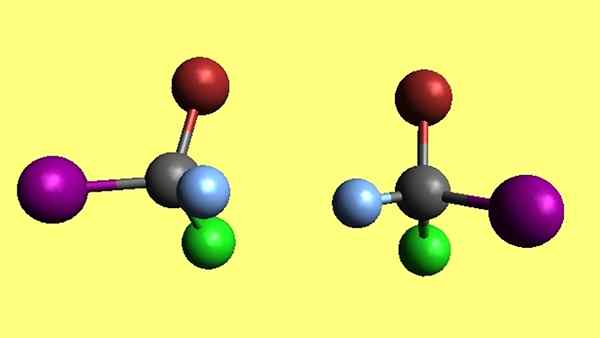 Bromokloreyodometaanien enantimeerien pari. Lähde: Gabriel Bolívar.
Bromokloreyodometaanien enantimeerien pari. Lähde: Gabriel Bolívar. Huomaa, että bromoclloroyodometaanin kaksi molekyyliä, CBRCLI, ovat enantiomeerejä. Niin paljon kuin yrität, neljä atomiasi eivät koskaan ole samaan. Sanotaan, että heillä on vastakkaisia avaruuskokoonpanoja.
2-bromi-4-etyylisiklohexan
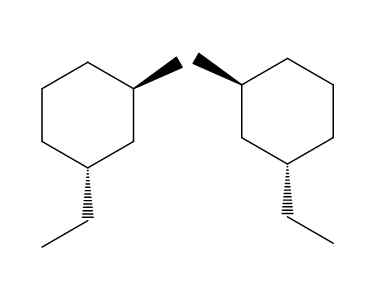 2-bromi-4-etyylisikloheksanin inantimerit. Lähde: Gabriel Bolívar Molviewin kautta.
2-bromi-4-etyylisikloheksanin inantimerit. Lähde: Gabriel Bolívar Molviewin kautta. 2-bromi-4-etyylisikloheksanimolekyylien vääntömomentin esimerkissä. Jos yritämme kääntää oikeanpuoleisen molekyylin, näemme, että ryhmä -CH2CH3 Se ei sijaitse renkaan alapuolella, vaan yllä.
Samoin Cho3 Se ei osoita rengasta, vaan alla. Avaruusasetukset sijoitetaan, ne ovat vastakkaisia. Tämä on toinen enatiomeían tärkeimmistä piirteistä.
Rotámeros del Propileno
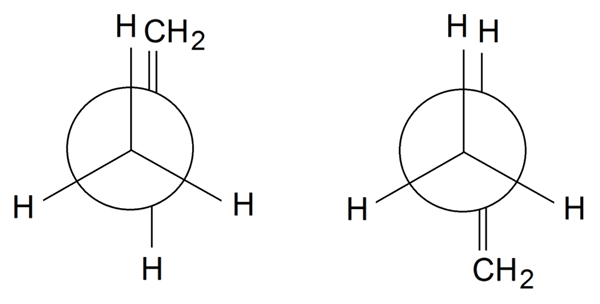 Rotámeros del Propileno. Lähde: Samuele Madini, CC BY-SA 4.0, Wikimedia Commons
Rotámeros del Propileno. Lähde: Samuele Madini, CC BY-SA 4.0, Wikimedia Commons Rotámeros del Propileno -tapahtumassa, päättymään, kiertämme yksinkertaisen linkin c: n välillä1 ja c2: H3C-ch = ch2. Ryhmä = ch2 Se on varjostetussa asennossa yhden H: n H: n kanssa3 Edessä vasemmalla olevassa rotameerissa. Samaan aikaan = Cho2 Ja h ovat vuorotetuissa asennoissa oikeassa.
Ryhmien pimennyksestä tai ei. Siksi oikeanpuoleinen rota on vakaampi kuin vasemmalla oleva.
Viitteet
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10th Painos.-A. Wiley Plus.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Morrison ja Boyd. (1987). Orgaaninen kemia. (Viides painos). Addison-Wesley Iberoamericana.
- DR. S. Gevorg. (2020). Enantiomeerit, diastreomeerit, identtiset tai perustuslailliset isomeerit. Kemian vaiheet. Toipunut: kemistroysteps.com
- Wikipedia. (2020). Isomeeri. Haettu: vuonna.Wikipedia.org
- Allison Soult. (13. elokuuta 2020). Isomeerit. Kemian librettexts. Palautettu: Chem.Librettexts.org
- James Ashenhurst. (2020). Stereokemia ja kiraalisuus. Toipunut: MasterorganicChemistry.com

