Lysiinin ominaisuudet, rakenne, toiminnot, biosynteesi
- 2396
- 318
- Gustavo Runte DVM
Se lysiini (Lys, K -k -) tai ε-diaminoproinihappo, Se on yksi 22 aminohapposta, jotka tekevät.
Drechsel havaitsi sen vuonna 1889 kasinogeenin hydrolyysin (hajoamisen) tuloksena. Vuosia myöhemmin Fischer, Siegfried ja Hedin päättivät, että se oli myös osa proteiineja, kuten gelatiinia, muna -albumiinia, konglutinia, fibriiniä ja muita proteiineja.
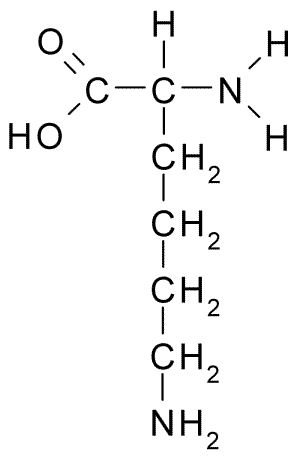
 Aminohappolysiinin kemiallinen rakenne (lähde: borb, Wikimedia Commonsin kautta)
Aminohappolysiinin kemiallinen rakenne (lähde: borb, Wikimedia Commonsin kautta) Sen esiintyminen osoitettiin sitten siementen taimissa itämisessä ja useimmissa tutkituissa vihannesproteiineissa, jotka määrittivät niiden runsauden kaikkien soluproteiinien yleisenä ainesosana elementtinä.
Sitä pidetään yhtenä tärkeimmistä "rajoittavista" aminohapoista viljoissa runsaasti ja tästä syystä ajatellaan, että maailman erilaisten alikehittyneiden populaatioiden kuluttama proteiinipitoisuus vaikuttaa.
Jotkut tutkimukset ovat päättäneet, että lysiinin saanti suosii insuliinin ja glukagonhormonien tuotantoa ja vapautumista, jolla on tärkeitä vaikutuksia kehon energian aineenvaihduntaan.
[TOC]
Ominaisuudet
Lysiini on positiivisesti ladattu a-aminohappo.53, mikä viittaa siihen, että fysiologinen pH, substituentin aminoryhmäsi on täysin ionisoitu, antaen positiivisen nettokuorman aminohappoon.
Sen esiintyminen erityyppisten elävien organismien proteiineissa on lähellä 6% ja erilaiset kirjoittajat katsovat, että lysiini on välttämätöntä kudosten asianmukaiselle kasvulle ja korjaamiseksi.
Soluilla on paljon lysiinijohdannaisia, jotka täyttävät suuren monimuotoisuuden fysiologisia toimintoja. Näissä ovat hydroksilisiini, metyyli-lysiini ja muut.
Se on ketogeeninen aminohappo, joka tarkoittaa, että sen aineenvaihdunta tuottaa välityssubstraattien hiilihapotettuja luurankoja molekyylien muodostumisreiteille, kuten asetyyli-CoA, kun maksan seuraavan ketonirunkojen muodostuminen muodostuu maksassa.
Toisin kuin muut välttämättömät aminohapot, tämä ei ole glykogeeninen aminohappo. Toisin sanoen sen hajoaminen ei lopu glukoosin tuottavien reittien välittäjien tuotantoon.
Rakenne
Lysiini luokitellaan emäksisten aminohappojen ryhmään, joiden sivuketjuilla on ionisoitavia ryhmiä, joilla on positiivinen kuorma.
Sen sivuketjussa tai R R -ryhmässä on toinen ensisijainen aminohuryhmä, joka on kiinnitetty hiiliatomiin sen alifaattisen ketjun ε-asennossa, joten sen nimi “ε-aminocaproico”.
Siinä on a-hiiliatomi, jolle vetyatomi, aminohuryhmä, karboksyyliryhmä ja R-sivuketju r, jolle on ominaista molekyylinen kaava (-CH2-CH2-CH2-CH2-NH3+), liitetään.
Koska sivuketjussa on kolme metyleeniryhmää, ja vaikka lysiinimolekyylillä on aminoryhmä, jolla on positiivinen varaus fysiologisesta pH: sta, tällä ryhmällä R on vahva hydrofobinen luonne, joten se on usein haudattu proteiinirakenteisiin, jättäen vain ε- aminoryhmä.
Lysiinin sivuketjun aminohuryhmä on erittäin reaktiivinen ja osallistuu yleensä monien proteiinien aktiivisiin keskuksiin, joilla on entsymaattinen aktiivisuus.
Funktiot
Lysiini, joka on välttämätön aminohappo, suorittaa useita toimintoja, kuten mikrotravinteita, etenkin ihmisillä ja muilla eläimillä, mutta se on myös metaboliitti eri organismeissa, kuten bakteereissa, hiivoissa, kasveilla ja levällä.
Sivuketjun ominaisuudet, erityisesti hiilivetyketjuun kiinnitetyn ε-amino-ryhmän ominaisuudet, jotka kykenevät muodostamaan vety silloja, antavat sille erityisiä ominaisuuksia, jotka tekevät siitä osallistumaan katalyyttisiin reaktioihin erityyppisissä entsyymeissä.
Se voi palvella sinua: Zacatecasin kasvisto ja eläimistö: edustavampi lajiSe on erittäin tärkeää lihasten normaalin kasvun ja uudelleenmuodostumisen kannalta. Lisäksi se on karnitiinin edeltäjä molekyyli, maksassa, aivoissa ja munuaisissa syntetisoitu yhdiste, joka on vastuussa rasvahappojen kuljettamisesta mitokondrioihin energiantuotannossa.
Tämä aminohappo on välttämätön myös synteesille ja kollageenin muodostumiselle, joka on ihmiskehon sidekudoksen järjestelmän tärkeä proteiini, joten se myötävaikuttaa ihon ja luiden rakenteen ylläpitämiseen.
Se on kokeellisesti tunnistanut toiminnot:
- Suoliston suojaaminen stressaaville ärsykkeille, saastuminen bakteerien ja viruspatogeenien kanssa jne.
- Vähennä kroonisia ahdistuneisuusoireita
- Suosittele heikkolaatuisten ruokavalioiden kasvavien imeväisten kasvua
Biosynteesi
Ihmiset ja muut nisäkkäät eivät pysty syntetisoimaan aminohappolysiiniä In vivo Ja tästä syystä heidän on saatava se eläin- ja kasviproteiineilta, jotka on nautittu ruokaa.
Luonnollisessa maailmassa on kehittynyt kaksi erilaista reittiä lysiinin biosynteesiin: toiseen, joka käyttää bakteereja, kasveja ja sieniä "alempi" ja toinen Euglénidesin ja "ylivoimaisten" sienten käyttämä.
Lysiini -biosynteesi kasveissa, alemmat sienet ja bakteerit
Näissä organismeissa lysiini saadaan diaminoopimaelihaposta 7 -askeleen reitin kautta, joka alkaa pyruvaattia ja puoliksi -eettisellä aspartaatilla. Esimerkiksi bakteereille tämä reitti merkitsee lysiinin tuotantoa (1) proteiinisynteesin tarkoituksiin, (2) (3) lysiinin diaminopimellaatin ja synteesien synteesiin, jota käytetään pepidoglinin soluseinämässä.
Aspartaatti, organismit, jotka esittävät tätä reittiä, ei vain Lisinaa, vaan myös johdetaan metioniinin ja Treoninen tuotannossa.
Erilainen reitti puolivälissä Asp.
Lysiini -biosynteesi Superior- ja Euglénidos -sienissä
Lysiinisynteesi Novo Ylivoimaisissa sienissä ja Euglénid-mikro-organismeissa se tapahtuu L-a-aminoadipato-välittäjän kautta, joka muuttuu useita kertoja eri tavoin kuin bakteereissa ja kasveissa tapahtuvat.
Reitti koostuu 8 entsymaattista vaihetta, joihin liittyy 7 vapaata välittäjää. Reitin ensimmäinen puoli tapahtuu mitokondrioissa ja saavuttaa a-aminoadipato-synteesin. Α-aminoadipato-muuntaminen L-Lisiinissä tapahtuu myöhemmin sytosolissa.
- Reitin ensimmäinen vaihe koostuu a-ketoglutaraatti- ja asetyyli-CoA-molekyylien kondensaatiosta entsyymi-homochitraattisyntaasilla, joka tuottaa homoosittista happoa.
- Homoksinen happo on kuivunut hapolla IVY-Homoaconitic, joka muuttuu sitten homoisositikkohappoksi homoaconitasa -entsyymillä.
- Homoisositrinen happo hapettuu homoisostraattidehydrogenaasilla, jolla saavutetaan siirtymävaiheinen oksiglutaraattien muodostuminen, joka menettää hiilidioksidimolekyylin (CO2) ja päättyy a-katodipihapona.
- Tämän viimeisen yhdisteen transaminoimalla glutamaatista riippuvainen prosessi aminotransferaasin aminoadipate-entsyymin vaikutuksen ansiosta, joka tuottaa L-a-aminoadipiinihappoa.
- L-α-aminoadipiinihapon sivuketju pelkistetään muodostamaan L-a-aminoadipic-δ-semia-assess.
- Sacoopine reduktaasi ja katalysoi. Myöhemmin imino vähenee ja sakoopine saadaan.
- Lopuksi, hiilidippisidos sakaopiinin osassa glutamaatissa "leikkaa" sakryymi-sakryraopiinidehydrogenaasilla, antautuen lopputuotteina L-Lisin ja a-zetoglutararaattihappo.
Vaihtoehtoja lysiinille
Kokeelliset testit ja rottien kanssa suoritetut analyysit ovat saaneet selvittää, että ε-N-Asetyyli-lysiini voi korvata lysiinin tukemaan nuorten kasvua ja tämä entsyymin läsnäolon ansiosta: ε-lisiini acilaasi.
Se voi palvella sinua: Afottinen vyöhyke: Ominaisuudet, kasvisto, eläimistöTämä entsyymi katalysoi ε: n hydrolyysiä-N-asetyylilysiini lysiinin tuottamiseksi ja tekee niin nopeasti ja runsaasti.
Heikkeneminen
Kaikissa nisäkkäiden lajeissa lysiinin hajoamisen ensimmäisen vaiheen katalysoi lysiini-2-oksoglutaraattientsyymi reduktaasi, joka kykenee muuttamaan lysiinin ja a-oksoglutaraatin sacalopiiniksi, aminohapposjohdannaisjohdannaismahdollisuuksissa ja kenen olemassaolo heissä osoitettiin 60 -luvun lopulla.
Sakrooppi on palannut a-aminoadipato Δ-SemialDehidiin ja glutamaattiin entsyymin sacaropiinidehydrogenaasin vaikutuksella. Toinen entsyymi pystyy myös käyttämään sacaropinaa substraattina hydrolyziin.
Sakaropiinilla, jolla on yksi tärkeimmistä metabolisista välittäjistä lysiinin hajoamisessa, on korvaava nopeus fysiologisissa olosuhteissa, erittäin korkeat, joten se ei keräänty nesteisiin tai kudoksiin, jotka on osoitettu kehittäjä -dehydrogenaasin korkeat aktiivisuudet, jotka ovat löydetty.
Lysiinin aineenvaihduntaan osallistuvien entsyymien määrä ja aktiivisuus riippuu kuitenkin suurelta osin kunkin tietyn lajin erilaisista geneettisistä näkökohdista, koska on olemassa luontaisia variaatioita ja spesifisiä kontrolli- tai säätelymekanismeja.
"Sacaropinuria"
Aminohappojen, kuten lysiinin, sitruliinin ja histidiinin, runsaan menetyksen runsaaseen menetykseen liittyy patologinen tila virtsan kautta ja tätä kutsutaan "saropinuria". Sacaropiini on lysiinimetabolian aminohappojohdannainen, joka erittyy yhdessä kolmen "saropinurisen" potilaiden virtsassa mainittujen aminohappojen kanssa.
Sacaropiini löydettiin alun perin oluthiivassa ja se on lysiinin edeltäjä näissä mikro -organismeissa. Muissa eukaryoottisissa organismeissa tätä yhdistettä tuotetaan lysiinin hajoamisen aikana hepatosyyttien mitokondrioissa
Ruoat, joissa on runsaasti lysiiniä
Lysiini saadaan ruokavalion kulutetusta ruoasta ja keskimääräinen aikuinen ihminen tarvitsee vähintään 0.8 g tätä päivää. Sitä löytyy lukuisista eläinperäisistä proteiineista, etenkin punaisessa lihassa, kuten lehmä, lammas ja kana.
Se on kaloissa, kuten tonnikala ja lohi sekä meren hedelmissä, kuten osterit, katkaravut ja simpukot. Sitä esiintyy myös maitotuotteiden ja niiden johdannaisten aineosissa.
Plant -ruokia löytyy perunoista, paprikoista ja purjoista. Se on myös avokadoissa, persikoissa ja päärynöissä. Palkokasveissa, kuten Arriñonados -pavut, kahviherneet ja soija; kurpitsansiemenissä, makadamian pähkinöissä ja anakardoissa (Merey, Marañón jne.).
Saannisi edut
Tämä aminohappo sisältyy lukuisiin ravitsemuslääkkeisiin, ts. Eristetty luonnollisista yhdisteistä, erityisesti kasveista.
Sitä käytetään kouristuksena ja sen tehokkuutta on myös osoitettu estämässä replikaatiota Herpes simplex -virus Tyyppi 1 (HSV-1), joka yleensä ilmenee stressin hetkinä, kun immuunijärjestelmä on masentunut tai "heikentynyt" ampouleina tai herpesinä huulilla.
L-soittolisäaineiden tehokkuus huulten herpesten käsittelyyn johtuu siitä, että tämä "kilpailee" tai "estää" arginiinia, toinen proteiiniaminohappo, joka on välttämätön HSV-1: n kertomiseksi.
On määritetty, että lysiinillä on myös anti-anti-anti-anti-antic-vaikutuksia, koska se auttaa estämään reseptoreita, jotka osallistuvat vasteisiin erilaisille stressaaville ärsykkeille, sen lisäksi, että osallistuvat kortisolitasojen laskuun "stressihormoni", "stressihormoni".
Jotkut tutkimukset ovat osoittaneet, että se voi olla hyödyllinen muun muassa syöpää aiheuttavien kasvainten estämisessä, silmien terveydelle, verenpaineen hallintaan.
Voi palvella sinua: Kulttuurimedia: Historia, toiminto, tyypit, valmisteluEläimissä
Yleinen strategia herpes I -virusinfektioiden hoitamiseksi kissassa on lysiinilisäys. Jotkut tieteelliset julkaisut kuitenkin osoittavat, että tällä aminohapolla ei ole kissassa, ei viruslääkettä, vaan se toimii pienentämällä arginiinipitoisuutta.
Imeväisten terveydessä
Lasten maidossa lisätty L-Lisinan kokeellinen saanti imetysjaksolla on osoittautunut hyödylliseksi kehon massan hyötyyn ja lasten ruokahalun induktioon synnytyksen jälkeisen kehityksen ensimmäisissä vaiheissa.
L-soiton ylimääräinen ylimääräinen voi kuitenkin aiheuttaa aminohappojen, sekä neutraalien että emäksisten ominaisuuksien liioiteltuja virtsan eritteita, mikä johtaa niiden kehon epätasapainoon.
L-soittolisän ylimääräinen ylimääräinen kasvu voi päättyä kasvun tukahduttamiseen ja muihin histologisiin vaikutuksiin, jotka ovat ilmeisiä tärkeissä elimissä, todennäköisesti johtuen aminohappojen menetyksestä virtsan kanssa.
Samassa tutkimuksessa todistettiin myös, että lysiinilisäys parantaa nauttimisten vihannesproteiinien ravitsemusominaisuuksia.
Muut samanlaiset tutkimukset, jotka tehdään Ghanan, Syyrian ja Bangladeshin molempien sukupuolten aikuisilla ja lapsissa.
Lysiinin puutoshäiriöt
Lysiini on, kuten kaikki välttämättömät ja ei -välttämättömät aminohapot, jotka ovat välttämättömiä soluproteiinien oikealle synteesille, jotka edistävät kehon orgaanisten järjestelmien muodostumista.
Merkittävät lysiinin puutteet ruokavaliossa, koska se on välttämätön aminohappo.
Viitteet
- Kulho, s., & Bunnik, ja. M. (2015). Lysin -rukous ei ole tehokas kissan herpesviruksen 1 tartunnan ehkäisyyn tai hoitoon kissoissa: systemaattinen katsaus. BMC: n eläinlääketieteellinen tutkimus, yksitoista(1).
- Carson, n., Scally, b., Neill, D., & Carré, minä. (1968). Saccharopinuria: Uusi lysiinimetabolian synnynnäinen virhe. Luonto, 218, 679.
- Colina R, J., Díaz e, m., Manzanilla M, L., Araque m, h., Martínez G, G., Rossini V, M., & Jerez-Timaure, N. (2015). Sulavien lysiinitasojen arviointi ruokavalioissa, joilla on suuri energiatiheys sikojen viimeistelyyn. MVZ Córdoba -lehti, kaksikymmentä(2), 4522.
- Fellows, b. F. C. Yllyttää., & Lewis, M. H. R -. (1973). Lysiinin aineenvaihdunta nisäkkäissä. Lehden biokemiallinen, 136, 329-334.
- Fornazier, r. F., Azevedo, r. -Lla., Ferreira, r. R -., & Varisi, V. -Lla. (2003). Lysiinikatabolismi: virtaus, metabolinen rooli ja säätely. Brasilian lehti kasvien fysiologiasta, viisitoista(1), 9-18.
- S, s., Smriga, m., Vuvor, f., Suri, D., Mohammed, H., S. S. M., & Scrimshaw, N. S. (2010). Lysiinin rukouksen vaikutus terveyteen ja sairastuvuuteen accran köyhille kaupunkien kotitalouksille kuuluvilla koehenkilöillä, Ghanassa. American Journal of Clinical Nutrition, 92(4), 928-939.
- Hutton, c. -Lla., Perugini, m. -Lla., & Gerrard, J. -Lla. (2007). Lysiinin biosynteesin estäminen: kehittyvä antibioottistrategia. Molekyyli, 3(7), 458-465.
- Kalogeropoul, D., LAFAVE, L., Schweim, k., Gannon, M. C., & Nuttall, f. Q -. (2009). Lysiinin nauttiminen heikentää huomattavasti glukoosivastetta nautittuun glukoosiin ilman insuliinivasteen muutosta. American Journal of Clinical Nutrition, 90(2), 314-320.
- Nagai, h., & Takeshita, S. (1961). L-lysiinilisän ravitsemuksellinen vaikutus imeväisten ja lasten kasvuun. Japanilainen paediatria, 4(8), 40-46.
- O'Brien, S. (2018). Terveyslinja. Haettu 4. syyskuuta 2019, www.Terveyslinja.com/ravitsemus/lysiini-hyöty
- Zabriskie, T. M., & Jackson, M. D -d. (2000). Lysiinin biosynteesi ja aineenvaihdunta sienissä. Luonnolliset tuoteraportit, 17(1), 85-97.

