Metallit
- 4161
- 1334
- Eddie Hackett
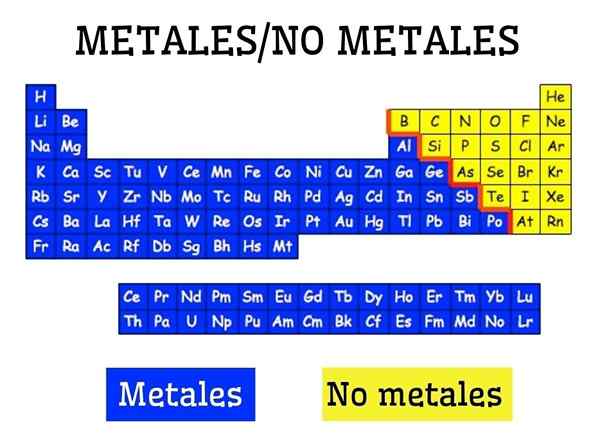
 Metallit ja ei -metallit elementtien jaksollisessa taulukossa
Metallit ja ei -metallit elementtien jaksollisessa taulukossa Mitkä ovat metallit?
Metallit muodostetaan vasemmalla puolella sijaitsevien elementtien ryhmä, lukuun ottamatta jaksollisen taulukon ei -metallista vetyä, lukuun ottamatta. Metallit muodostavat noin 75 % kemiallisista elementeistä, joten voidaan todeta, että suuri osa luonnosta on metallista.
Metallit, jotka ihminen alun perin syytti esihistoriassa, olivat seuraavat: kulta, hopea, kupari, tina, lyijy ja rauta. Tämä johtui siitä, että he olivat kotoperäisiä tai heidän käsittelyn helppoutta suorittaa apuohjelmia.
Vaikuttaa taikuudesta, että monien kivien ja mineraalien voidaan erottaa kiiltävät ja hopeakappaleet (tietyillä tärkeillä ja erinomaisilla poikkeuksilla). Näin on bauksiitti ja alumiini, jonka savikivet tämä metalli vähenee levyissä tai hopeapapereissa.
Metallit ovat toimialojen puitteita; Heidän johdotus, reaktorit, yksiköt, astiat, kaikki jollain tavalla tai toisella koostuvat metalleista ja seoksista.
Metallien kanssa tehtiin ensimmäiset kolikot, aseet, työkalut, panssarit, ja sitten niitä käytettiin ajoneuvojen valmistuksissa, polkupyörissä, aluksissa, lentokoneissa, tietokoneissa muun muassa välttämättömiä esineitä nykyaikaisessa elämässä.
Historia
Kuparikausi
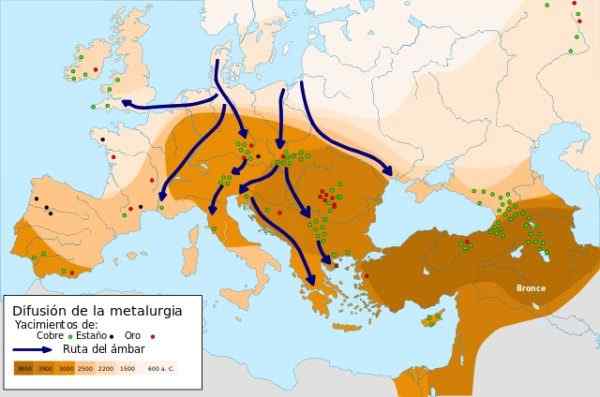 Metallurgian laajennus - Lähde: Metallurginen diffuusio.SVG Creative Commons Attribution-Compartigual 4 Lisenssi 4.0 kansainvälinen
Metallurgian laajennus - Lähde: Metallurginen diffuusio.SVG Creative Commons Attribution-Compartigual 4 Lisenssi 4.0 kansainvälinen Vuonna 9000 a.C. Lähi -idässä taottujen kuparin ensimmäiset metalliesineet kehitettiin, kun mies huomasi, että kuparin iskun jälkeen hän lisäsi vahvuuttaan ja vastustustaan käyttämällä sitä veitsien valmistukseen. Tämä on kuparin ikä.
Havaittiin, että kuparia voitiin saada sinisten mineraalien, kuten Corvellita ja Malachite, lämmittämisen kautta (4000-3000-.C.-A.
Kalsoliittinen ajanjakso on aika, joka edeltää pronssikautta, mikä vastaa 5000-3000.C. Mies alkoi kokeilla kuparin fuusiota ja valimoa, saadakseen kuparioksidista taottuja kuparia.
Pronssikausi (3000-1500 a.C.-A
 Pronssikauden materiaalit - Lähde: Gaguilella Creative Commons Attribution -Shareigual 4 Lisenssi 4.0 kansainvälinen.
Pronssikauden materiaalit - Lähde: Gaguilella Creative Commons Attribution -Shareigual 4 Lisenssi 4.0 kansainvälinen. Mies aloitti vahingossa seosten, alun perin kuparin ja arseenin, laatimisen ja sitten kuparin ja tinan kanssa pronssin saamiseksi Lähi -idässä.
Tätä aikaa vastaavilla pronssiartikkeleilla oli 87 % kuparia, 11 % tinaa ja pieniä määriä rautaa, arseenia, nikkeliä, lyijyä ja antimonia.
Rautakausi (700 a.C.-A
Mies käytti kokemustaan takorautatuotannon tuotannosta takoraudan tuottamiseksi Lähi -idässä. Samana ajanjaksona Erusco -pölyn rakeista oli Italia.
Ensimmäinen tunnettu terästuotanto, rauta- ja hiiliseos, ilmeni metallikappaleiksi arkeologisessa paikassa Anatoliassa (1800.C.-A
Voi palvella sinua: gravimetria: gravimetrinen analyysi, menetelmät, käytöt ja esimerkitKohti 1122 d.C., Tuntemattomalla päivämäärällä ja paikalla valurauta otetaan käyttöön. Vuonna 1440 d.C. Pekingin suuri kello on tuotettu, Kiina. Lähes kolme vuosisataa myöhemmin, vuonna 1709 D.C., Valurauta tuotetaan käyttämällä koksia palavana materiaalina.
Vuonna 1779 valurautaa Englannissa käytettiin arkkitehtonisena materiaalina. Vuonna 1855 Henry Bessenir käytti Arrabioa raaka -aineena pehmeän teräksen saamiseksi. Englantilainen Clark and Wood (1872) patentoi seoksen, jota tällä hetkellä pidetään ruostumattomana teräksessä.
Metallien fysikaaliset ominaisuudet
 Näiden muinaisten kellojen pronssi osoittaa metallien hyödyllisyyden koristeellisiin tai uskonnollisiin tarkoituksiin. Lähde: Pxhere.
Näiden muinaisten kellojen pronssi osoittaa metallien hyödyllisyyden koristeellisiin tai uskonnollisiin tarkoituksiin. Lähde: Pxhere. Joidenkin metallien fysikaalisten ominaisuuksien joukosta meillä on:
-Metallit ovat loistavia ja kykenevät heijastamaan valoa.
-Yleensä ne ovat hyviä sähkön ja lämmön johtimia.
-Heillä on korkea fuusio- ja kiehumispisteet.
-Ne ovat muokattavia, toisin sanoen niitä voidaan vasarata tuottamaan matala paksuja arkkeja.

-Ne ovat sitkeitä, niiden kanssa voit valmistaa johtoja tai kuituja, joiden halkaisija on hyvin vähän.
-Ne esitetään kiinteässä tilassa, lukuun ottamatta elohopeaa, että huoneenlämpötilassa on nestemäisessä tilassa, ja gallium, joka sulaa vain kiristämällä käsissä käsissä. Seuraavassa kuvassa voit nähdä elohopeasäiliön:

-Ne ovat läpinäkymättömiä kappaleita, valo ei ole ohuet arkit.
-Heillä on suuri kovuus, paitsi natrium ja kalium, joka voidaan leikata veitsellä.
-Heillä on korkea tiheys, koska ne ovat korkein osmium ja iridium ja alhaisimman tiheyden litium.
Metallien kemialliset ominaisuudet
Joidenkin metallien kemiallisista ominaisuuksista:
-Heillä on taipumus menettää elektroneja ja muodostavat metallikationeja, mn+, missä N osoittaa sen hapettumisluvun, joka vain alkali- ja emäalistimetallien osuus on samanaikainen sen valenssinumero.
-Sen elektronegativiteetti on alhainen.
-Ne juoksevat ja kokevat hapettumisvaurioita.
-Ne muodostavat emäksisiä oksideja reagoidessaan hapen kanssa. Nämä oksidit yhdistettynä veteen muodostavat metallihydroksideja. Metallioksidit reagoivat happojen kanssa suolojen ja veden muodostamiseksi.
-He ovat hyviä vähentäviä aineita, koska he tuottavat elektroneja.
Metallien tyypit
Metallit luokitellaan seuraavaksi: emäksinen, emäksinen tutkimus.
Alkalimetallit

Ne eivät yleensä ole luonteeltaan vapaana, koska ne hapettuu helposti. Olla suborbitaaliset1 Sen ulkoisessa kiertoradalla, joten heillä on hapettumistila +1. Ne ovat metalleja, jotka reagoivat eksotermisesti veden kanssa ja vähenevät voimakkaasti.
Emäksinen térreos-metallit
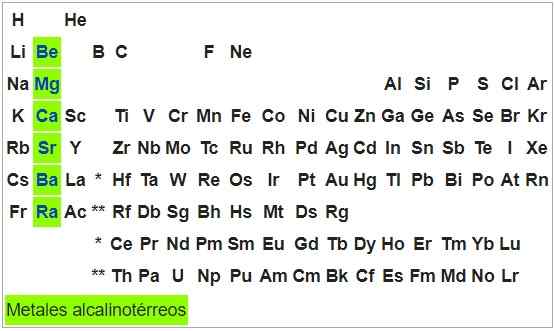
Ne ovat muokattavia ja muovautuvia metalleja. Tämän ryhmän elementtien atomeilla on kokoonpano2, Joten he voivat tuottaa kaksi elektronia ja niiden hapettumistila on +2. Berylliumia lukuun ottamatta ne ovat hapettuvia ilma -altistumiseen.
Voi palvella sinua: hiilialotroopejaSiirron jälkeiset metallit
Ne ovat Metalleja SO -called P -lohkosta, joka sijaitsee siirtymämetallien ja metalloidien välissä jaksollisessa taulukossa.
Ryhmän 3 elementeillä on hapettumisvaltiot +1 ja +3 yleisimmänä, vaikka alumiini esittelee vain hapettumistila +3. Se on myös osa ryhmissä 14 ja 15.
Siirtymämetallit d
Ne muodostavat ryhmän emäksen muotoisten elementtien ja happojen muotoilun välillä. Atomien orbitaalit d ja f ovat puutteellisia ja ne täytetään. Vaikka termi siirtymämetallit viittaavat siirtymämetalleihin d.
Siirtymämetallit ovat enemmän kuin yksi hapettumistila. Heillä on fuusio- ja kiehumispisteitä korkeampi kuin muut metalliryhmät. Siirtymämetallit ovat erittäin heterogeeninen metalliryhmä, joka sisältää muun muassa raudan, kromin, hopean jne.
Harvinainen maa
 Harvinainen maapallon mineraali
Harvinainen maapallon mineraali Tämä metalliryhmä koostuu elementtien scandion ja itititriosta sekä Lantanides- ja Actinids -sarjojen elementeistä. Termi 'harvinainen maametalli' viittaa siihen, että niitä ei löydy luonnossa puhtaissa tiloissa ja että ne kiinnitetään hapolla.
Metallien käyttö/sovellukset
Alkalimetallit
Litiumia käytetään lämmönsiirtovälineinä joissakin ydinreaktorissa. Sitä käytetään joissakin kuivissa paristoissa ja akuttimissa, joilla on vähän painoa. Kloridi ja litiumbromidi ovat hygroskooppisia yhdisteitä, joita käytetään teollisuuskuivaus- ja ilmastointiprosesseissa.
Natriumia käytetään metallimetallurgiassa, kuten titaani ja zirkonium. Sitä käytetään natriumkaarilamppujen julkisessa valaistuksessa. Natriumkloridia (NaCl) käytetään elintarvikkeiden mausta ja lihan säilyttämiseksi.
Alkalinetrimetallit
Valokuvassa käytettiin magnesiumia flash -valoina ja ilotulituksina. Barium on komponentti seoksista, joita käytetään sytytystulpaissa, koska elementti helppo emittoi elektroneja. Bariumsuoloja käytetään rajoittamaan vaurioita, jotka aiheutuvat maha -suolikanavan x -säiliöistä.
Kalsiumia käytetään sulan metallien liuenneiden epäpuhtauksien poistamiseen ja jäännöskaasujen poistamiseen tyhjiöputkissa. Se on osa kipsiä, materiaalia, jota käytetään rakenteessa ja luun murtumien käsittelyssä.
Siirron jälkeiset metallit
Alumiini, koska se on vaalea metalli, jota käytetään lentokoneiden ja alusten rakentamisessa. Sitä käytetään myös lukuisten keittiövälineiden kehittämisessä. Sitä käytetään raaka -aineena hikoilua rajoittavien deodoranttien valmistuksessa.
Voi palvella sinua: ProsenttiosuusratkaisutGalliumia käytetään transistoreissa ja lämpömittarissa korkeissa lämpötiloissa. Isotooppi 67GA: ta käytetään lääketieteessä joidenkin melanoomien hoidossa. Lyijyä käytetään paristojen rakentamisessa ja suojauksessa ionisoivalta säteilystä.
Siirtymäkauden metallit
Kuparia käytetään vesihuoltoputkissa, jääkaapissa ja ilmastointijärjestelmissä. Sitä käytetään myös osana tietokoneita lämmön hajoamismekanismia. Sitä käytetään sähkövirran johtamisessa, sähkömagneetteissa ja lasin värissä.
Nikkeliä käytetään ruostumattoman teräksen kehittämisessä, kitarajonot ja ladattavat akut. Sitä käytetään myös galvanoplastiassa metallisuojauksessa. Sitä käytetään ajoneuvojen osissa olevissa seoksissa, kuten venttiilit, laakerit ja jarrut.
Nikkeliä on käytetty pitkään kolikoiden kehittämisessä.
Sinkkiä käytetään korroosiometallisuojassa, messinkituotannossa. Sinkkioksidia ja sinkkisulfaattia käytetään kattojen, kourujen ja alamäkeissä käytettyjen levyjen valmistuksessa.
Kromia käytetään metallikorroosiosuojauksessa ja tarvikkeet loistavat. Sitä käytetään katalysaattorina ammoniakin synteesireaktiossa (NH3-A. Kromioksidia käytetään puun suojauksessa.
Harvinainen maa
Skandia käytetään alumiinialumiinissa ilmailu-. Se on lisäaine elohopeahöyryvalaisimissa.
Lantanoa käytetään korkean taitekerroksen ja alkalin resistentissä lasissa. Lisäksi sitä käytetään kameroiden linssien valmistuksessa ja katalyyttisenä katalyytinesteinä öljynjalostamoihin.
Cerioa käytetään kemiallisena aineena. Lisäksi sitä käytetään keltaisen lasin ja keraamisen värin tarjontaan sekä katalyyttiä itseopiskelijoille.
Esimerkkejä metallielementeistä
Emäksinen
Natrium (Na), kalium (K), Cesio (CS), litium (Li) ja Rubidium (Ru).
Emäksinen terreot
Beryllium (BE), magnesium (mg), kalsium (CA), strontium (MR), barium (BA) ja radio (RA).
Siirtymäkauden jälkeinen
Alumiini (al), gallium (ga), intialainen (in), talio (tl), tin (sn) ja lyijy (pb).
Siirtymä-
Titanium (TI), Vanadium (V), kromi (CR), mangaani (MN), rauta (usko), koboltti (CO), nikkeli (Ni), kupari (cuinc), sinkki (Zn), zirkonium (ZR), Niobio (NB), molybdeeni (MO), Paladio (PD), hopea (AG), Volframium (W), Renio (RE), Osmio (OS), Iridido (IR),
Platinum (PT), kulta (Au) ja elohopea (HG).
Harvinainen maa
Scandio (SC), Itrio (Y), Lantano (La), Cerio (CE), Praseodimio (PR), neodymium (nd), samarium (SM), Europio (EU), gadolinio (gd), holmio (ho), Erbio (ER), Tulio (TM), Iterbio (YB) ja Luthacio (LU).
Viitteet
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. ed.-A. Cengage -oppiminen.
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Helmestine, Anne Marie, PH.D -d. (5. lokakuuta 2019). Metallit verrattuna ei -metalleihin. Toipunut: Admingco.com
- Metallit ja niiden ominaisuudet-fyysinen ja kemiallinen. [PDF]. Toipunut: csun.Edu
- Jonathan -mestari. (2019). 18 erityyppistä metallia (tosiasiat ja käytöt). Palautettu: MakeitFrommetal.com

