Sommerfeld Atomic Model -ominaisuudet, postulaatit, edut ja haitat
- 1826
- 543
- Joshua Emmerich
Hän Sommerfeld Atom -malli Sen on luonut saksalainen fyysikko Arnold Sommerfeld vuosina 1915–1916 selittääkseen tosiasiat, jotka Bohr -malli, joka julkaistiin vähän ennen vuonna 1913, ei pystynyt tyydyttävästi selittämään. Sommerfeld esitteli tuloksensa ensin Baijerin tiedeakatemialle ja julkaisi ne sitten Annalen Der Physik -lehdessä.
Tanskalaisen fyysikon Niels Bohrin ehdottama atomimalli kuvaa.
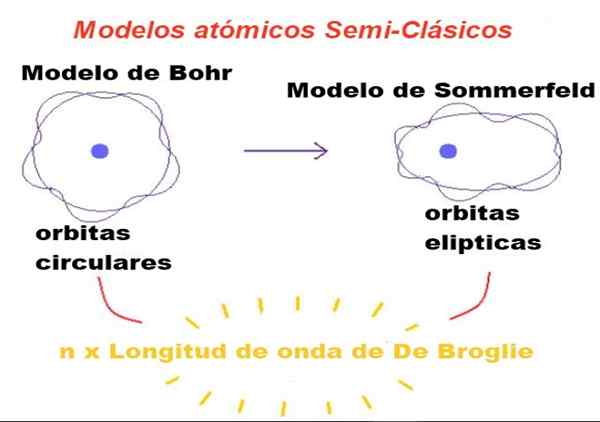
 Kuvio 1. Puoliklassisissa malleissa kiertoradat ovat newtonia, mutta vain ne, joiden kehä on kokonaisluku, kuinka monta kertaa broglie-aallonpituus on sallittu. Lähde: f. Zapata.
Kuvio 1. Puoliklassisissa malleissa kiertoradat ovat newtonia, mutta vain ne, joiden kehä on kokonaisluku, kuinka monta kertaa broglie-aallonpituus on sallittu. Lähde: f. Zapata. Bohrin ehdottamassa teoriassa ytimen ympärillä kiertävällä elektronilla voi olla vain tietyt arvot sen kiertoradan kulmomenkistä, ja siksi se ei voi olla millään kiertoradalla.
Bohr katsoi myös, että nämä kiertoradat olivat pyöreitä ja yksi kvantinumero nimeltään pääkvantinumero n = 1, 2, 3 ... palveli sallittuja kiertoratoja.
Sommerfeldin Bohr -malliin esittämä ensimmäinen modifikaatio koostui olettamisesta, että elektronien kiertorata voi olla myös elliptinen.
Ympäristö kuvataan sen säteen perusteella, mutta ellipsille sinun on annettava kaksi parametria: puoliksi -senije ja vähäinen puoli -semi, saman avaruussuuntauksen lisäksi. Tämän kanssa hän esitteli vielä kaksi kvantinumeroa.
Toinen päämuutos, jonka Sommerfeld teki, oli lisätä relativistisia vaikutuksia atomimalliin. Ei ole mitään nopeampaa kuin valoa, mutta Sommerfeld oli löytänyt elektroneja, joilla oli huomattavasti läheisiä nopeuksia, joten oli tarpeen sisällyttää relativistiset vaikutukset mihin tahansa atomin kuvaukseen.
[TOC]
Sommerfeld -atomimallin postulaatit
Elektronit seuraavat pyöreitä ja elliptisiä kiertoratoja
Atomin elektronit seuraavat elliptistä kiertorata (ympyrä kiertoradat ovat tietty tapaus) ja niiden energiatila voidaan karakterisoida 3 kvanttiluku: pääkvanttiluku n, Toissijainen kvantinumero tai atsimutaalinen numero lens ja magneettinen kvanttiluku mLens.
Voi palvella sinua: binaarisuolatToisin kuin ympärysmitta, ellipsillä on suurempi puoli- ja pieni puoli.
Mutta ellipsit, joilla on sama merkittävä puoli -akseli, niillä voi olla erilainen vähäinen puoli -sekemi, epäkeskeisyyden asteesta riippuen. Epäkeskeisyys, joka on yhtä kuin 0, vastaa ympyrää, joten se ei sulje pois pyöreitä ratoja. Lisäksi avaruudessa ellipseillä voi olla erilaisia taipumuksia.
Siksi Sommerfeld lisäsi malliinsa toissijaisen kvanttiluku L osoittamaan pienen puolikkaan ja magneettisen kvanttiluvun mLens. Siten hän huomautti, mitkä ovat elliptisen kiertoradan sallitut alueelliset suuntaukset.
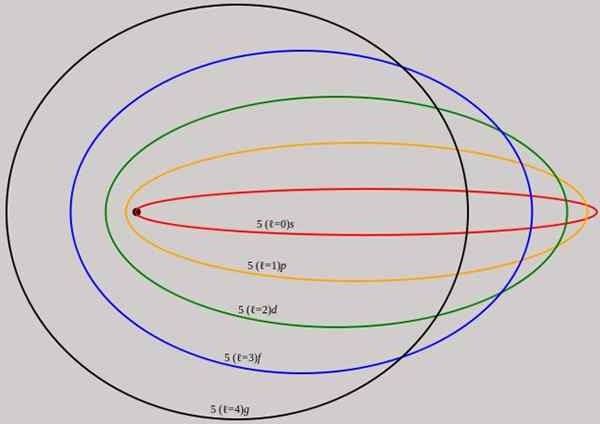 Kuva 2. Energiatasoa n = 5 vastaavat kiertoradat esitetään eri kulman momentin l, joilla on täydelliset aallonpituudet de broglie. Lähde: Wikimedia Commons.
Kuva 2. Energiatasoa n = 5 vastaavat kiertoradat esitetään eri kulman momentin l, joilla on täydelliset aallonpituudet de broglie. Lähde: Wikimedia Commons. Huomaa, että se ei lisää uusia pääkvanttilukuja, joten elliptisellä kiertoradalla olevan elektronin kokonaisenergia on sama kuin Bohr -mallissa. Siksi ei ole uutta energiatasoa, vaan lukumäärän n tasojen avautumista.
Zeeman -vaikutus ja karkea vaikutus
Tällä tavoin on mahdollista määritellä tietty kiertoradalla kokonaan mainittua 3 kvantinumeroa ja selittää siten kahden vaikutuksen olemassaolon: Zeeman -vaikutus ja Stark Effect.
Ja selittää siten normaalin Zeeman -efektissä esiintyvän energian etenemisen (on myös poikkeava Zeeman -vaikutus), jossa spektrin linja on jaettu useisiin komponentteihin, kun se on magneettikentän läsnä ollessa.
Tämä linjojen avaaminen tapahtuu myös sähkökentän läsnä ollessa, joka tunnetaan nimellä Stark Effect, joka johti Sommerfeldin ajattelemaan Bohr -mallin muutosta näiden vaikutusten selittämiseksi.
Atomien ydin ja elektronit liikkuvat sen massakeskuksen ympärillä
Sen jälkeen kun Ernest Rutherford löysi atomien ytimen ja että tosiasia, että melkein koko atomin massa on keskittynyt sinne, tutkijat uskoivat, että ydin oli enemmän tai vähemmän paikallaan olevaa.
Se voi palvella sinua: litiumhydroksidi (LIOH)Sommerfeld kuitenkin postuloi, että sekä ytimet että kiertoradalla olevat elektronit liikkuvat järjestelmän massakeskuksen ympäri, mikä on tietysti hyvin lähellä ydintä. Sen malli käyttää elektronimassan vähentynyttä massaa elektronimassan sijasta.
Elliptisillä kiertoradalla, kuten auringon ympärillä olevien planeettojen kanssa, on aikoja, jolloin elektroni on lähempänä ja muissa kauempana ytimestä. Siksi sen nopeus on erilainen jokaisessa kiertoradan kohdassa.
 Kuva 3.- Arnold Sommerfeld. Lähde: Wikimedia Commons. Gfhund [cc 3: lla.0 (https: // creativecommons.Org/lisenssit/by/3.0)].
Kuva 3.- Arnold Sommerfeld. Lähde: Wikimedia Commons. Gfhund [cc 3: lla.0 (https: // creativecommons.Org/lisenssit/by/3.0)]. Elektronit voivat saavuttaa relativistiset nopeudet
Sommerfeld tuotiin malliinsa hienon rakenteen vakio, vakio ilman sähkömagneettiseen voimaan liittyviä mittoja:
α = 1/137.0359895
Se määritellään elektronikuormituksen väliseksi jakamaan ja I neliön korkea, ja tuote Planckin vakiona h ja valon nopeus c Tyhjiössä kaikki kerrottuna 2π:
α = 2π (E2/h.c) = 1/137.0359895
Hienon rakenteen vakio liittyy kolme atomifysiikan tärkeintä vakio. Toinen on elektronin massa, jota ei tule täällä.
Tällä tavoin se on kytketty elektroneihin fotonien kanssa (jotka liikkuvat nopeudella C tyhjyydessä), ja selitä siten joidenkin ennusteiden vetyatomin joidenkin spektririvien poikkeamat BOHR -mallin avulla.
Relativististen korjausten ansiosta energiatasot ovat yhtä suuret n Mutta erilainen lens Ne erottuvat, mikä johtaa hienon rakenteen rakenteen, sieltä vakion α nimi.
Ja kaikki atomin ominaispituudet voidaan ilmaista tämän vakion suhteen.
 Kuva 4. Kulmaisen momentin l kvantisointi on esitetty. Toisin kuin pyöreät kiertoradat, elliptiset. Lähde: f. Zapata.
Kuva 4. Kulmaisen momentin l kvantisointi on esitetty. Toisin kuin pyöreät kiertoradat, elliptiset. Lähde: f. Zapata. Hyödyt ja haitat
Edut
-Sommerfeld osoitti, että yksi kvanttiluku ei ollut riittävä selittämään vetyatomin spektriviivoja.
-Se oli ensimmäinen malli, joka ehdotti alueellista kvantisointia, koska kiertoratojen projektiot sähkömagneettisen kentän suuntaan on käytännössä kvantisoitu.
Voi palvella sinua: Plasmatila: Ominaisuudet, tyypit ja esimerkit-Sommerfeld -malli selitti tyydyttävästi, että elektronit, joilla on sama pääkvanttiluku n, eroavat energiatilastaan, koska niillä voi olla erilaiset kvantinumerot l ja mLens.
-Esitteli vakion α atomispektrin hienon rakenteen kehittämiseksi ja Zeeman -vaikutuksen selittämiseksi.
-Se sisälsi relativistiset vaikutukset, koska elektronit voivat liikkua nopeuksilla melko lähellä valoa.
Haitat
-Hänen mallinsa oli sovellettavissa vain elektronin atomiin ja monin tavoin alkalimetallien atomeihin, kuten Li2+, Mutta se ei ole hyödyllinen heliumiatomisessa, jossa on kaksi elektronia.
-Ei selittänyt atomin elektronista jakautumista.
-Malli antoi laskea sallittujen tilojen energiat ja tilojen välisissä siirtymissä annettujen tai absorboitujen säteilyn taajuudet antamatta tietoa näiden siirtymien aikoista.
-Nyt tiedetään, että elektronit eivät seuraa etenemissuuntaisia muotoja kiertoradalla, vaan että ne miehittävät Kiertoradat, Avaruusalueet, jotka vastaavat Schrodinger -yhtälöratkaisuja.
-Malli yhdisti mielivaltaisesti klassiset näkökohdat kvanttien näkökohtiin.
-Hän ei selittänyt poikkeavaa Zeeman -vaikutusta, sillä tätä tarvitaan Dirac -malli, joka myöhemmin lisäsi uuden kvantinumeron.
Kiinnostavia artikkeleita
Schrödinger Atomic -malli.
Broglie -atomimalli.
Chadwick Atomic -malli.
Heisenberg Atomic -malli.
Perrin Atomic -malli.
Thomson Atomic -malli.
Dalton Atomic -malli.
Dirac Jordan Atomic -malli.
Leucpo -atomimalli.
Bohr -atomimalli.
Nykyinen atomimalli.
Viitteet
- Brainkart. Sommerfeld Atom -malli ja sen haitat. Toipunut: Brainkart.com.
- Kuinka saimme tietää Cosmos: Light & Matter. Sommerfeldin atomi. Haettu: maistaja.yhteistyö.Yhdistynyt kuningaskunta
- Parker, P. Bohr-Sommerfeld-atomi. Palautettu: Physnet.org
- Koulutuskulma. Sommerfeld -malli. Toipunut.com.
- Wikipedia. Sommerfeld Atom -malli. Palautettu: on.Wikipedia, org.

