Ominaisuudet monosyytit, toiminnot, arvot, sairaudet
- 2645
- 128
- Joshua Emmerich
Se Monosyytit Ne ovat verisoluja, jotka kuuluvat leukosyyttien alaryhmään, nimeltään mononukleaarinen fagosyyttijärjestelmä. Niillä on yhteinen alkuperä muiden fagosyyttien kanssa hematopoieettisissa kantasoluissa. He ovat vastuussa synnynnäisen ja mukautuvan immuniteetin sääntelystä, samoin kuin kudoksen uudelleenmuodostumisesta ja homeostaasista.
Monosyyttien alaryhmiä on kaksi, jotka eroavat toiminnoistaan ja kohteistaan, nimittäin: 1) yksi, joka tuottaa makrofageja perifeerisen verenkierron ekstravasaation jälkeen; 2) toinen, joka tulehduksellisissa olosuhteissa eroaa tulehduksellisissa dendriittisoluissa.
 Lähde: Tohtori Graham-partat [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)]
Lähde: Tohtori Graham-partat [CC BY-SA 3.0 (https: // creativecommons.Org/lisenssit/by-SA/3.0)] Makrofagit ovat fagosyyttisiä soluja, jotka sijaitsevat imusolmukkeessa ja ei -symfoidisessa kudoksessa. He ovat mukana kudoksen homeostaasissa paikallaan olevassa tilassa eliminoimalla apulaiskennot. Lisäksi heillä on laaja valikoima reseptoreita, jotka tunnistavat patogeenit.
Toisaalta dendriittisolut ovat erikoistuneet antigeenien prosessointiin ja esittelyyn sekä B- ja T -solujen vasteen hallintaan.
Infektioiden puolustamisen lisäksi monosyytit voivat vaikuttaa sairauksien, kuten ateroskleroosin ja multippeliskleroosin, tai päinvastoin, ne voivat vaikuttaa lihaksen uudistamiseen vaurioiden jälkeen ja amyloidifibrillien hajoaminen Alzheimerin taudissa.
[TOC]
Ominaisuudet
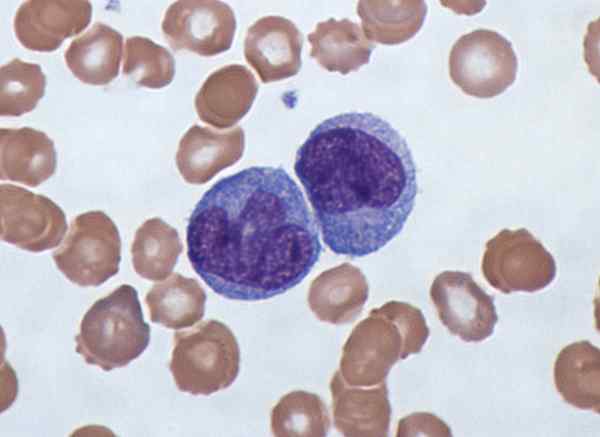
Monosyytit ovat epäsäännöllisiä soluja. Heillä on munuaisten muotoinen ydin. Heillä on vesikkelit sytoplasmassa. Sen halkaisija vaihtelee välillä 16 - 24 um. Kun monosyyttejä on värjätty Wrightin väriaineen kanssa, heidän sytoplasmansa havaitaan sinertävän.
Ne johdetaan luuytimen pluripotenteista kantasoluista. Monosyyttejä tuotetaan useiden vaiheiden ja välitilojen kautta, joihin sisältyy: 1) yleinen myeloidinen vanhempi (CMP); 2) granulosyytti-makrofaginen vanhempi (GMP); 3) MAKROFAGIAPAIKKOT TENDRITISEN VOIMA (MDP).
Heillä on plastisuus, koska niistä voi tulla makrofaageja tai dendriittisoluja. Heistä tulee makrofageja, kun he tulevat kudoksiin tai voivat erottaa itsensä tulehduksellisissa dendriittisoluissa.
Ihmisillä monosyytit muodostavat 8% leukosyyteistä, ja niiden puoli -elämä on 70 tuntia, kun taas hiirillä on 4% leukosyyteistä ja niiden puoli -elämä on 17 tuntia.
Luureseptoreiden ilmentymisen perusteella monosyytit on jaettu kahteen pääryhmään. Ihmisillä nämä ovat: CD14++CD16- ja CD14+CD16+. Hiiressä nämä ovat gr-1Hei ja GR-1LOma.
Monosyyttien kehitys määrää spesifisten transkriptiotekijöiden, kuten PU: n, ilmentyminen.1, ja CCAAT, AML-1B, SP-1, GAT-1 ja -2 siirtymäkertoimet.
Alkuperä ja kehitys
Nykyiset hiirpohjaiset mallit ehdottavat, että monosyytit ovat peräisin hematopoieettisista kantasoluista (HSC, Hamatopoieettiset kantasolut) luuytimestä, jotka kehittyvät kohti granulosyyttimarrofagien muodostumista, muodostaa makrofagipéladle Dendritica (MDP) ja yleisen monosyytin vanhemman (CMOP -A.
Verisuonten luumenissa, paikallaan olevassa tilassa CMOP on ensin eroaa LY6C -soluissaHei, ja sitten LY6C -soluissaMatala. LY6C -solutMatala hiiren (sen ihmisen vastine on CD14MatalaCD16+), heistä tulee verenkiertoja makrofaageja enemmän kuin monosyytit kunnolla, ja ne liikkuvat endoteelin luumen pinnalla.
LY6C -solutMatala Ne koordinoivat stressivastetta luumenissa ja vastaavat vastaanottajan 7 tietullimaisen kautta paikallisten vaurioiden merkkeihin indusoimalla neutrofiilien rekrytointia. Tämä laukaisee endoteelin nekroosin ja siten ly6c -monosyytitMatala Puhdista solujätteet.
LY6C -solutHei hiiren (sen ihmisen vastine on CD14+), edusta "klassisia monosyyttejä". Ne rekrytoidaan tulehduskohtiin, jotka toimivat perifeeristen mononukleaaristen fagosyyttien edeltäjinä. LY6C -solutHei Heillä on tärkeä rooli isäntävasteessa patogeeneihin, kuten Listeria monocytogenes.
Monosyytistä johdetut makrofagit
Termi makrofagi viittaa suuriin fagosyyttisiin munkkisoluihin. Kankaasta riippuen makrofagit saavat tiettyjä nimiä.
Voi palvella sinua: Valkoinen mangrove: Ominaisuudet, elinympäristö, taksonomia, käyttötarkoituksetMakrofageja kutsutaan kupfferisoluiksi maksassa, keuhkojen alveolaariset makrofagit, sidekudoksen histiosyyttit, luun osteoklastit, aivojen mikroglia ja ihon Langerhans -solut. He saavat myös elimen nimen, jossa se sijaitsee, kuten imusolmukkeen, kateenkorvan tai endokriinisen makrofagit.
Vakaan tilan olosuhteissa kudoksissa asuvien makrofagien populaatio ylläpidetään sen paikallisella leviämisellä. Tulehdusten aikana kuitenkin tapahtuu preekursorisolujen nopea rekrytointi vastaavaa kudoksen makrofagiosastoa kohti.
LY6C -monosyyttien erotteluMatala Makrofagus merkitsee muutoksia geenien ilmentymisessä, jotka määrittävät fenotyyppiset muutokset ja makrofagiin liittyvien pinta -antigeenien ilmentyminen. Makrofageja on kahta tyyppiä, nimittäin: M1 -makrofagit tai tulehdukselliset makrofagit; M2 -makrofagit tai anti -inflammatoriset (tai säätelevät) makrofagit.
M1 -makrofagit reagoivat voimakkaasti patogeenien ja muiden haitallisten signaalien tunkeutumiseen muodostamalla tulehdukselliset sytokiinit sekä typpioksidin ja reaktiivisten happilajien synteesi. M2 -makrofageilla on tolerogeenisiä ja palauttavia ominaisuuksia.
Monosyytistä johdetut dendriittisolut
Klassiset dendriittisolut on kehitetty makrofagi-shelule-dendriittisestä (MDP), nimeltään Preclassic Dendriitisolu. Dendriittisolut muodostuvat monosyyteistä, jotka kulkevat endoteelin läpi ablumenal-lumenaaliseen suuntaan. Endoteelimatriisin monosyytit kehitetään makrofageissa.
LY6C -solujen rekrytointiHei Se tapahtuu paikalla, jossa tulehduksia tapahtuu. LY6C -solutHei Rekrytoidaan transformoituna dendriittisoluiksi, jotka muuttuvat imusolmukkeisiin kyhmyihin. Ly6c -monosyytitHei Niistä tulee CX -dendriittisoluja3CR1+D14+. Edellisistä dendriittisoluista tulee CD103+.
Kun ihon tulehdus tuotetaan säteilytyksellä UV -valolla, LY6C -monosyytitHei Orvaskeus saapuvat ja niistä tulee soluja, joilla on Langerhans -soluominaisuuksia. Näitä soluja löytyy yleensä myös emättimen ja suun onteloiden limakalvojen epiteelilinjasta.
Emättimen epiteelidendriittisolut rekonstituoidaan luuytimen esiasteilla. Ly6C -monosyytit asuttavat tulehduksellisissa olosuhteissaHei.
Funktiot
Monosyyttien toiminta infektiossa
Terveissä yksilöissä perifeeriset veren monosyytit koostuvat 90% klassisista monosyyteistä (CD14++CD16++-A. Loput 10% ovat CD16 -monosyyttejä+ (Keskitason CD14++CD16+) ja ei -klassiset monosyytit (CD14+CD16+-A.
Minkä tahansa infektion tai haavan aikana neutrofiilit reagoivat nopeasti (tunteina). Monosyytit kuitenkin moduloivat tulehdusta tuottamalla sytokiineja, kuten IL-1β, IL-6, TNF-α ja typpioksidisyntaasi indusoitava. Jokainen monocitotyyppi reagoi eri tavalla ärsykkeisiin.
Esimerkiksi tartunnan aikana Candida albicans, Klassiset monosyytit indusoivat immuunivasteen Th7. Ollessaan tartunnassa jtk Aspergillus fumigatus, Klassiset monosyytit ja CD16+ Heillä on samanlaiset fagosytoosimahdollisuudet, ja klassiset monosyytit estävät konidian itämistä.
Infektioolosuhteissa CD16 -monosyyttien lukumäärä+ kasvaa. Tätä on havaittu raskaana olevilla malarialla olevilla naisilla (Plasmodium SPP.) ja kolinfekoitu HIV: llä. Monosyytit voivat vähentää loisten lukumäärää, fagosyyttivät tartunnan saaneet punasolut uunien tai ei -opsonilisen fagosytoosin kautta.
Monosyytit voivat kuitenkin vaikuttaa malarian vakaviin ilmenemismuotoihin, mikä vaikuttaa isännän fysiologisiin toimintoihin ja johtaa patologioiden ulkonäköön. Monosyytteillä, dendriittisoluilla ja makrofagisoluilla on myös kriittinen rooli HIV -patogeneesissä.
Voi palvella sinua: osteosyytit: koulutus, ominaisuudet ja toiminnotMonosyyttien toiminta angiogeneesissä ja aterogeneesissä
Monosyytit kerääntyvät kasvavien alusten seinämään kasvavat, mikä viittaa siihen, että ne edistävät aterogeneesiä. Ne eivät muodosta verisuoniverkkoja, vaan jäljittelevät endoteelisoluja, joiden kanssa heillä on fenotyyppiset ominaisuudet ja pintamarkerit.
Kun ääreiskierto -monosyytit siirtyvät verisuonista ekstravaskulaariseen osastoon, ne kypsyvät makrofageihin. Erityisesti M2.
Ateroskleroottisen plakin muodostumisen ominaispiirre on lipoproteiinien kertyminen valtimon intiimille alueelle, johon liittyy monosyyttien rekrytointi verenkierrosta.
Monosyytit siirtyvät subendotelelitilaan ja ovat vuorovaikutuksessa solunulkoisen matriisin komponenttien kanssa, kuten kollageeni I, valtimoiden seinämän pääasiallinen aineosa. Solunulkoisen matriisin ja monosyyttien välillä on vahva vuorovaikutus.
Matala -densiteetti lipoproteiinit (LDL), jotka ovat säilyttäneet solunulkoisen matriisin proteoglukaania, kaappaavat makrofageilla. Metrix -metalloproteiinit (MMP) ovat tärkeitä aterokleroottisen plakin muodostumiselle. Makrofagit ovat vastuussa Uroquinaasin tuottamisesta, joka aktivoi MMP: n.
Monosyyttien toiminta tulehduksessa
Monien tulehduksellisten tilojen, kuten akuutin sydäninfarktin, aivohalvauksen, sepsiksen, sokerin artriitin, HIV: n ja hemodialyysin monosyyttien markkerien alaryhmät. Esimerkiksi potilailla, joilla on sydäninfarkti ja kammion aneurysma.
Monosyytit ja makrofagit ovat tärkein sytokiinien lähde, jotka toimivat solujenvälisinä lähettiläinä, ja säätelevät solujen lisääntymistä, erilaistumista ja migraatiota. Tärkeimmät sydämen vajaatoimintaan osallistuvat sytokiinit ovat kasvaimen nekroositekijä (TNF) ja interleuquina IL6.
Tutkimus sydämen vajaatoimintapotilaiden tulehduksellisista prosesseista osoitti, että TNF, TNFR1 ja TNFR2 ovat kuolleisuuden ennustajia tutkitun populaatiossa. IL6 ei ole tulehduksen merkki, mutta sillä on suora haitallinen vaikutus sydänlihakseen.
Sytokiinijärjestelmän terapeuttinen modulointi kliinisissä tutkimuksissa ei ole onnistunut ihmisillä. Toinen strategia koostuu carvedilolin, ei-selektiivisen beeta-reseptoriantagonistin, käytöstä, joka vähentää TNF: n tuotantoa monosyytteillä.
Fenofibraatti, Phíbric-hapon johdannainen, estää merkittävästi monosyyteistä johdettujen sytokiinien vapautumista, kuten IL1, IL6 ja MCP-1.
Veren monosyyttitasot
Erityyppisten veren leukosyyttien kvantitatiivinen analyysi osoittaa seuraavat normaalit arvot: kaistamuodot (neutrofiilien granulosyytit), 3-5%; Segmentoitu (neutrofiilien granulosyytit), 40-75%; eosinofiilit (granulosyytit), 2-4%; Basofilos (granulosyytit), 0-1%; lymfosyytit, 25-40%; Monosyytit, 2-8%.
Normaali veren monosyyttien lukumäärä on välillä 0 - 800 solua/µL ja normaali keskiarvo on 300 solua/µL (0.3 x 109 solut/l). Krooniset tulehdukselliset prosessit liittyvät monosytoosiin, mikä on monosyyttien lukumäärän kasvu. Absoluuttinen arvo ylittää 800 solua/µL (> 0.8 x 109 solut/l).
Jotkut monosytoosiin liittyvät häiriöt ovat tulehduksellisia sairauksia, kuten tuberkuloosi, syfilis ja ihonalainen bakteerien endokardiitti, granulomatoosi/autoimmuuni, eimatoottinen systeeminen lupus, nivelreuma ja ajallinen tierit.
Monosytoosia tuottavien pahanlaatuisten häiriöiden joukossa ovat leukemia, nolinfosyyttinen leukemia, histiosytoosi, Hodgkinin tauti, ei-Hodgkinin lymfooma ja karsinoomat.
Monosytopenia on monosyyttien lukumäärän väheneminen (alle 200 solua/ µL; 0;.2 x 109 solut/l). Se tapahtuu vasteen stressillä, endotoksemialla ja glukokokokortikoidien, alfa-interferonin ja TNF-Alfa: n antamisen jälkeen.
Jotkut monosytopeniaan liittyvät kauppiaat ovat krooninen lymfosyyttinen leukemia, syklinen neutropenia ja vaikea lämpövaurio.
Liittyvät sairaudet: syöpä
Monosyyttit sen lisäksi, että sillä on tärkeä rooli luontaisessa immuunijärjestelmässä patogeenisten mikrobien isännän puolustamiseksi, osallistuvat myös taudin patogeneesiin ja sairauksien, kuten ateroskleroosin, multippeliskleroosin ja kasvaimen metastaasien etenemiseen.
Voi palvella sinua: mikä on ovocell? (Eläimissä ja kasveissa)M1 -tulehdukselliset makrofagit osallistuvat tarpeettomien kasvainsolujen eliminointiin, mutta kasvaimen (TAM) M2: een liittyvät makrofagit voivat estää kasvaimen vastaista vastetta, lisäämällä kasvaimen kasvua ja edistävää metastaasia.
Tämän vuoksi TAM: n läsnäolo ja määrä korreloivat potilaan huonon elinajanodotuksen kanssa. Hiirillä, joihin perna on poistettu.
Kasvaimen hypoksia -ympäristössä TAM: iin vaikuttaa voimakkaasti signaalimolekyylien, immuunijärjestelmän solujen ja kasvainsolujen eritys. Invasiivinen TAM tuottaa kasvutekijöitä, kuten EGF, jotka edistävät kasvaimen kasvua.
Lisäksi TAM tuottaa tekijöitä, kuten VEGF, joka edistää verisuonten ja etäpesäkkeiden kasvua. Toinen TAM: n tuottama tekijä on VEGFR1, joka osallistuu PRETMEASTásic -markkinaraon muodostumiseen.
Viitteet
- Abbas, a. K -k -., Lichtman, a. H., Pillai, s. 2017. Immunologia solu ja molekyyli. Elsevier, Amsterdam.
- Auffray, c., Sieweke, M. H., Geissmann, f. 1009. Verimonosyytit: kehitys, heterogeenisyys ja suhde dendriittisoluihin. Immunologian vuosikatsaus, 27, 669-92.
- Deves, P. J -., Martin, S. J -., Burton, D. R -., Roitt, i. M. 2017. Roittin välttämätön immunologia. Wiley, Chichester.
- Eales, L.-J -. 2003. Immunologia elämän tutkijoille. Wiley, Chichester.
- Fraser, minä. P., Ezekowitz, a. B -. 2001. Monosyytit ja makrofagit. Julkaisussa: Austen, k. F., Frank, m. M., Atkinson, J. P., Heht., toim. Samterin immunologiset sairaudet, osa I. Lippinott Williams & Wilkins Publishers.
- Geissmann, f., Manz, m. G., Jung, S., Sieweke, M. H., Merad, m, laki, k. 2010. Monosyyttien, makrofagien ja dendriittisolujen kehitys. Science, 327, 656-661.
- Hoffman, R., Benz, e. J -., Jr., Silberstein, L. JA., Heslop, h., Weitz, J. Yllyttää., Anastasi, J., Salama, m. JA., Abutalib, s. -Lla. 2017. Hematologia: Perusperiaatteet ja käytännöt. Elsevier, Amsterdam.
- Karlmark, k. R -., Tacke, f., Dunay, minä. R -. 2012. Monosyytit terveydessä ja sairauksissa - Mini -katsaus. European Journal of Microbiology and Immunology 2, 97-102.
- Lameijer, m. -Lla., Tang, J., Nahrendorf, M., Beelen, r. H. J -., Mulder, W. J -. M. 2013. Monosyytit ja makrofagit nanolääketieteellisinä kohteina sairauden diagnoosin ja hoidon parantamiseksi. Asiantuntijakatsaukset molekyylidiagnostiikassa, 13, 567-580.
- Lameijer, m., Tang, J., Nahrendorf, M., Mulder, W. J -. M. 2013. Monosyytit ja makrofagit nanolääketieteellisinä kohteina sairauden diagnoosin ja hoidon parantamiseksi. Diagnostinen molekyylikatsaus, 13, 567-580.
- Lasarus, H. M., Schmaier, a. H. 2019. Hematologian tiivis opas. Springer, Cham.
- Lichtman, m. -Lla., Kaushansky, k., Prchal, J. T., Levi, m. M., Palovamma, l. J -., Armitage, j. JOMPIKUMPI. 2017. Hematologian käsikirja. MC Graw Hill, New York.
- Löffler, H., Rastetter, J., Haferlach, t. 2000. Kliinisen hematologian atlas. Springer, Berliini.
- Longo, D. Lens. 2010. Harrisonin hematologia ja onkologia. McGraw-Hill, New York.
- Murphy, k., Kutoja, c. 2016. Janewayn immunobiologia. Garland Science, New York.
- Østerud, b., Bjørklid, E. 2003. Monosyyttien rooli athelegogeneesissä. Physiology Review, 83, 1069-1112.
- Parham, P. 2014. Immuunijärjestelmä. Garland Science, New York.
- Paul, W. JA. 2012. Perustavanlaatuinen immunologia. Lippinott Williams & Wilkins, Philadelphia.
- Richards, D. M., Hettinger, j., Feuerer, m. 2013. Monosyytit ja makrofagit syövässä: kehitys ja toiminta. Mikroympäristösyöpä, 6, 179-191.
- Wrigley, b. J -., Huuli, g. JA. Lens., ShantLa, E. 2011. Monosyyttien ja tulehduksen rooli sydämen vajaatoiminnan patofysiologiassa. European Journal of Heart Wanding, 13, 1161-1171.
- Yona, S., Jung, S. 2009. Monosyytit: osajoukot, alkuperä, kohtalot ja toiminnot. Nykyinen mielipide hematologiassa. Doi: 10.1097/moh.0B013E3283324F80.
- « Basofiilien ominaisuudet, morfologia, toiminnot, sairaudet
- Helichrysum Stoechas -ominaisuudet, elinympäristö, ominaisuudet, hoito »

