Pencanona -kemiallinen rakenne, ominaisuudet, synteesi, käyttää
- 3469
- 997
- Eddie Hackett
Se Pentanona Se on orgaaninen yhdiste, joka kuuluu ketonien perheeseen, jonka kemiallinen kaava on C5H10JOMPIKUMPI. Se on edelleen yksi yksinkertaisimmista ketoneista ja koostuu värittömästä nesteestä, jonka aromi on samanlainen kuin asetonin,. Siitä lähtien siitä lähtien, suhteessa luurankojen hiilimäärään, ketonit esittävät isomeerin.
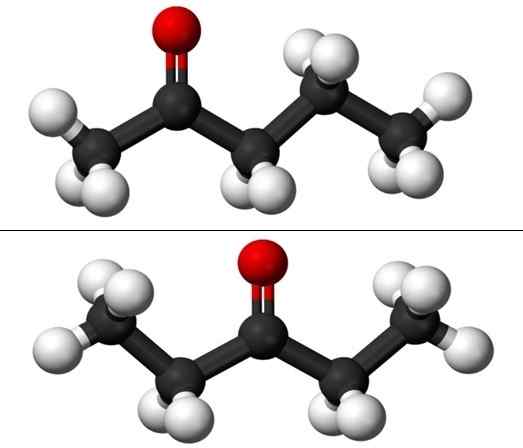
Kun puhut asemasta, isomeria viittaa siihen, missä karbonyyliryhmä on, c = o. Siten Puntanona koostuu tosiasiallisesti kahdesta yhdisteestä, joilla on fysikaaliset ominaisuudet, jotka eroavat tuskin toisistaan: 2-penoni ja 3-penoni (alempi kuva). Molemmat ovat nestemäisiä, mutta niiden kiehumispisteet ovat samat, joten niitä ei voida erottaa tislaamalla.
 Pentanonan aseman isomeerien molekyylit. Lähde: Jynto & Ben Mills Wikipedian kautta.
Pentanonan aseman isomeerien molekyylit. Lähde: Jynto & Ben Mills Wikipedian kautta. Kummallakin kahdella pentanonilla on kuitenkin oma synteesireiti, joten on epätodennäköistä, että niistä on sekoitus; seos, joka voi olla mahdollista erottaa jäädyttämällä.
Sen käyttö on rajoitettu etenkin orgaanisina liuottimina; Vaihtoehtoja asetonille mediassa, jossa työskentelet lämpötilan kanssa korkeammalla kuin sen alhainen kiehumispiste. Ne ovat myös aloitusmateriaaleja muille orgaanisille synteesille, koska niiden ryhmä C = O voi vähentää tai kärsiä nukleofiilistä lisäystä.
[TOC]
Kemiallinen rakenne
Sijainti isomeerit
Kuvassa meillä on Puntanonan kahden aseman isomeerin molekyylirakenteet, joita edustaa malli pallo- ja palkkien malli. Mustat pallot vastaavat hiilihapotettuja luurankoja, valkoisia vetyatomeja ja punaisia happiatomeja ryhmässä C = O.
2-pintanoni
2-ponanonassa (yllä) on ryhmä C = tai toisessa hiilessä, joka vastaa, jos se olisi huoneessa; toisin sanoen 2-ponanona ja 4-pantanona ovat vastaavia, koska se riittää kiertämään niitä 180º: ta niin, että niiden rakenteet ovat samat.
Voi palvella sinua: hiilitetrakloridi (CCL4)Vasemmalla puolella c = o sinulla on metyyliradikaali, CHO3-, Ja hänen oikealla puolellaan radikaali potkuri. Siksi tämä Cetona vastaanottaa myös nimen (vähemmän käytetty) Metil Propil Cetona (MPK englanniksi). Voit nähdä tämän rakenteen epäsymmetrian ensi silmäyksellä.
3-penoni
3-Péntanona (alla) on ryhmä C = O kolmannessa hiilessä. Huomaa, että tämä isomeeri on suurempi versio asetonista ja että se on myös erittäin symmetrinen; Kaksi radikaalia ryhmän c = O sivuilla ovat samat: kaksi etyyliradikaalia, ch3CH2-. Siksi 3-pananonaa kutsutaan myös cetona diestiliksi (tai dimetyyliasetoniksi).
Molekyylien väliset vuorovaikutukset
Karbonyyliryhmän läsnäolo, sekä 2-pantaanissa että 3-penonassa, antaa polaarisuuden molekyylille.
Siksi molemmat Pentanona-isomeerit kykenevät vuorovaikutukseen toistensa kanssa dipolin dipolin kautta.
Samoin Lontoon dispersiovoimat hiilen ja hydrattujen luurankojen välillä puuttuvat vähemmässä määrin.
Puntanonalla, suurempi molekyylipinta -ala ja massa verrattuna asetoniin, tämä panos lisää dipolimomenttiin ja sallii suuremman kiehumispisteen (102 ºC> 56 ºC) korkeamman kiehumispisteen hallussapidon). Itse asiassa kaksi isomeeriä höyrystyy 102 ºC: n nopeudella; Vaikka ne jäätyvät eri lämpötiloissa.
Kiteet
Luultavasti kiteytymisessä symmetriat ovat tärkeä rooli. Esimerkiksi 2 -pantanonan fuusiopiste on -78 ºC, kun taas 3 -péntanona, -39 ºC.
Voi palvella sinua: Avogadro -lakiTämä tarkoittaa, että 3-pantanona-kiteet ovat vakaampia lämpötilaa vastaan; Sen molekyylit ovat yhtenäisempiä ja vaativat enemmän lämpöä erottua nestefaasissa.
Jos molemmista isomeereistä olisi seos, 3-penoni olisi ensimmäinen, joka kiteytyy, lopulta 2-pananona alhaisemmassa lämpötilassa. 3-pantaanin molekyylit, symmetrisempi, suuntautuvat helpommin kuin 2-ponanonan: epäsymmetrinen ja samalla dynaamisempi.
Ominaisuudet
Fyysinen ulkonäkö
Värittömät nesteet, joiden aromi on samanlainen kuin asetonin.
Moolimassa
86,13 g/mol
Tiheys
0,81 g/ml (3-ponanona)
0,809 g/ml (2-ponanona)
Sulamispiste
-78 ºC (2-ponanona)
-39 ºC (3-Ponanona)
Kiehumispiste
102 ºC (molemmille isomeereille)
Vesiliukoisuus
35 g/l (3-ponenona)
60 g/l (2-ponenona)
Höyrynpaine
35 mmHg (3-ponenona)
270 mmHg (2-pantaani) 20 ºC: n lämpötilassa
Nämä arvot eivät ole hyödyllisiä vertailemaan suoraan molempien isomeerien höyrypainetta, koska ensimmäinen ilmoitetaan ilman lämpötilaa, jolla se mitattiin.
Leimahduspiste
12,78 ºC (3-Ponanona)
10 ºC (2-Ponanona)
Vakaus
Kaksi Pentanona -isomeeriä ovat erittäin syttyviä, joten niiden on pysyttävä niin kaukana mistä tahansa lämmönlähteestä. Flash -pisteet osoittavat, että liekki voi asettaa molempien pentanojen höyryt jopa 10 ºC: n lämpötilassa.
Synteesi
Vaikka kaksi Pentanona -isomeeriä ovat fyysisesti ja kemiallisesti hyvin samankaltaisia, niiden synteettiset reitit ovat toisistaan riippumattomia, joten on epätodennäköistä, että molemmat saadaan samassa synteesissä.
2-pintanoni
Alkaen 2-penolireagenssista, sekundaarisesta alkoholista, tämä voidaan hapettaa 2-ponanoniksi käyttämällä hypokloorihappoa, joka on muodostettu in situ, HCLO, hapettumisaineena. Hapetus olisi:
Se voi palvella sinua: Ei elektrolyyttejä: ominaisuudet ja esimerkit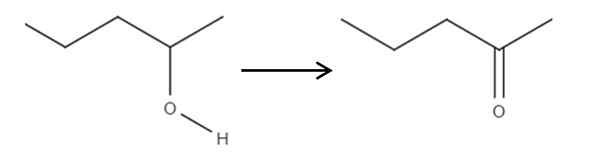 2-pantanolin hapettuminen 2-pantanonalla. Lähde: Gabriel Bolívar.
2-pantanolin hapettuminen 2-pantanonalla. Lähde: Gabriel Bolívar. Yksinkertaisesti C-OH-linkistä tulee c = o. 2-penonan syntetisoimiseksi on muitakin menetelmiä, mutta tämä on yksinkertaisin ymmärtää.
3-penoni
3-pintanoni voidaan syntetisoida keinoin3CH2Haittaa. Tämä synteettinen reitti tuottaa symmetrisiä ketoneja, ja se on CHO -molekyyli3COOH menettää COOH -ryhmän CO: n muodossa2, Kun taas toinen ryhmäsi oi h: n muodossa2JOMPIKUMPI:
2CH3CH2Cooh => ch3CH2Kokki2CH3 + Yhteistyö2 + H2JOMPIKUMPI
Toinen hiukan monimutkaisempi reitti on reagoida suoraan eteenin seos, Cho2= Ch2, Yhteistyö2 ja h2 3-ponanonan muodostamiseksi.
Sovellukset
Ellei sovellus ole erittäin tiukka, se on erityinen synteesi tai että on myös osoitettu, että kaksi isomeeriä eivät aiheuta samoja tuloksia, ei ole merkitystä valita 2-penonin tai 3-penonin käytön välillä missä tahansa sen sisällä käyttötarkoitukset.
Eli "sillä ei ole merkitystä", jos haluat käyttää 2-ponanonaa tai 3-penonaa maalausten tai hartsien liuottimena tai kurjaksi, koska tärkeimmistä kriteereistä tulee sen hinta ja saatavuus. Autoteollisuudessa käytetään 3-penonia tutkimaan kaasujen käyttäytymistä polttomoottoreiden sisällä.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. Amiini. (10. painos.-A. Wiley Plus.
- Wikipedia. (2019). 3-pain. Haettu: vuonna.Wikipedia.org
- Kansallinen bioteknologiatietojen keskus. (2019). 2-pontenoni. Pubchem -tietokanta. CID = 7895. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Kuninkaallinen kemian yhdistys. (2019). 3-pain. Toipunut: Chemspider.com
- Professori T. Nalli. (2013). 2-pintanolin hapettuminen ja tuotteen tislaus. Toipunut: kurssi1.Winona.Edu

