Vastaava paino
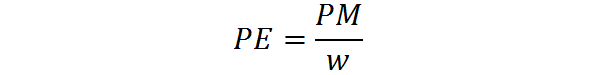
- 2620
- 153
- Gustavo Runte DVM
Mikä on vastaava paino?
Hän vastaava paino Se on aineen ekvivalentin paino tai massa. Toisin sanoen, aineen paino tai massa on kemiallisesti yhtä suuri kuin yksi mooli toisen tyyppisen aineen kanssa, jota käytetään vertailukinteenä ja sitä pidetään normaalina.
Referenssinä otettu normaali aine riippuu kyseessä olevan kemiallisen reaktion tyypistä ja yhdisteen roolista siinä reaktiossa. Normaalit yhdisteet reagoivat aina keskenään stökiometrialla 1: 1.
Esimerkiksi, jos puhumme happo/emäsreaktiosta, hapon ekvivalenttipaino olisi mainitun yhdisteen paino, joka vastaa yhtä moolia normaalia happoa, jolla on yksi ionisoitava protoni.
Ennen tiedettiin, että aine muodostui atomilla ja molekyyleillä, sarja lakeja, jotka määrittivät kemiallisen reaktion reagenssien ja tuotteiden välisen massasuhteen (tai painon), oli jo muodostettu.
Nämä lait muodostivat stökiometristen laskelmien perustan kemian alussa tieteenä.
Vastaava painokonsepti liittyy tähän kemian kehityksen varhaiseen vaiheeseen. Seuraavaksi keskustelemme siitä, miten se lasketaan, mihin se on tarkoitettu ja joitain yleisiä esimerkkejä laskelmastasi.
Kaava ja vastaavat painoyksiköt
Vastaava paino lasketaan yhden aineen molekyylipainosta seuraavan kaavan avulla:
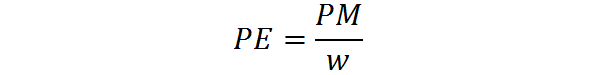
Missä PE on vastaava paino, PM on aineen molekyylipaino tai molaarinen massa ja W - edustaa ekvivalenttien lukumäärää molia kohti.
Jälkimmäinen koostuu aina kokonaisluvusta, joka on yhtä tai suurempi kuin 1. Se edustaa ”normaalin” reagenssin molekyylien lukumäärää, johon kukin ainemolekyyli on ekvivalentti. Siksi se riippuu kyseessä olevan reagenssin tyypistä ja siihen liittyvän kemiallisen reaktion tyypistä.
Voi palvella sinua: dihydroksiasetoni: rakenne, ominaisuudet, hankkiminen, käyttöSe voidaan myös laskea taikinasta M ja vastaavan lukumäärästä:
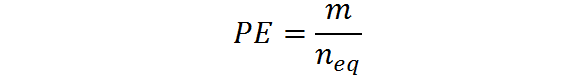
Vastaavat painoyksiköt
Kuten edellisestä kaavasta voidaan nähdä, vastaava paino ilmaistaan massayksiköissä (yleensä grammissa) vastaavien lukumäärässä. Eli yksiköt ovat g/eq.
Arvo W - Ensimmäisessä edellisessä kaavassa se ekspressoituu ekvivalentteina yksiköissä moolilla (ekvivalentti/mol), kun taas molaarimassa ekspressoituu grammina molin (g/mol) yli (g/mol).
Mikä on vastaava paino?
Vastaavan painon tärkein hyödyllisyys on, että se yksinkertaistaa stökiometrisiä laskelmia. Aineen ekvivalenttipaino vastaa saman tyyppistä ainetta ja samanlaista kemiallista reaktiota. Itse asiassa sieltä hän saa nimensä.
Tämän avulla voimme suorittaa stökiömetrisiä laskelmia hyvin yksinkertaisella tavalla ja ilman tarvetta kirjoittaa ja tasapainottaa kemiallisia yhtälöitä.
Kuinka vastaava paino lasketaan?
Kuten aiemmin näimme, vastaava paino lasketaan molekyylipainosta ja ekvivalenttien lukumäärästä molia tai w.
Molekyylipainon laskenta
Aineen molekyylipaino määritetään lisäämällä kaikkien atomien atomipaino. Nämä atomipainot löytyvät jaksollisesta taulukosta.
Päättäväisyys jstk W -
Arvo W - Aineelle se riippuu reaktiotyypistä, johon se on. Eli se riippuu kyseisen reagenssin tyypistä. Jokaiselle ainetyypille on erilainen tapa määrittää W -.
Seuraava taulukko näyttää kuinka se määritetään W - Eri tapauksissa.
Se voi palvella sinua: kalsiumhypokloriitti (CA (CLO) 2)| Reagenssin tyyppi | Jonkin arvo W - |
| Hapot | Ionisoitavissa olevien hydrogeneiden lukumäärä jokaiselle happamolekyylille. |
| Pohjat | Protonien lukumäärä, jotka voivat kaapata tai neutraloida jokaisen emäsmolekyylin. |
| Hapettavia aineita | Elektronien lukumäärä, joka vangitsee kukin hapettavan aineen mool. |
| Vähentävät edustajat | Elektronien lukumäärä vapautti kukin moolia pelkistävästä aineesta hapettumisessa puoliksi. |
| Menet ulos | Positiivisten tai negatiivisten varausten kokonaismäärä, jotka syntyy, kun yksi suolasta. |
| Neutraalit aineet | 1 |
On huomattava, että jos aine voi osallistua useampaan kuin yhteen kemialliseen reaktiotyyppiin, sillä voi olla useampi kuin yksi arvo W - Ja siksi useampi kuin yksi vastaava paino.
Vastaavan painon merkitys ja sovellukset
Vastaavaa painoa käytetään kemikaalin ekvivalenttien lukumäärän laskemiseen. Tämä ekvivalenttien lukumäärä on aina yhtä suuri kuin toisen aineen ekvivalenttien lukumäärä, jolla se reagoi.
Tätä käytetään pääasiassa kahdella eri alueella:
Analyyttisessä kemiassa
Equivalentteja käytetään usein stökiometristen laskelmien helpottamiseen analyyttisessä kemiassa. Tämä pätee erityisesti tilavuus- ja gravimetrisen analyysin tapauksessa.
Tieto asteen tilavuudesta ekvivalenssipisteessä ja nimellisen pitoisuutena sekä oikeuden vastaava paino sallii helposti laskea näytteessä olevan analyytin massan.
Elektrolyysissä
Elektrolyysikentällä vastaava paino edustaa yhden metallin tai muun aineen painoa, joka voi tapahtua, kun 96.500 ° C Lataus elektrolyyttisen solun läpi. Tämä helpottaa elektrolyysiprosessin stökiometrisiä ja taloudellisia laskelmia.
Voi palvella sinua: Elohopeaoksidi (HG2O)Esimerkkejä vastaavasta painolaskelmasta
Kalsium
Kalsiumin atomipaino on 40 ja tämä metalli muodostaa kationeja Valencia +2: lla, joten sen vastaava paino on 40/2 = 20 g/eq.
Rikkihappo (H2Sw4-A
Tämän yhdisteen molekyylipaino on 98 ja on diproottinen happo, niin W = 2. Siksi vastaava paino on PE: 98/2 = 49 g/eq.
Alumiinihydroksidi (Al (OH)3-A
Alumiinihydroksidi (PM = 78) on amfoottoriyhdiste, joka voi toimia happona ja emäksenä.
Jos käytät pohjana vapauttamalla kolme hydroksidiasi, niin niin W = 3, Joten PE: 78/3 = 26 g/Eq. Toisaalta, kun se toimii happona, se vangitsee vesimolekyylin ja vapauttaa protonin, joten tässä tapauksessa tässä tapauksessa, W = 1 ja PE = 78 g/Eq.
Kalsiumfosfaatti (CA3(PO4-A2-A
Kalsiumfosfaatti on suola, joka dissosioituessa tuottaa 3 ca -ionia2+ ja 2 ionia PO43-.
Joka tapauksessa saman merkin kuormien lukumäärä, jonka kukin kalsiumfosfaattiyksikkö tuottaa, on 6, joten W = 6 ja PE = 310/6 = 51,67 g/eq.
Viitteet
- Universal Encyclopedia (S. F.-A. Vastaava paino. Otettu tietosanakirjasta_universal.ES-akateeminen.com.
- Kemia, epäorgaaninen kemia (S. F.-A. Vastaava paino. Otettu Fullquimicasta.com.
- Kemia.Se on (s. F.-A. Vastaava. Kemiasta.On.
- Spiegato (2021). Mikä on vastaava paino? Otettu Spiegatosta.com.

