Muskariinireseptoreiden rakenne, tyypit ja niiden toiminnot, antagonistit
- 2239
- 226
- Eddie Hackett
Se muskariinireseptorit Ne ovat molekyylejä, jotka välittävät asetyylikoliinia (ACH) ja sijaitsevat synapsien postsynaptisessa kalvossa, jossa mainittu välittäjäaine vapautuu; Hänen nimensä tulee hänen herkkyydestään sienen tuottamaan muskariinialkaloidiin Amanita Muscaria.
Keskushermostossa on useita hermosolujen sarjoja, joiden aksonit vapauttavat asetyylikoliinia. Jotkut heistä päättyvät aivoihin, kun taas suurin osa muodostavat luurankojen lihaksen moottorit tai autonomisen hermoston efektorireitit rauhasten ja sydämen ja sileiden lihaksille.
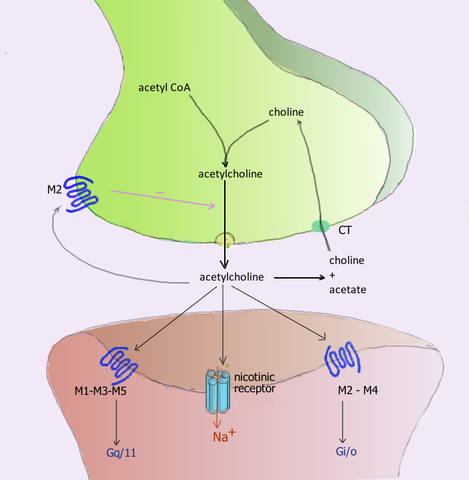
 Asetyylikoliinin neuroreseptori synapsin aikana ja niiden vastaavat reseptorit postsynaptisessa kalvossa (lähde: Käyttäjä: Pancrat [GFDL 1.2 (http: // www.GNU.Org/lisenssit/vanhojen lisenssit/FDL-1.2.HTML)] Wikimedia Commonsin kautta)
Asetyylikoliinin neuroreseptori synapsin aikana ja niiden vastaavat reseptorit postsynaptisessa kalvossa (lähde: Käyttäjä: Pancrat [GFDL 1.2 (http: // www.GNU.Org/lisenssit/vanhojen lisenssit/FDL-1.2.HTML)] Wikimedia Commonsin kautta) Aktiivisten luurankojen kolinergisten reseptoreiden neuromuskulaarisissa ammattiliittoissa vapautuneen asetyylikoliini, jota kutsutaan nikotiiniksi, sen herkkyyden nikotiinialkaloidille ja joita esiintyy myös autonomisen hermoston (SNA) synapsissa.
Tämän järjestelmän parasympaattisen jakautumisen postganglioniset neuronit käyttävät toimintojaan vapauttamalla asetyylikoliinia, joka vaikuttaa efektorisolujen kalvoissa sijaitseviin muskariinisiin kolinergisiin reseptoreihin ja indusoimalla niitä sähköisiä modifikaatioita läpäisevyyden muutoksella ionisissa kanavissa.
 Asetyylikoliinin välittäjäaineen kemiallinen rakenne (lähde: Neurotokeker [julkinen alue] Wikimedia Commonsin kautta) [TOC]
Asetyylikoliinin välittäjäaineen kemiallinen rakenne (lähde: Neurotokeker [julkinen alue] Wikimedia Commonsin kautta) [TOC]
Rakenne
Muskariinireseptorit kuuluvat metabotrooppisten reseptorien perheeseen, termillä, jolla ne reseptorit, jotka eivät ole oikein ionisia kanavia.
Termiä käytetään erottamaan ne ionotrooppisista reseptoreista, jotka ovat todellisia ionikanavia, jotka avautuvat tai lähellä välittäjäaineen suoraa vaikutusta, kuten myös nikotiinireseptorit, jotka ovat jo nimettyjä luurankojen lihaksen neuromuskulaarisia plakkeja.
Metabotrooppisten reseptoreiden sisällä muscarinics sisältyy ryhmään, joka tunnetaan nimellä Grozed G, ne aktivoivat fosfolipaasi C (PLC).
Muskariinireseptorit ovat pitkiä kattavia membraaniproteiineja; Heillä on seitsemän alfa -taipumusta koostuneen transmarket -segmenttiä, jotka ylittävät peräkkäin lipidikalvojen kaksikerroksiset. Sisällä, sytoplasmisissa kasvoissa, ne liittyvät vastaavaan G-proteiiniin, joka siirtyy ligandin vastaanottimen vuorovaikutukseen.
Se voi palvella sinua: Embrioblastit: kehitys, toiminnot ja kerroksetTyypit muskariinireseptorit ja niiden toiminnot
Ainakin viisi tyyppiä muskariinireseptoreita, jotka on nimetty käyttämällä kirjainta M: n, jota seuraa lukumäärä, on tunnistettu, nimittäin: M1, M2, M3, M4 ja M5.
M1-, M3- ja M5 -reseptorit muodostavat M1.
- M1 -reseptorit
Niitä löytyy pääasiassa keskushermostosta, eksokriinisistä rauhasista ja Nodon Autonomic System Gangliasta. Ne on kytketty GQ -proteiiniin, joka aktivoi fosfolipaasi C -entsyymin, joka muuntaa fosfatidyyli -inositoliksi (PIP2) inositoli -tryposfaatiksi (IP3), joka vapauttaa solunsisäistä ja diasilglyserolia (DAG), joka aktivoi proteiineja C C: n.
- M2 -reseptorit
Niitä löytyy pohjimmiltaan sydämessä, pääasiassa sinourikulaarisen solmun soluissa, joihin ne toimivat vähentämällä niiden purkaustiheyttä, kuten alla on kuvattu.
Sydämen automatismi
M2 -reseptoreita on tutkittu perusteellisemmin sydämen nodoaurikulaarisessa solmussa (SA), jossa automatismi, joka tuottaa säännöllisesti sydämen mekaanisesta aktiivisuudesta vastaavat rytmiset viritykset, ilmenee normaalisti.
Sinouricular -solmun solut, kun jokainen toimintapotentiaali (PA) laukaisee sydämen systoolin (supistuminen), repolarisoidaan ja palautetaan noin -70 mV: n tasolle noin -70 mV. Mutta jännite ei pysy siinä arvossa, vaan kärsii progressiivisesta depolarisaatiosta kynnystasolle, joka laukaisee uuden toimintapotentiaalin.
Tämä progressiivinen depolarisaatio johtuu spontaaneista muutoksista ionisten virtojen (i) spontaanista muutoksista, jotka sisältävät: K+ (IK1) lähtövähennys, Na+: n (FI) merkintävirran ulkonäkö ja sitten CA ++ (ICAT) merkintä, kunnes se saavuttaa kynnyksen ja toinen CA ++ (ical) -virta, joka vastaa toimintapotentiaalista.
Jos K+: n (IK1) lähtö on erittäin alhainen ja Na+ (If) ja Ca ++ (ICAT) sisääntulovirrat ovat korkeat, depolarisaatio tapahtuu nopeammin, toimintapotentiaali ja supistuminen tapahtuu aikaisemmin, ja taajuus sydämen on korkeampi. Näiden virtojen vastakkaiset muutokset pienemmällä taajuudella.
Voi palvella sinua: karioklesisNorepinefriinin (sympaattinen) ja asetyylikoliinin (parasympaattinen) aiheuttamat metabotrooppiset muutokset voivat muuttaa näitä virtoja. AMPC aktivoi IF -kanavat, proteiinit A (PKA) fosforyila ja aktivoi ICAT CA +++.
Muskariininen vaikutus M2
Kun sydämen vagaalikuitujen (parasympaattisten) postganglionisten päätteiden vapauttamat asetyylikoliini sitoutuu sinourikulaarisen solmun M2 -muskariinireseptoreihin, GI -proteiinin aliyksikön aliyksikkö muuttaa GTP: n ja eroaa, jättäen vapautuvan βy: n kanssa.
Αi. Tämä viimeinen tosiasia vähentää CA ++ -kanavien fosforylaatiota ja aktiivisuutta ICAT: lle; Tuloksena on depolarisoivien virtojen väheneminen.
GI -proteiinin βγ -alayksiköiden muodostama ryhmä aktivoi K+: n (IKACH) virran, jolla on taipumus torjua Na+: n ja Ca ++: n tuloja ja pienentää depolarisaation nopeutta.
Niveltulos on spontaanin depolarisaation kaltevuuden väheneminen ja sykkeen väheneminen.
- M3 -reseptorit
 M3 Muskariinireseptorijärjestelmä (lähde: Takuma-Sa [CC0] Wikimedia Commonsin kautta)
M3 Muskariinireseptorijärjestelmä (lähde: Takuma-Sa [CC0] Wikimedia Commonsin kautta) Niitä löytyy sileästä lihaksesta (ruuansulatusjärjestelmä, virtsarakko, verisuonet, keuhkoputket) joissakin eksokriinisissä rauhasissa ja keskushermostossa.
GQ -proteiini on myös kytketty ja keuhkotasolla ne voivat aiheuttaa keuhkoputkien supistumista, samalla kun ne toimivat verisuonten endoteelin vapauttamisessa typpioksidissa (NO) ja aiheuttavat verisuonten laajenemista.
- M4- ja M5 -reseptorit
Nämä reseptorit ovat vähemmän karakterisoituja ja tutkittuja kuin aiemmat. Hänen läsnäolonsa keskushermostossa ja joissain ääreiskudoksissa on raportoitu, mutta niiden toiminnot eivät ole selvästi vahvistettuja.
Voi palvella sinua: Tata -laatikko: Ominaisuudet ja toiminnotAntagonistit
Näiden reseptorien yleinen antagonisti on atropiini, alkaloidi, joka on uutettu kasvista Belladon Atropa, joka sitoutuu heihin korkealla affiniteettilla, joka edustaa kriteeriä erottaa ne nikotiinireseptoreista, jotka ovat herkkiä tälle molekyylille.
On suuri joukko muita antagonistisia aineita, jotka sitoutuvat erityyppisiin muskariinireseptoreihin, joilla on erilaiset affiniteetit. Joidenkin affiniteettiarvojen yhdistelmä on palvellut tarkasti näiden reseptoreiden sisällyttämiseksi yhteen kuvattuihin luokkiin.
Osittainen luettelo muista antagonisteista ovat: Pirentsepiini, metoteektramiini, 4-vaimo, hymbaciini, AF-DX 384, tripitramiini, darifenaasiini, PD 102807, AQ RA 741, PFHHSID, MT3 ja MT7; toksiinit, jotka jälkimmäinen sisälsi vastaavasti vihreän ja mustien mamban myrkkyjä.
Esimerkiksi M1 -reseptoreilla on suuri herkkyys pirentsepiinille; M2 tripitramiinilla, metctramiinilla ja hybasiinilla; M3 4 -vesillä; M4 liittyy hyvin MT3 -toksiiniin ja myös hybasiiniin; M5 ovat hyvin samankaltaisia kuin M3, mutta niiden suhteen he ovat vähemmän sukulaisia tässä 741.
Viitteet
- Ganong WF: Neurotransmitterit ja neuromodulaattorit, julkaisussa: Katsaus lääketieteelliseen fysiologiaan, 25. ed. New York, McGraw-Hill Education, 2016.
- González JC: Muskariinireseptoreiden rooli GABAergisen leviämisen moduloinnissa hippokampuksessa. Muisti lääkärin tutkinnon valitsemiseksi. Madridin autonominen yliopisto. 2013.
- Guyton AC, Hall JE: Sydämen rytminen herätys, julkaisussa: Lääketieteellisen fysiologian oppikirja , 13. ed; AC Guyton, Je Hall (toim.). Philadelphia, Elsevier Inc., 2016.
- Piper HM: Herzerregung, julkaisussa: Physiologie des Menschen punkki patofysiologie, 31. painos; RF Schmidt et ai (toim.). Heidelberg, Springer Medizin Verlag, 2010.
- Schrader J, Gödeche A, Kelm M: Das Hertz, julkaisussa: Fysiologia, 6. painos; R Klinke et ai (toim.). Stuttgart, Georg Thieme Verlag, 2010.
- Siegelbaum SA, Clafam DE, Schwartz JH: Synaptisen siirron modulointi: Toiset lähettilät, julkaisussa: Neuraalisen tieteen periaatteet, 5. painos; E Kandel et ai (toim.). New York, McGraw-Hill, 2013.
- « Solubiologian historia, mitä tutkimuksia, sovelluksia ja käsitteitä
- Kuinka kasvit lisääntyvät? Aseksuaalinen ja seksuaalinen lisääntyminen »

