Samario -ominaisuudet, rakenne, hankkiminen, käyttö

- 3736
- 440
- Gustavo Runte DVM
Hän samarium Se on harvinaisille maametalle kuuluva kemiallinen elementti, erityisesti lantanideille ja joiden symboli on SM. Hänen nimensä on peräisin Samarskitan mineraalista, eversti Vassili Samarskyn kunniaksi, joka oli venäläinen kaivosviranomainen ja joka lahjoitti näytteitä tästä mineraalista hänen tutkimukseensa. Ranskalainen kemisti, Paul Émile Lecoq, sai oksidin ja jotkut hänen suolistaan Samarskitasta vuonna 1879, työskennellessään Pariisissa.
Boisbaudranin LeCoqille annetaan yleensä ansio Samariumin löytämiselle, vaikka oli olemassa muita kemikaaleja ja mineralogisia. Vasta vuonna 1901 ranskalainen kemisti Eugène Anatole onnistui tuottamaan ensimmäisen puhtaan Samarium -näytteen.
 Samario Samario varastoi tiukasti läpipainopakkauksen sisällä. Lähde: Hi-Res-kuvat kemiallisista elementeistä/CC kirjoittanut (https: // creativecommons.Org/lisenssit/by/3.0)
Samario Samario varastoi tiukasti läpipainopakkauksen sisällä. Lähde: Hi-Res-kuvat kemiallisista elementeistä/CC kirjoittanut (https: // creativecommons.Org/lisenssit/by/3.0) Syynä tähän eristyksen viivästymiseen johtui siitä, että Samario on suhteellisen reaktiivinen metalli, joten se ei ole luonteeltaan puhdasta, vaan muodostaa osan monista mineraalimassoista. Samoin se pitää läheisen geologisen suhteen muihin harvinaisten maametallien, kuten europiumin ja neodymiumin, kanssa, joten on vaikea erottaa sitä sellaisista epäpuhtauksista.
Samario on metalli, jolla on hyvin monimuotoisia sovelluksia, joita käytetään syöpään, treffiin, ydinreaktoreita, orgaanisia magneetit ja katalyysi.
[TOC]
Samario -ominaisuudet
Fyysinen
Samariossa on hopeavalkoinen kiilto, mutta siitä tulee nopeasti kultaa2JOMPIKUMPI3, jota kutsutaan Samariaksi. Se on yksi kovimmista ja haihtuvimmista lantanidimetalleista, joilla on vastaavasti 1072 ja 1900 ºC.
Se hapettuu suhteellisen hitauden kanssa, kun se altistetaan ilmaan tai upotettuna mineraaliöljyyn. Siksi se on säilytettävä rakkuloihin tai argonilla tai muilla inertteillä kaasulla suljetuissa astioissa. Kun lämmitetään 150 ºC: n lämpötilassa, hän hapettaa voimakkaasti sanomalla palavat kipinät, jos hän makaa kovaa.
Voi palvella sinua: lutecio: rakenne, ominaisuudet, käyttötarkoitukset, hankkiminenKemikaalit
Samariolla, kuten muilla lantanideilla, on +3 hapettumistila melkein kaikissa sen yhdisteissä; eli sitä löytyy sm -kationista3+. Se pystyy kuitenkin myös ottamaan käyttöön +2, SM: n hapettumistilan2+, Yhdisteissä, kuten SMO (samarium -monoksidi), tekstiviestit (samarium -monosulfidi) ja SMI2 (Samario Diyoduro).
Liukenee kuumaan veteen ja erityisesti laimennettuihin happoihin, kuten HCl, H2Sw4 ja ch3Cooh; Lukuun ottamatta HF: tä, koska se muodostaa SMF -suojakerroksen3 hidastaa sen purkamista. Oksidisi, sm2JOMPIKUMPI3, Se on kohtalaisen perusta, joten liuotettaessa veteen se vapauttaa huomattavia määriä OH -ioneja- SM -hydroksidin (OH) vaikutuksella3.
Suurimmalle osalle samariumyhdisteistä +3 on ominaista kelta-vihreät värit, ja jotkut erottuvat jopa luminesoiviksi.
Kemiallinen rakenne
Huoneen lämpötilassa samarium käyttää rhomboedrista kiteistä rakennetta, joka vastaa polymorfia tai a -vaihetta. Kun sitä lämmitetään 731 ºC: n lämpötilassa, tapahtuu vaihesiirtymä, joka on tiivistämällä sen kiteet kompaktiin kuusikulmaiseen rakenteeseen (HCP), jota kutsutaan faasi β β: ksi.
Jatkamalla lämmitystä lämpötilassa 922 ºC, Samario kärsii toisesta siirtymisestä kehossa olevaan kuutiorakenteeseen (BCC), nimeltään y -faasi.
Samario -kiteet voivat myös kärsiä muista siirtymistä, kun ne puristetaan suurissa paineissa tuhansien kilobarien luokkaa, jotka ovat tetragonaalisia ja kaksinkertaisia kompakteja kuusikulmaisia (DHCP) joitain näissä tutkimuksissa saatuja rakenteita.
Elektroninen kokoonpano
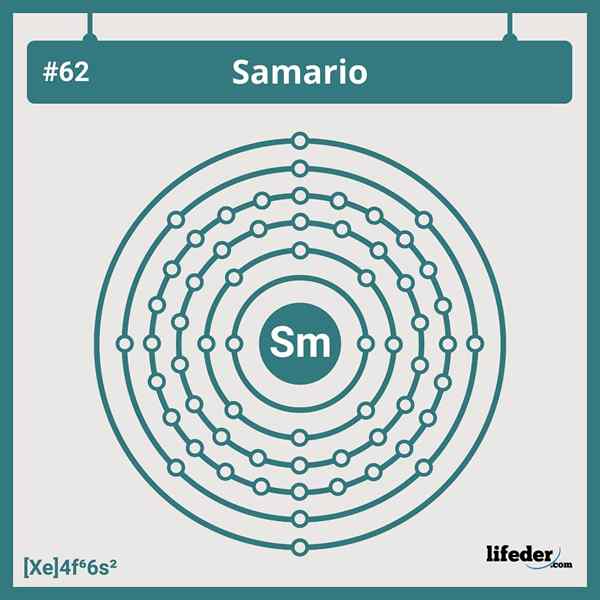 Samario -elektroninen kokoonpano
Samario -elektroninen kokoonpano Samarion lyhennetty elektroninen kokoonpano on:
Voi palvella sinua: dihydroksiasetonifosfaatti (DHAP): Ominaisuudet ja sovellukset[Xe] 6s24F6
Sen 4F -kiertoradalla on kuusi elektronia, mikä on yhtä mieltä sen asemasta Lantanides -ryhmässä. Siksi sen elektroninen kokoonpano ei koske mitään monista poikkeamista, joita näemme jaksollisessa taulukossa.
Saada
 Monazite -mineraalihiekka, pääraaka -aine samariumin saamiseksi. Lähde: D. Kemp, a. C. CilliersSSSSSSSICHLY-muokkaama Gretarsson (korvattu punainen, huonosti näkyvä SCA-palkki valkoisella)/cc by-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0)
Monazite -mineraalihiekka, pääraaka -aine samariumin saamiseksi. Lähde: D. Kemp, a. C. CilliersSSSSSSSICHLY-muokkaama Gretarsson (korvattu punainen, huonosti näkyvä SCA-palkki valkoisella)/cc by-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0) Huolimatta siitä, että se on osa harvinaisia maametallia, samarion runsaus on parempi kuin tinan ja muiden metallien. Se liittyy harvinaisten maametallien ruosteeseen, joka säveltää nämä mineraalit, kuten Cerita, La Gadolinita, La Monazita ja La Bastnasita, monatsite on yksi sen tärkeimmistä mineralogisista lähteistä, koska se sisältää noin 2.8% samarium.
Sen saamiseksi on useita menetelmiä. Yksi heistä koostuu monasiittihiekan käsittelystä ja SM -ionien erottamisesta3+, joko liuoksilla ja myöhemmillä liuottimien uuttamisella tai ioninvaihtokromatografialla.
Samarion ionit saadaan SMCL: nä3, Heille altistetaan elektrolyysi sulan NaCl- tai CACL -seoksella2. Toisaalta, jos nämä ionit saadaan SM: nä2JOMPIKUMPI3, Sitten oksidi vähenee tantalium -sulamisessa käyttämällä Lantanoa, missä samariumhöyryt tislataan niiden alemman kiehumispisteen takia. Tämän vähentämisen yhtälö on seuraava:
Tei2JOMPIKUMPI3 + 2la → 2sm +2JOMPIKUMPI3
Vähennys suoritetaan kuumana (lähes 1400 ° C) ja tyhjiöinduktiouunissa, mikä lisää samariumista johtuvien höyryjen tislausta.
Käyttää/sovelluksia Samarion
Magneetit
 SMCO -magneetteja käytetään osana kvartsikellojen funktionaalisia komponentteja. Lähde: © 2010 Tomasz Sienicki [Käyttäjä: TSCA, Mail: Tomasz.Sienicki Gmailissa.com]/cc by (https: // creativecommons.Org/lisenssit/by/3.0)
SMCO -magneetteja käytetään osana kvartsikellojen funktionaalisia komponentteja. Lähde: © 2010 Tomasz Sienicki [Käyttäjä: TSCA, Mail: Tomasz.Sienicki Gmailissa.com]/cc by (https: // creativecommons.Org/lisenssit/by/3.0) Samario on seosta koboltilla, jotta saadaan aikaan SMCO -seokset, joiden magnetointi on pysyvä ja noin 10000 kertaa suurempi kuin raudan.
Voi palvella sinua: YksikköoperaatiotNäitä Samario-Colto-magneetteja käytetään pääasiassa kameroiden, kuulokkeiden, moottorien, sähkökitarapillereiden ikkunaluukuissa sekä sotilassovelluksissa, joissa ne tukevat yli 400 ° C lämpötiloja.
Lääke
 Molecular Structure Quadramet, 153SM-EDTMP.
Molecular Structure Quadramet, 153SM-EDTMP. Itse Samario on suhteellisen myrkyllinen. Kuitenkin yksi sen radioaktiivisista isotoopeista, 153SM, jota valittaa EDTMP -molekyyli (etylendiaminotetrametyleeni -fosfonaatti, kuva yllä), palvelee kivun torjumiseksi eturauhassyövän, keuhkojen ja rintojen hoidossa. Tätä lääkettä kutsutaan Samario (153SM) lexidronamiksi, joka tunnetaan kaupallisesti nimellä Quadramet.
Ydinreaktorit
Isotooppi 149SM on erinomainen neutronien absorboiva, joten sitä käytetään ydinreaktoreissa reaktioiden kontrolloimiseksi ja räjähdyksen estämiseksi.
elektroniikka
SMS tekee lämpötilaeron sähköksi, joten sitä käytetään termoelektrisenä eri laitteissa. Sillä on myös erityispiirteistä tulla metallista suhteellisen alhaisissa paineissa.
Treffit
Isotooppin alfa -rappeutuminen 147Te (te (t1/2= 1.06 × 10yksitoista) isotooppiin 143ND: tä käytetään nykyisiin näytteisiin kivistä tai meteoriiteista maan sisällä tai sen ulkopuolella. On se etu, että atomit 147SM ja 143ND: llä on samat geologiset ominaisuudet, ts. Ne eivät kärsi suuria erotteluja metamorfisten prosessien aikana.
Katalyysi
Samarioa käytetään orgaanisessa synteesissä, kuten SMI2, Toimii pelkistävää aineena luonnollisten tuotteiden synteettisten versioiden lukuisessa synteesissä. Toisaalta SM2JOMPIKUMPI3 Se on katalysaattori etanolin kuivumiselle ja dehydralle.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Wikipedia. (2020). Samarium. Haettu: vuonna.Wikipedia.org
- Oleg d. Neikov, ja Stanislav S. (2019). Ei-rautametallijauheiden käsikirja: tekniikat ja sovellukset. (Toinen painos). Tiede.
- Enyclopaedia Britannica -toimittajat. (2020). Samarium. Toipunut: Britannica.com
- Kansallinen bioteknologiatietojen keskus. (2020). Samarium. Pubchem -elementti. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- DR. Doug Stewart. (2020). Samarium -elementti tosiasiat. Toipunut: Chemicool.com
- Strekopytov, s. (2016). Tervehdys samariumiin. Nature Chem 8, 816. doi.org/10.1038/nhem.2565
- « Gerardo Murillo (DR. ATL) elämäkerta, seinämaalaus ja teokset
- Rukoukset C -sääntöjen ja esimerkkien kanssa »

