Esterit
- 3430
- 922
- Louis Moen
 Esterit ovat orgaanisia yhdisteitä, joissa on komponentti karboksyylihappoa ja toinen alkoholi
Esterit ovat orgaanisia yhdisteitä, joissa on komponentti karboksyylihappoa ja toinen alkoholi Mitkä ovat esterit?
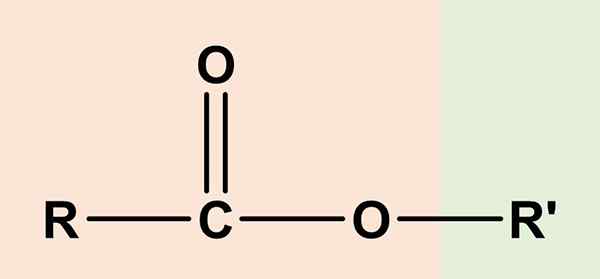
Se esterit Ne ovat orgaanisia yhdisteitä, joissa on karboksyylihappokomponentti ja toinen alkoholi. Sen yleinen kemiallinen kaava on RCO2R -' tai rcoor'. Oikea puoli, RCOO, vastaa karboksyyliryhmää, kun taas oikea tai' Se on alkoholia. Molemmilla on happiatomi ja heillä on tietty samankaltaisuus eetterien kanssa (ROR ').
Tästä syystä etyylin asetaatti, ch3Keittää2CH3, Yksinkertaisin estereistä pidettiin Etikka- tai etikkahappoeetteri, Ja sieltä nimen 'ester' etymologinen alkuperä. Niin, että esteri koostuu COOH -ryhmän happaman vedyn korvaamisesta alkoholin alkoholin vuokrauksella.
Missä ovat esterit?
Orgaanisen kemian maaperästä on monia luonnollisia lähteitä. Hedelmien miellyttävä tuoksu, kuten banaanit, päärynät ja omenat, on estereiden vuorovaikutuksen tuote monien muiden komponenttien kanssa. Niitä löytyy myös öljyjen tai rasvojen triglyseridien muodossa.
Kehomme valmistaa triglyseridejä rasvahapoista, joissa on pitkät hiilihapolliset ketjut, ja glyserolialkoholi. Se, mikä erottaa jotkut esterit muista, on sekä R: ssä, happokomponentin ketjussa, kuten R ', alkoholikomponentin ketju.
Pienen molekyylipainon esterillä on oltava vähän hiiliä R: ssä ja R: ssä, kun taas toisilla, kuten vahoilla, on monia hiiliä, etenkin R ': ssä, alkoholikomponentissa ja siten korkean molekyylipainot.
Kaikki esterit eivät kuitenkaan ole tiukasti orgaanisia. Jos karbonyyliryhmän hiilhel -ryhmän atomi korvataan yhdellä fosforilla, niin RPOOR: lla on '. Tätä kutsutaan fosfaattiesteriksi, ja ne ovat ratkaisevan tärkeitä DNA: n rakenteessa.
Siten aina, kun atomi voidaan yhdistää tehokkaasti hiileen tai happea, kuten rikkiä (Rsoor '), se voi siten muodostaa epäorgaanisen esterin.
Estres -ominaisuudet
Esterit eivät ole happoja tai alkoholia, joten ne eivät käyttäytyy sellaisenaan. Esimerkiksi sen sulatus- ja kiehumispisteet ovat alhaisemmat kuin ne, joilla on samanlaiset molekyylipainot, mutta lähempänä arvoja kuin aldehydit ja ketonit.
Butaanihappo, Cho3CH2CH2COOH: n kiehumispiste on 164º C, kun taas etyyliasetaatti, ch3Keittää2CH3, 77.1. c.
Viimeaikaisen esimerkin lisäksi 2-metyylibutaanin kiehumispisteet3Ch (ch3) Ch2CH3, Metyyliasetaatti, CHO3Keittää3, ja 2-butanoli, Cho3,Ch (oH) ch2CH3, Ne ovat seuraavat: 28, 57 ja 99º C. Kolme yhdistettä on molekyylipainot 72 ja 74 g/mol.
Matalan molekyylipesosesterit ovat yleensä haihtuvia ja niissä on miellyttäviä hajuja, minkä vuoksi heidän hedelmien sisällönsä antaa heille heidän perheensä tuoksut. Toisaalta, kun niiden molekyylipainot ovat korkeat, ne ovat värittömiä ja hajutonta kiteistä kiintoainetta tai niiden rakenteesta riippuen, niillä voi olla rasva -ominaisuuksia.
Vesiliukoisuus
Karboksyylihapot ja alkoholit ovat yleensä liukenevia veteen, ellei niillä ole korkea hydrofobinen luonne molekyylirakenteissa. Sama pätee estereihin. Kun r tai r 'ovat lyhyitä ketjuja, esteri voi olla vuorovaikutuksessa vesimolekyylien kanssa dipolidipolon ja Lontoon joukkojen voimien kautta.
Voi palvella sinua: kemiallinen yhdisteTämä johtuu siitä, että esterit ovat vetysillan vastaanottajia. Kuten? Kahdelle Rcoor -happiatomille '. Vesimolekyylit voivat muodostaa vety silloja minkä tahansa näiden hapen kanssa. Mutta kun R- tai R -ketjut ovat erittäin pitkiä, ne hylkäävät veden ympäristössään, mikä tekee mahdottomaksi heidän liukenemiselle.
Ilmeinen esimerkki tästä tapahtuu triglyseridiesterien kanssa. Heidän sivuketjunsa ovat pitkät ja tekevät öljyistä ja rasvoista liukenemattomia veteen, elleivät ne ole kosketuksissa vähemmän polaarisen liuottimen kanssa, enemmän liittyy näihin ketjuihin.
Hydrolyysireaktio
Esterit voivat myös reagoida vesimolekyylien kanssa ns. Ne vaativat kuitenkin happoa tai emäksistä ympäristöä mainittujen reaktion mekanismin edistämiseksi:
Rcoor ' + H2JOMPIKUMPI RCOvai niin + RypäleH
(Hapan puoli)
Vesimolekyyli lisätään karbonyyliryhmään, c = o. Happohydrolyysi on tiivistetty alkoholikomponentin kunkin r ': n korvaamisessa vedestä. Huomaa myös, kuinka esteri "rikkoutuu" kahdessa komponentissaan: karboksyylihappo, RCOOH ja R'OH -alkoholi.
Rcoor ' + vai niin- => RCOJOMPIKUMPI- + RypäleH
(Perusväliaine)
Kun hydrolyysi suoritetaan emäksisessä väliaineessa, peruuttamaton reaktio tunnetaan nimellä saponifikaatio. Tätä käytetään hyvin ja on kulmakivi käsityöläisten tai teollisuus saippuiden kehittämisessä.
Rcoo- Se on karboksylaatti -anioni, stabiili, joka liittyy sähköstaattisesti keskellä olevaan kationiin.
Jos käytetty pohja on NaOH, suola muodostuu. Kun esteri on triglyseridi, jolla on määritelmän mukaan kolme R -sivuketjuja, muodostetaan kolme rasvahapposuolaa, Rcoone ja glyserolialkoholi.
Pelkistysreaktio
Esterit ovat erittäin hapettuneita yhdisteitä. Se tarkoittaa, että sillä on useita kovalenttisia sidoksia hapen kanssa. Eliminoimalla C-O-sidokset tapahtuu tauko, joka lopulta erottaa happo- ja alkoholikomponentit; Ja vielä enemmän, happo pelkistetään vähemmän hapettuneeksi, alkoholiksi:
Rcoor '=> rch2Voi + r'oh
Tämä on pelkistysreaktio. Tarvitaan voimakasta pelkistävää aineita, kuten litium- ja alumiinihydridi, Lialh4, ja happamasta väliaineesta, joka edistää elektronien kulkeutumista. Alkoholit ovat pienimmät muodot, toisin sanoen ne, joilla on vähemmän kovalenttisia sidoksia hapen kanssa (vain yksi: C-OH).
Kaksi alkoholia, rch2Voi + r'oh, tule alkuperäisen Ester Rcoorin kahdesta vastaavasta ketjusta '. Tämä on menetelmä arvonerän alkoholien synteesiksi sen estereistä.
Esimerkiksi, jos halusit valmistaa eksoottisten estereiden alkoholia, tämä olisi hyvä reitti tähän tarkoitukseen.
Transterifikaatioreaktio
Esterit voidaan muuttaa muiksi, jos ne reagoivat happamiksi tai emäksisiksi väliaineiksi alkoholien kanssa:
Rcoor ' + R "Voi RCOTai " + RypäleH
Esterirakenne
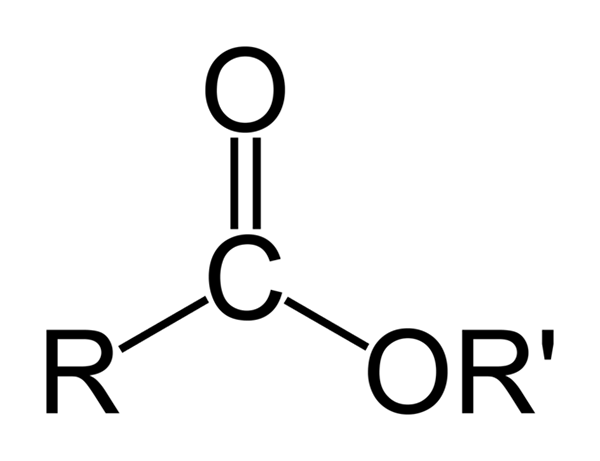 Orgaanisten estereiden yleinen kemiallinen rakenne. Lähde: Ben Mills Wikipedian kautta
Orgaanisten estereiden yleinen kemiallinen rakenne. Lähde: Ben Mills Wikipedian kautta Ylivoimainen kuva edustaa kaikkien orgaanisten estereiden yleistä rakennetta. Huomaa, että r, karbonyyliryhmä C = O ja tai ', muodostavat tasaisen kolmion, SP -hybridisaation tuote2 Keski -hiiliatomi. Muut atomit voivat kuitenkin omaksua muita geometrioita, ja niiden rakenteet riippuvat R: n luontaisesta luonteesta r: n luonteesta.
Voi palvella sinua: Nitraatit: Ominaisuudet, rakenne, nimikkeistö, koulutusJos r tai r 'ovat yksinkertaisia alqulicas -ketjuja, esimerkiksi tyyppiä (valitse2-AnCH3, Näytät sikzagueadalta avaruudessa. Näin on Pentilo Butanoat3CH2CH2Keittää2CH2CH2CH2CH3.
Mutta missä tahansa näiden ketjujen hiilissä löydettiin haara tai tyydyttymättömyys (c = c, c≡c), joka modifioi esterin globaalia rakennetta. Ja tästä syystä sen fysikaaliset ominaisuudet, kuten liukoisuus ja sen kiehumis- ja fuusiopisteet, vaihtelevat jokaisen yhdisteen mukaan.
Esimerkiksi tyydyttymättömien rasvojen R -ketjuissa on kaksoislinkkejä, jotka vaikuttavat negatiivisesti molekyylien välisiin vuorovaikutuksiin. Seurauksena heidän sulatuspisteet laskeutuvat, kunnes ne ovat nestemäisiä tai öljyjä huoneenlämpötilassa.
Vetysillan vastaanottaja
Vaikka esterien luurankojen kuva erottuu enemmän, R- ja R -ketjut, jotka vastaavat rakenteidensa monimuotoisuudesta.
Esterien rakenteellinen ominaisuus on kuitenkin ansainnut kolmioon: ne ovat vety -sillan vastaanottajia. Kuten? Karbonyyli- ja alkoholiryhmien happea (-or ').
Näillä on vapaat elektroniparit, jotka voivat houkutella vesimolekyylien osittain positiivisia vetyatomeja.
Siksi se on erityinen dipoli-dipolin vuorovaikutus. Vesimolekyylit lähestyvät esteriä (jos r o r 'ketjut eivät estä ja sillat muodostuvat C = O-H2Tai, tai OH2-O-R '.
Estereiden nimikkeistö
Esterin asianmukainen nimeäminen on välttämätöntä. Myös mahdolliset haarat, substituentit tai tyydyttymättömyys.
Kun tämä on tehty, alkoholiryhmän r 'nimi' tai jälkiliite lisätään -Ilo, Kun taas karboksilo -kooriryhmäketju r, jälkiliite -Ato. Ensin mainitaan osa R, jota seuraa sana 'of' ja sitten r '-osan' nimi '.
Esimerkiksi Cho3CH2CH2Keittää2CH2CH2CH2CH3 Siinä on viisi hiilyä oikealla puolella, ts. Ne ovat niitä, jotka vastaavat r '. Ja vasemmalla puolella on neljä hiiliatomia (mukaan lukien karbonyyliryhmä C = O).
Siksi r 'on Pentil -ryhmä ja r a butaani (karbonyylin sisällyttämiseksi ja pääketjun huomioon ottamiseen). Sitten yhdisteelle nimi on riittävä lisäämään vastaavat jälkiliitteet ja nimetä ne oikeassa järjestyksessä: butaaniAto penttiIlo.
Kuinka nimetä seuraava yhdiste: ch3CH2COOC (CH3-A3? Ketju -c (Cho3-A3 vastaa recto-butyyli-alquilical substituenttia. Koska vasemmalla puolella on kolme hiilyä, se on "propaani". Hänen nimensä on sitten: propaaniaAto Tert-mutta muttaIlo.
Kuinka esterit muodostuvat?
Esteröinti
Esterin syntetisointiin on monia reittejä, joista osa voi olla jopa uusi. Ne kaikki lähentyvät kuitenkin sitä, että rakenteen kuvan kolmio on muodostettava, ts. CO-O-linkki. Tätä varten sen on aloitettava yhdisteestä, jolla on aiemmin karbonyyliryhmä: karboksyylihappona.
Ja mitä karboksyylihappoa tulisi kytkeä? Alkoholille, muuten siinä ei olisi alkoholikomponenttia, joka karakterisoi estereitä. Karboksyylihapot vaativat kuitenkin lämpöä ja happamuutta reaktiomekanismin etenemisen sallimiseksi. Seuraava kemiallinen yhtälö edustaa yllä:
Voi palvella sinua: alumiinihydridi (ALH3): rakenne, ominaisuudet, käyttötarkoituksetRcoh + r'oh rcoor ' + h2JOMPIKUMPI
(Hapan puoli)
Tämä tunnetaan nimellä esteröinti.
Esimerkiksi rasvahapot voivat esterfisoida metanolilla, CHO: lla3Voi, niiden happojen korvaamiseksi metyyliryhmillä, joten tätä reaktiota voidaan pitää myös metylaatio. Tämä on tärkeä vaihe määritettäessä tiettyjen öljyjen tai rasvojen rasvahappoprofiili.
Happokloridien esterejä
Toinen tapa syntetisoida estereitä on asyylikloridista, RCOCL. Niissä sen sijaan, että korvataan OH -hydroksyyliryhmä, CL -atomi korvataan:
Rcocl + r'oh => rcoor ' + hcl
Ja toisin kuin karboksyylihapon steriointi, vesi ei vapautu, vaan suolahappo.
Muita menetelmiä on saatavana orgaanisen kemian maailmassa, kuten Baeyer-Villigerin hapettuminen, joka käyttää peroksihapoja (RCOOOH).
Estres käyttää
 Esterejä käytetään erilaisiin asioihin, kuten kynttilänvalmistukseen
Esterejä käytetään erilaisiin asioihin, kuten kynttilänvalmistukseen Esterien pääkäyttöön kuuluu:
- Kynttilöissä tai kynttilöissä, kuten ylemmässä kuvassa. Tätä varten käytetään erittäin pitkiä sivuketjuestereitä.
- Lääketieteen säilöntäaineita tai ruokia. Tämä johtuu parabeenien vaikutuksesta, jotka eivät ole muuta kuin para-hydroksibentsoehapon esterejä. Vaikka ne säilyttävät tuotteen laadun, on olemassa tutkimuksia, jotka kyseenalaistavat sen positiivisen vaikutuksen kehoon.
- Ne palvelevat keinotekoisten tuoksujen valmistusta, jotka jäljittelevät monien hedelmien tai kukien hajua ja makua. Niin että estereitä on herkkuissa, jäätelöissä, hajusteissa, kosmetiikassa, saippuissa, shampoissa, muun muassa kaupallisten tuotteiden joukossa, jotka ansaitsevat aromit tai houkuttelevat maut.
- Esterit voivat myös tarjota positiivisen farmakologisen vaikutuksen. Tästä syystä lääketeollisuus on omistautunut kehossa olevista hapoista johdettujen estereiden syntetisointiin arvioidakseen mahdollisia parannuksia sairauksien hoidossa. Aspiriini on yksi yksinkertaisimmista esimerkeistä näistä estereistä.
- Nestemäiset esterit, kuten etyyliasetaatti, ovat riittäviä liuottimia tietyntyyppisille polymeereille, kuten nitroselluloosa ja monenlaisia hartseja.
Esimerkkejä estereistä
Joitakin ylimääräisiä estereita esimerkkejä ovat seuraavat:
- Butanato de pentilo, ch3CH2CH2Keittää2CH2CH2CH2CH3, joka haisee albicoquesta ja päärynöistä.
- Vinyyliasetaatti, CHO3Keittää2= Ch2, josta polyvinyyliasetaattipolymeeri tapahtuu.
- Isopentilo pentaooto, ch3CH2CH2CH2Keittää2CH2Ch (ch3-A2, Mikä jäljittelee omenoiden makua.
- Etyyli -propanoaatti, ch3CH2Keittää2CH3.
- Propyylimetanoaatti, hcooch2CH2CH3.
Viitteet
- T.W -. Graham Solomons, Craight B. Freedle. Orgaaninen kemia. (Kymmenes painos, s. 797-802, 820) Wiley Plus.
- Carey, f. -Lla. Orgaaninen kemia (2006) Kuudes painos. MC Graw Hill -toimitus-
- Kemian librettexts. ESERS -nimikkeistö. Palautettu: Chem.Librettexts.org
- Hallinto. (19. syyskuuta 2015). Esterit: sen kemiallinen luonne, ominaisuudet ja käyttötarkoitukset. Otettu: Puhdas kemiallinen.com
- Orgaaninen kemia jokapäiväisessä elämässämme. (9. maaliskuuta 2014). Mitkä ovat estereiden käyttötarkoitukset? Haettu: Gen2ChemSassignment.Pikkuhenkilö.com
- Kemiat.Netto (2018). Esimerkkejä estereistä. Toipunut: kemiat.netto
- Paz María de Lourdes Cornejo Arteaga. Esterien tärkeimmät sovellukset. Otettu: UAEH.Edu.MX
- Jim Clark. (Tammikuu 2016). Johdanto -esterit. Otettu: Chemguide.yhteistyö.Yhdistynyt kuningaskunta

