Kuparisulfidirakenne, ominaisuudet, käyttö

- 3422
- 1039
- Kelly Kilback
Hän kuparisulfidi Se on epäorgaanisten yhdisteiden perhe, jonka yleinen kemiallinen kaava on CuxSja. Joo x Se on suurempi kuin ja Se tarkoittaa, että tämä sulfidi on rikkaampi kuparissa kuin rikki; ja jos päinvastoin, x Se on pienempi kuin ja, Sitten sulfidi on rikkaampaa rikkiä kuin kuparissa.
Luonnossa lukuisat mineraalit, jotka edustavat tämän yhdisteen luonnollisia lähteitä. Lähes kaikki heistä ovat rikkaampia kuparissa kuin rikkiä, ja niiden koostumus ilmaisee ja yksinkertaistaa kaavan kanssaxS; tässä x Voit jopa ottaa murto -arvoja, mikä osoittaa stökiometrisen kiinteän aineen (Cu1.75S esimerkiksi).
 Näyte Covellita Mineralista, yksi monista luonnollisista kuparisulfidin lähteistä. Lähde: James St. John [CC 2: lla.0 (https: // creativecommons.Org/lisenssit/by/2.0)]
Näyte Covellita Mineralista, yksi monista luonnollisista kuparisulfidin lähteistä. Lähde: James St. John [CC 2: lla.0 (https: // creativecommons.Org/lisenssit/by/2.0)] Vaikka rikki on elementtitilassa, sen johdannaiset yhdisteet näyttävät tummilta väriltä; Sellaista tapahtuu myös kuparisulfidilla. Kuitenkin Covelita -mineraali (ylivoimainen kuva), joka koostuu pääasiassa CUS: sta, osoittaa metallikimalaa ja sinertävää iridescenceä.
Ne voidaan valmistaa erilaisista kupari- ja rikkilähteistä, käyttämällä erilaisia tekniikoita ja muuttamalla synteesiparametreja. Siksi voit saada cus -nanohiukkasia mielenkiintoisilla morfologioilla.
[TOC]
Kuparisulfidirakenne
Linkit
Tämän yhdisteen ilme on kiteinen, joten voit heti ajatella, että se koostuu cu -ioneista+ (Monovalentti kupari), cu2+ (Kaksiosainen kupari), S2- E, jopa, s2- ja s22- (Disulfur -anionit), jotka ovat vuorovaikutuksessa sähköstaattisten voimien tai ionisidoksen kautta.
Cu: n ja S: n välillä on kuitenkin pieni kovalenttinen luonne, ja siksi Cu-S-linkkiä ei voida sulkea pois. Tästä päättelystä CUS: n (ja kaikkien sen johdettujen kiinteiden aineiden) kiteinen rakenne alkaa eroa muista ionisista tai kovalenttisista yhdisteistä löydetyistä tai karakterisoiduista.
Toisin sanoen siitä ei voida puhua puhtaista ioneista, vaan sen keskellä nähtävyyksiä (kation-anionia) sen ulkoisten orbitaalien (elektronien jakaminen) on pieni päällekkäisyys.
Koordinaatiot Covelita
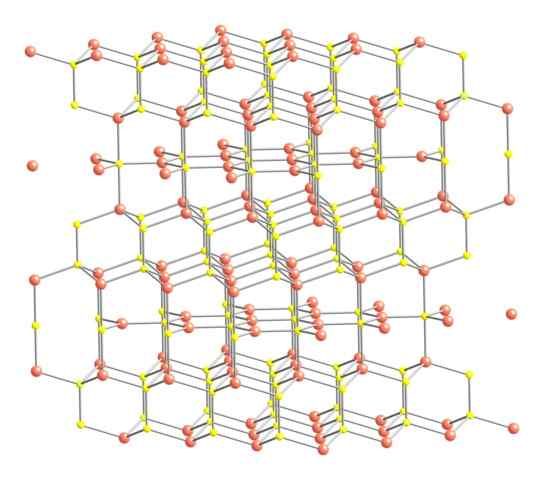 Covellitan kiteinen rakenne. Lähde: Benjah-BMM27 [julkinen alue].
Covellitan kiteinen rakenne. Lähde: Benjah-BMM27 [julkinen alue]. Edellä esitetyn koveliitin kiteinen rakenne on esitetty kuvassa. Se koostuu kuusikulmaisista kiteistä (määritelty niiden yksikkösolujen parametrit), joissa ionit sitoutuvat ja ohjaavat erilaisia koordinaatioita; Nämä ovat monipuolinen määrä läheisiä naapureita.
Voi palvella sinua: 02 -linkin tyyppiKuvassa kupari -ionit on esitetty vaaleanpunaisella palloilla, kun taas rikki keltaisilla palloilla.
Keskittymällä huomion ensin vaaleanpunaisiin palloihin, huomaa, että jotkut ympäröivät kolme keltaista palloa (trigonaalinen tasainen koordinaatio) ja toiset neljälle (tetraedrinen koordinaatio).
Ensimmäinen kuparityyppi, trigonaalinen, voidaan tunnistaa kohtisuorassa olevissa tasoilla, jotka ne antavat lukijalle, jossa ne ovat puolestaan toinen hiilityyppi, tetraedrinen.
Osallistuessaan nyt keltaisiin palloihin, joillakin on viisi vaaleanpunaista palloa (trigonaalinen bipyramidikoordinaatio) ja vielä kolme ja keltainen pallo (taas tetraedrinen koordinaatio); Jälkimmäisessä se on ennen disulfidianionia, joka voidaan visualisoida alas ja samassa koveliitin rakenteessa:
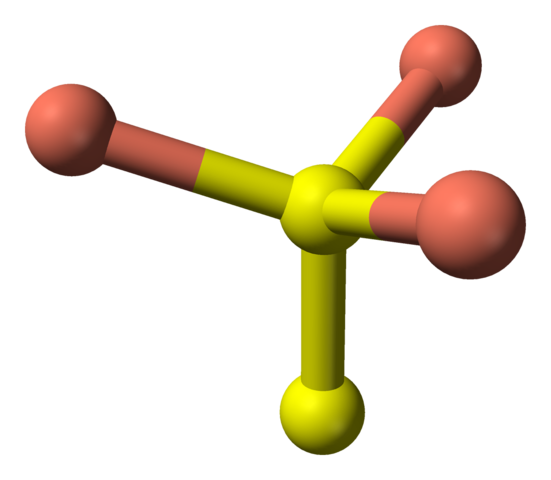 Disulfidianionin tetraedrinen koordinointi Covellitassa. Lähde: Benjah-BMM27 [julkinen alue].
Disulfidianionin tetraedrinen koordinointi Covellitassa. Lähde: Benjah-BMM27 [julkinen alue]. Vaihtoehtoinen kaava
Silloin on cu -ioneja2+, Cu+, S2- ja s22-. XPS (XPS) -valoelektroniikkaspektroskopialla tehdyt tutkimukset huomauttavat kuitenkin, että kaikki kupari on kuin kationit cu+; Ja siksi alkuperäinen CUS -kaava ilmaistaan "paremmin" (Cu+-A3(S2 -) (S2-A-.
Huomaa, että edellisen kaavan suhde Cu: Suhde on edelleen 1 ja myös kuormat peruutetaan.
Muut kiteet
Kuparisulfidi voi ottaa käyttöön ortoromisia kiteitä, kuten polymorfissa, y-cu2S, kalkkostosta; kuutio, kuten toisessa kalkkiittien polymorfissa, a-cu2S; Tetragonaali, Anilita -mineraalissa, cu1.75S; monokliininen, djurleita, cu1.96S, muun muassa.
Jokaiselle määriteltylle lasille on mineraali, ja puolestaan jokaisella mineraalilla on omat ominaisuutensa ja ominaisuutensa.
Ominaisuudet
Yleinen
Kuparisulfidin ominaisuudet ovat niiden kiinteiden aineiden suhteessa Cu:. Esimerkiksi ne, jotka esittävät anionit S22- Heillä on kuusikulmainen rakenne, ja ne voivat olla joko puolijohteita tai metallisia johtimia.
Voi palvella sinua: kaliumfosfaatti (K3PO4): rakenne, ominaisuudet, käyttötarkoituksetJos toisaalta rikkipitoisuus koostuu anioneista S2-, Sulfidit käyttäytyvät puolijohteina ja esittävät myös ionisia johtavuutta korkeissa lämpötiloissa. Tämä johtuu siitä, että heidän ionit alkavat värähtyä ja liikkua kiteiden sisällä, kuljettaen siten sähkövarauksia.
Optisesti, vaikka se riippuu myös sen kuparista ja rikki koostumuksesta, sulfidit voivat tai eivät välttämättä absorboida säteilyä sähkömagneettisen spektrin infrapuna -alueella. Nämä optiset ja sähköiset ominaisuudet tekevät potentiaalisista materiaaleista toteutettavissa eri laitteissa.
Toinen muuttujat, jotka on otettava huomioon Cu -suhteen: S, on kiteiden koko. Kyse ei ole vain enemmän "rikki" tai "kuparista" kuparisulfideja, vaan niiden kiteiden mitat antavat epätarkka vaikutuksen niiden ominaisuuksiin; Siksi tutkijat haluavat tutkia ja etsiä sovelluksia nanohiukkasten kanssa CuxSja.
Kotelo
Jokaisella mineraalilla tai kuparisulfidilla on ainutlaatuiset ominaisuudet. Kaikista niistä Covelita on kuitenkin mielenkiintoisin rakenteellisesta ja esteettisestä näkökulmasta (sen ironesenssin ja sinisten sävyjen takia). Siksi jotkut sen ominaisuuksista mainitaan alla.
Moolimassa
95,611 g/mol.
Tiheys
4,76 g/ml.
Sulamispiste
500ºC; Mutta se hajoaa.
Vesiliukoisuus
3,3 · 10-5 G/100 ml 18ºC: ssa.
Sovellukset
Lääketieteen nanohiukkaset
Ei vain vaihtelee hiukkasten kokoa, ennen kuin saavuttaa. Siten kuparisulfidi voi muodostaa nanosfäärit, sauvat, levyt, ohuet elokuvat, häkit, kaapelit tai putket.
Nämä hiukkaset ja niiden houkuttelevat morfologiat saavat yksittäisiä sovelluksia eri lääketieteen maassa.
Esimerkiksi nanojaulat tai tyhjät pallot voivat toimia huumeiden kuljettajina kehossa. Nanosferoja on käytetty, tukevat hiililasi ja hiilinanoputket, toimimaan glukoosiilmaisimina; samoin kuin niiden aggregaatit ovat herkkiä biomolekyylien havainnoille, kuten DNA.
Se voi palvella sinua: 6 luonnon PH -indikaattoria ja niiden ominaisuuksiaCUS -nanoputket ylittävät nanosferat glukoosin havaitsemisessa. Näiden biomolekyylien lisäksi immunosensorit on suunniteltu ohuista CUS -kalvoista ja tietyistä tuet patogeeniselle havaitsemiselle.
Nanokiteet ja CUS: n amorfiset aggregaatit voivat jopa aiheuttaa syöpäsolujen apoptoosia aiheuttamatta vaurioita terveille soluille.
Nanotiede
Etuosan alaosassa sanottiin, että heidän nanohiukkaset ovat olleet osa biosensoreita ja elektrodeja. Tällaisten käyttötapojen lisäksi tutkijat ja teknikot ovat hyödyntäneet ominaisuuksiaan myös aurinkokennojen, kondensaattorien, litiumparistojen ja katalyyttien suunnittelussa hyvin erityisten orgaanisten reaktioiden suhteen; välttämättömät elementit nanotieteessä.
On myös syytä mainita, että kun niitä tuetaan aktivoidulla hiilellä, NPCUS-CA-sarja (CA: Aktivoitu hiili ja NP: nanohiukkaset) osoittautui toimivan ihmisille haitallisten väriaineiden haitallisten väriaineiden poistoksi ja siksi toimivat puhdistajana puhdistajana. Lähteet veden lähteistä, jotka absorboivat ei -toivottuja molekyylejä.
Viitteet
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Wikipedia. (2019). Kuparisulfidi. Haettu: vuonna.Wikipedia.org
- Ivan Grozdanov ja Methodija Najdoski. (tuhatyhdeksänsataayhdeksänkymmentäviisi). Muuttuvan koostumuksen kuparisulfidikalvojen optiset ja sähköiset ominaisuudet. Journal of Solid State Chemistry Volume 114, numero 2, 1. helmikuuta 1995, sivut 469-475. doi.org/10.1006/JSSC.tuhatyhdeksänsataayhdeksänkymmentäviisi.1070
- Kansallinen bioteknologiatietojen keskus. (2019). Kuparisulfidi (CUS). Pubchem -tietokanta. CID = 14831. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Pietari a. Ajibade ja nandipha l. Bothri. (2017). Synteesi, optiset ja rakenteelliset ominaisuudet
- kuparisulfidi -nanokiteitä yhden molekyylin esiasteista. Kemian laitos, Fort Haren yliopisto, yksityinen laukku X1314, Alice 5700, Etelä -Afrikka. Nanomateriaalit, 7, 32.
- Yhteistyö: Volumes III/17E-17F-41C: n kirjoittajat ja toimittajat (S.F.-A. Kuparisulfidit (Cu2S, Cu (2-X) S) Kiderakenne, Latice-parametrit. Julkaisussa: Madelung tai., Rössler u., Schulz m. (toim.) Ei-tetraedrisesti sitoutuneita elementtejä ja binaarisia yhdisteitä I. Landolt-Börnstein-Group III tiivistetty aine (numeeriset tiedot ja funktionaaliset suhteet tieteessä ja tekniikassa), osa 41c. Springer, Berliini, Heidelberg.
- Äiti, f., Vafaei, a., Ghaedi, m. et al. Korean J. Kemia. Eng. (2018). Kuparisulfidin nanohiukkasten levittäminen, joka on ladattu aktivoidun hiilen termaryvärien samanaikaiseen adsorptioon: vastepintamenetelmä. 35: 1108. doi.org/10.1007/S11814-018-0012-1
- Goel, s., Chen, f., & Cai, w. (2014). Kuparisulfidin nanohiukkasten synteesi ja biolääketieteelliset sovellukset: anturista teranosteihin. Pieni (Weinheim an Der Bergstrasse, Saksa), 10 (4), 631-645. Doi: 10.1002/smll.201301174

