Jodiominaisuuksien, käyttötapojen, vasta -aiheen tinktuuri

- 1106
- 213
- Eddie Hackett
Se jodi tinktuuri Se on tummanruskea neste, joka sisältää jodia, jodidisuolaa, alkoholia ja vettä. Sitä käytetään pääasiassa antiseptisenä ja desinfiointiaineena. Sitä käytettiin ensimmäisen kerran vuonna 1839 haavojen tai vammojen käsittelemiseen.
Jodin läsnäolo (minä2) tekee siitä nopean ja aktiivisen mikrobin agentin, omaisuuden, jonka tämä elementti jakaa muiden halogeenien, kuten kloorin ja bromin kanssa. Sillä on laaja aktiivisuus bakteereja, itiöitä, viruksia ja sieniä vastaan.
 Jodi tinktuuri. Elrond/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons.
Jodi tinktuuri. Elrond/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons. I: n lisäksi2 Sisältää jodidi -ionit i- jotka mahdollistavat seoksen muodostavien ionien I stabiloinnin3-, estää jodia haihtumasta ajan myötä. Sen antimikrobinen vaikutus voi kuitenkin deaktivoida nopeasti alkalis, koska muut ioniset lajit, jotka eivät hyökkää mikro -organismeja.
Se on tuote, jota myydään apteekkeissa, joiden koostumus on hieman erilaisia toistensa välillä, vaikkakin hyvin samanlaisia kuin toisiaan, koska se on samat ainesosat.
Sitä ei pidä sekoittaa Lugol -liuokseen tai jodopovidoniliuoksiin.
[TOC]
Lääketieteellinen tuote
Nimi
- Jodi tinktuuri
- Jodi
Farmaseuttinen muoto
Tummanruskea neste alkoholin hajusta.
Sävellys
Esimerkki kaupallisesta koostumuksesta on seuraava: jodi (i2) = 2,5% (P/V), kaliumjodidi (KI) = 2,5% (P/V), etanoli (CH (CH3CH2OH) = 89% (tilavuus/tilavuus) ja puhdistettu vesi.
Jodin kemialliset ominaisuudet
Jodi on halogeeni. Se on kiinteä mustien asteikkojen muodossa, sulaa 113,7 ° C: ssa ja kiehuu 184,4 ° C: ssa. Se on vähän vesiliukoista: 0,03 g/100 g 20 ° C: ssa. Se liukenee etanoliin, bentseeniin, eetteriin ja kloroformiin.
 Jodikiteitä. Vadim Sedov/CC by (https: // creativecommons.Org/lisenssit/by/4.0). Lähde: Wikimedia Commons.
Jodikiteitä. Vadim Sedov/CC by (https: // creativecommons.Org/lisenssit/by/4.0). Lähde: Wikimedia Commons. Jodireaktiot vedessä
Vedessä suhteellisen tai disstaatioreaktio tapahtuu jodidi -ionin ja hypoydihapon muodostaen:
Yllyttää2 + H2Tai ⇔ h+ + Yllyttää- + Hoi
HOI: n pitoisuus jodiliuoksessa 25 ° C: ssa on halveksittava, koska se erottuu protonissa ja hypoyodite -ionissa.
Hoi ⇔ H+ + Io-
Voi palvella sinua: Lyijy nitraatti: rakenne, ominaisuudet, hankkiminen, käyttötarkoituksetSeuraava saldo esiintyy myös:
3 i2 + 3 h2Tai ⇔ ⇔3- + 6 h+ + 5 i-
Jodin liukoisuus veteen kasvaa lisäämällä3-) se on erittäin vakaa:
Yllyttää2 + Yllyttää- → I3-
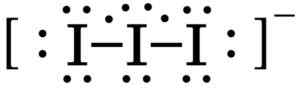 Trayoduro I3 -ionin Lewis -rakenne-. Bioika0201 / julkinen alue. Lähde: Wikimedia Commons.
Trayoduro I3 -ionin Lewis -rakenne-. Bioika0201 / julkinen alue. Lähde: Wikimedia Commons. Jodireaktiot alkalisessa liuoksessa
Kun liuotat jodia alkaliseen liuokseen, hypoydiitti -ioni muodostuu helposti:
Yllyttää2 + 2 OH- → I- + Io- + H2JOMPIKUMPI
Mutta hypoyodiitti -ioni alkalisessa liuoksessa on erittäin epävakaa ja on välittömästi suhteeton Yodato -ioniin:
3 io- ⇔ 2 i- + Io3-
Muut jodin ominaisuudet
Se ei ole yhteensopiva ammoniakin, raudan, kuparin, lyijyn, elohopean ja vismuttisuolojen, mineraalihapojen, kaliumkloorin ja muiden hapettavien yhdisteiden kanssa.
Se on pidettävä hyvin suljetussa astiassa alle 25 ° C: n lämpötiloissa.
Terapeuttinen käyttö
Se on ratkaisu, joka koskee vain ihoa.
Siinä on antiseptinen ja desinfiointiaineen käyttö ei -syventäviin haavoihin, leikkauksiin, hankauksiin ja pieniin bakteeri -infektioihin. Se palvelee gram -positiivisten ja gram -negatiivisten bakteerien aiheuttamien iho -infektioiden ennaltaehkäisyä ja estämistä ja hoitoa.
Se on tehokkain desinfiointiaine terveelle iholle ja sitä käytetään steriloimaan sitä ennen toimintaa tai ennen verinäytteitä analysoitavaksi.
Se levitetään puuvillaa tai pienellä harjalla. Se sopii aikuisille, lapsille ja vanhuksille ja se on osoitettu vain ulkoiseen käyttöön.
On kuitenkin tilanteita, joita sovelletaan suun limakalvoihin, hampaisiin tai hammaslaitteisiin, joilla on desinfiointitarkoitukset, mutta voivat aiheuttaa suun kautta tapahtuvan vuorauksen ärsytystä, joka tuottaa Itchzónin tunnetta ja johtaa joskus ampulien muodostumiseen.
 Joskus jodi -tinktuuria käytetään vastasyntyneiden vasikoiden napanuoran desinfiointiin. Kirjoittaja: Gisela Kortenbruck. Lähde: Pixabay.
Joskus jodi -tinktuuria käytetään vastasyntyneiden vasikoiden napanuoran desinfiointiin. Kirjoittaja: Gisela Kortenbruck. Lähde: Pixabay. Sitä käytetään myös pienten eläinten desinfiointiin eläimistä. Myös napanuorassa vasikoiden syntymän jälkeen.
Toimintamekanismi
Laji I2 Ja HOI ovat jodien tehokkaimpia biosidisia muotoja ja niitä on runsaasti 97%: lla, kun pH on 9 tai alhaisempi.
Voi palvella sinua: kemiallinen huokoisuus: ominaisuudet, tyypit ja esimerkitJodi suorittaa voimakkaan mikrobisidisen vaikutuksen, joka on tehokas sienten, virusten, alkueläinten (esimerkiksi Tricomonasia vastaan), kystat ja itiöiden vastaan.
Vaikka toimintamekanismia tutkitaan edelleen, on arvioitu, että diatominen jodi (I2) hyökkää mikro -organismin solun tai kapselin seinämiin ja saostaa proteiinit halogenointireaktion avulla aiheuttaen kalvolle peruuttamattomia vaurioita, mikä johtaa solukuolemaan tai virukseen.
 Jodi rikkoo bakteerien solukalvon. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay.
Jodi rikkoo bakteerien solukalvon. Kirjailija: Clker-Vector-kuvat. Lähde: Pixabay. Hapetus
On myös tutkimuksia, jotka osoittavat, että I2 Se voi muodostaa reaktiivisia happilajeja, jotka aiheuttavat hapettumisstressiä bakteerisolujen sytoplasmassa, mikä johtaa ne kuolemaan.
On määritetty, että noin 90% bakteerien absorboimasta jodista on jodidin muodossa, mikä vahvistaa hapettumisvaikutuksen. Antimikrobinen mekanismi toimii paremmin happamassa pH: ssa.
Varotoimenpiteet ja vasta -aiheet
Sitä ei pidä käyttää yliherkkailla ihmisillä jodiin tai jodideihin tai vastasyntyneillä tai kilpirauhasen häiriöillä olevilla potilailla tai jotka saavat litiumhoitoa.
Sitä tulisi käyttää varoen raskaana olevilla naisilla, koska jodidi ylittää istukan ja voi aiheuttaa vaurioita sikiölle aiheuttaen kilpirauhasen vajaatoimintaa ja kilpirauhasen soittoa.
Sen käyttö synnytyksen aikana voi johtaa imeytymiseen sekä äidin että sikiön että vastasyntyneenä voi kärsiä väliaikaisesta kilpirauhasen vajaatoiminnasta.
Sitä tulisi myös välttää äiteissä, jotka imettävät vauvaa, koska jodidi erittyy rintamaitoon ja voi tuottaa väliaikaisen kilpirauhasen vajaatoiminnan.
Haittavaikutukset joditnktuuriin
Sen pitkittyä käyttöä tulisi välttää. Iho ei tule peittää sen levityksen jälkeen. Sitä ei tule käyttää suurissa avoimissa haavoissa tai eläinten puremissa tai vakavissa palovammoissa. Se voi vaikuttaa limakalvoihin.
Tutkimuksissa potilailla, jotka oli upotettu jodin tinktuurilla terveelle iholle, havaittiin, että laastarit oli poistettava 24 tunnin kuluttua vakavien ihoreaktioiden läsnäolon vuoksi.
Se voi palvella sinua: Calomel -elektrodi: toiminta, ominaisuudet, käyttöSe voi aiheuttaa allergisia reaktioita, kuten urtikariaa, ihon alapuolella olevia infektioita, ihon verenvuotoja, kuumetta, nivelkipuja, ganglian tulehduksia ja epänormaalin korkeaa valkoisen verisolujen tasoa.
Jos nautitaan. Voi jopa johtaa kuolemaan.
Muut vastaavat tuotteet
Lugoliliuos
SO -niminen "vahva liuos" tai "Lugol -liuos" on samanlainen kuin jodin tinktuuri, mutta se voi sisältää suurempia määriä jodi- ja kaliumjodidia vesiliuoksessa.
Sitä ei pidä sekoittaa jodin tinktuuriin, koska se sisältää alkoholia, kun taas Lugol -liuoksessa on vain vettä liuottimena.
 Kaupallinen Lugol -ratkaisu. Amin/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons.
Kaupallinen Lugol -ratkaisu. Amin/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons. Yodoforinen
Ne ovat jodikomplekseja, joissa on pinta -aktiiviset aineet, kuten polyvinyylipirrolidonijohdannaiset. Sen stabiilisuus ylläpidetään happamassa väliaineessa ja suuret määrät kaliumjodidia (KI) lisätään estämään jodinusmuodostumaa.
Ne eivät ole ärsyttäviä, heillä on alhainen myrkyllisyys, hyvä pesuaine, he eivät tahraa, mutta he menettävät toimintansa alkalisessa väliaineessa.
Viitteet
- Karsa, D.R -. (2007). Biosidit. Halogeenit ja halogeenin vapauttavat yhdisteet. Käsikirjassa pintojen puhdistamiseen/puhdistamiseen. ScienEdirect.com.
- Barabas, E.S. ja Brillain, H.G. (1998). DR -aineiden ja apuaineiden analyyttiset profiilit. Ihon tutkimukset. ScienEdirect.com.
- Thornton & Ross Ltd. (2015). Jodi sävy BP, EMC. Toipunut lääkkeistä.org.Yhdistynyt kuningaskunta.
- Huumeet.com (2020). Jodi tinktuuri. Huumeet palautuivat.com.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Jodi. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Wikimedia -säätiö (2020). Lugolin jodi. Haettu jstk.Wikipedia.com.
- Malick, s. et al. (2012). Jodi-stabiloidut qu-nanohiukkasten kitosaanikomposiitti antibakteerisiin sovelluksiin. ACS App Mater ja rajapinnat. 2012 meri; 4 (3): 1313-23. NCBI toipunut.Nlm.NIH.Hallitus.
- Lyijy, d.R -. (Toimittaja) (2003). CRC: n kemian ja fysiikan käsikirja. 85th CRC -lehdistö.
- Banerjee, m. et al. (2010). Korkeus on reaktiivinen happilajien muodostuminen kolmen komponentin jodinoidun kitosaani-hopea-nanohiukkasen komposiitin antimikrobisessa aktiivisuudessa. Langmuir. 2010 AP; 26 (8): 5901-8. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Robinson, a.Lens. et al. (2015). Lyhyt viestintä: 4 antisepme -yhdisteen vaikutus napanuoran paranemiseen ja infektioasteisiin ensimmäisen 24 tunnin aikana meijerikokoissa kaupallisesta karjasta. J -. Meijerituotteet. 2015 elokuu; 98 (8): 5726-8. NCBI toipunut.Nlm.NIH.Hallitus.
- « Maquiladoran ominaisuudet, tyypit, edut ja haitat
- Säätiön jodihakemisto, menettely ja sovellukset »

