Tiosyanaatin muodostuminen, rakenne, tyypit, käyttötarkoitukset
- 3538
- 1080
- Shawn Stanton II
Hän Tiociato Se on epäorgaaninen anioni, jonka kaava on SCN-. Tätä Pseudohalogenuro tiedetään, koska sen kemiallinen käyttäytyminen muistuttaa halogeenien, ts. Fluoridin, kloridin jne. Käyttäytymistä, jne. Se tunnetaan myös nimellä Rodanida, vaikka sitä käytetään tällä hetkellä harvemmin.
Tiokianaatti on utelias laji, koska se on sijoitettu orgaanisen ja epäorgaanisen kemian väliselle rajalle. Täydellisesti se on osa sekä orgaanista että epäorgaanisia yhdisteitä, vaihtelee vain tapaan, jolla se on linkitetty tai vuorovaikutus. Tällä pseudohalogenurolla on vahva biokemiallinen yhteys syanidi -ioneihin ja niiden aineenvaihduntaan.
 Tiosyanaatti -anionia, jota edustaa täysi avaruusmalli. Lähde: Benjah-BMM27 / julkinen verkkotunnus.
Tiosyanaatti -anionia, jota edustaa täysi avaruusmalli. Lähde: Benjah-BMM27 / julkinen verkkotunnus. Ylivoimaisessa kuvassa on SCN: n esitys- Täysin avaruusmallin käyttäminen. Keltainen pallo vastaa rikkiatomia, kun taas musta ja sinertävä ovat vastaavasti hiili- ja typpiatomit. Tiokianaatissa on happea veli: Cyanato, OCN-, jossa rikiatomi korvataan happea.
Kalium Tiocianate, KSCN, on yksi tämän pseudohalogenuron edustavimmista esimerkeistä. Toisaalta orgaanisessa kemiassa on tiiosianaatteja, joiden yleiset kaavat ovat RSCN, kuten metyyli -tiokeskiaseen, CHO3SCN.
[TOC]
Koulutus
Syanidin ja rikin välinen reaktio
SCN -kaava- antaa sinun vilkaista sen, että sen synteesi perustuu syanidireaktioon, CN-, Lajin kanssa, joka lahjoittaa rikkiatomeja. Syanidi todellakin voi hyvinkin reagoida alkuaineen rikin kanssa, S8, tai tiosulfaatti -anionien kanssa, S2JOMPIKUMPI32- Tiosyanaatin tuottaminen:
8 CN- + S8 → 8 SCN-
CN- + S2JOMPIKUMPI32- → SCN- + S2JOMPIKUMPI32-
Voi palvella sinua: CO2 -linkkityyppiToista reaktiota katalysoi kuitenkin entsyymijärjestelmä, joka koostuu rikkitransferaasitiosulfaatista. Kehomme on nämä entsyymit, ja siksi pystymme metaboloimaan syanoglukosideista tulevia syanideja (hiilihydraatit, joilla on CN -ryhmä). Tällä tavalla ruumis pääsee eroon haitallisesta CN: stä-, jotka häiritsevät solujen hengitysprosesseja.
Tiokianaatit liuotetaan sylkeen ja vähemmässä määrin plasmassa. Heidän pitoisuutensa paljastavat, kuinka altistuneet ovat yksilöitä syanideille joko liiallisen ruuan saannin vuoksi, jotka sisältävät sitä luonnollisessa muodossaan (pähkinät, mantelit, palkokasvit, linazat jne.) tai savukkeiden ja tupakan savun pitkäaikainen hengittäminen.
Tiocian happo neutralointi
SCN- Se voidaan saada neutraloimalla happama muoto: Tiocianiinihappo, HSCN tai isotosyaaninen, HNCS. Käytetystä pohjasta riippuen saadaan myös tiokianaattisuola.
Rakenne
Linkit
 Tiokianaattiresonanssirakenteet. Lähde: Ben Mills Wikipedian kautta.
Tiokianaattiresonanssirakenteet. Lähde: Ben Mills Wikipedian kautta. Ylivoimainen kuva osoittaa, kuinka SCN: n negatiivinen kuorma on jaettu-. Huomaa, että kaikilla atomeilla on SP -hybridisaatio2, Joten ne sijaitsevat samalla linjalla.
Elektronipari voi olla hyvällä paikalla typpiatomilla tai rikkiatomilla. Tämä tosiasia selittää tiokianaatin tärkeän ominaisuuden: se on bident ligandi, toisin sanoen kykenevä yhdistämään kahdella eri tavalla.
Isomería
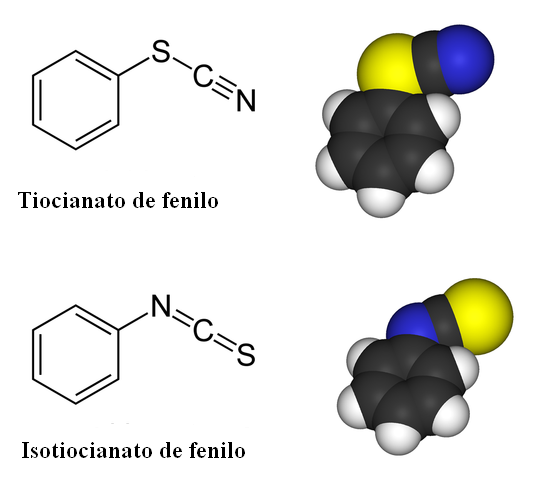
 Liitäntä isomeria fenyylitiosyanaatille. Lähde: Benjah-BMM27 / julkinen verkkotunnus
Liitäntä isomeria fenyylitiosyanaatille. Lähde: Benjah-BMM27 / julkinen verkkotunnus Tiokianaattiyhdisteissä linkki isomeeri on läsnä. Kuten ylemmässä kuvassa voidaan nähdä, SCN- Se voidaan yhdistää bentseenirenkaaseen tai fenyyliryhmään joko sen rikkiatomin tai typpiatomin avulla. Kun sitä on linkitetty S: ksi, sitä kutsutaan Tiocianaatiksi; Vaikka se on linkitetty N: hen, sitä kutsutaan isotiohianaatiksi.
Voi palvella sinua: Stanislao CannizzaroHuomaa, kuinka -Scn tai -NCS näyttää lineaarisilta fragmentteilta. Tämä lineaarinen geometria pysyy muuttumattomana sekä orgaanisissa että epäorgaanisissa tiiolesiaatteissa.
-CS -sidos on vahvempi kuin -Scn, koska typpi, koska se on pienempi, keskittyy paremmin elektroniparin negatiiviseen kuormaan, jonka kanssa kovalenttinen sidos muodostuu.
Vuorovaikutus
SCN -anionit- He eivät voi olla vuorovaikutuksessa toistensa kanssa sähköstaattisten torjumien takia. Siksi he tarvitsevat kationeja, jotta he voivat olla vuorovaikutuksessa sähköstaattisesti ja "rakentaa" kristallin. Epäorgaaniset tiokianaatit ovat yhdisteitä ionisessa olemuksessa.
Samaan aikaan orgaanisten tiokosianaattien suhteen niiden vuorovaikutukset perustuvat van der Waalsin voimiin; Erityisesti dipoli-dipolotyypin edustajat. SCN -ryhmä, joko linkitettynä, on polaarinen, ja siksi se myötävaikuttaa yhdisteen napaisuuden lisääntymiseen. On selvää, että dipoli-dipolo-vuorovaikutukset ovat heikompia kuin ioniset nähtävyydet, esimerkiksi KSCN: ssä+SCN--A.
Orgaaniset tiokeianaatit
Orgaaniset tiokeianaatit on esitetty RSCN -kaavalla. Toisaalta, koska meillä on yhteyshenkilö isomeria, meillä on myös isoofilaatteja, RNC: t.
Siten se riittää korvaamaan r alkyyli- tai aromaattisilla molekyylifragmenteilla useiden yhdisteiden saamiseksi. Esimerkiksi Cho3CH2SCN on etyylitiohianaatti. Edellisessä osassa r6H5SCN tai φ-SCN.
Epäorgaaniset tiokeianaatit
Epäorgaanisia tiosyanaatteja pidetään tiokianihapon, HSCN: n suoloina, ja niitä voidaan edustaa MSCN: nä, missä M on metallinen kationia tai ammoniumkationia. Siten meillä on esimerkiksi:
-Nascn, natrium -tiosyanaatti
-Nh4SCN, Ammonium Tiocianate
Se voi palvella sinua: erot orgaanisten ja epäorgaanisten yhdisteiden välillä-Usko (SCN)3, Ferri -tiosyanaatti
Monet epäorgaaniset tiokianaatit ovat värittömiä kiinteitä suoloja.
Toisaalta, meillä on myös tiokianaattikompleksit liuoksessa. Esimerkiksi vesiliuos, joka sisältää uskon ionit3+ valmistuu SCN -ioneilla- Muodostaa [usko (NCS) (H2JOMPIKUMPI)5-2+, joka on veripunainen.
Samoin SCN- Se kykenee kompleksointiin muiden metallikationien, kuten CO: n kanssa2+, Cu2+ ja sinä4+, Jokainen on peräisin värikkäästä kompleksista.
Sovellukset
SCN -anioni- Sitä käytetään fotometrisiin metallimäärityksiin vesiliuoksissa. Tämä menetelmä perustuu tarkasti tiocianaattien värikkäiden kompleksien absorbanssin mittaamiseen metallien kanssa.
Tästä erityisestä käytöstä toiset ovat yhtä monipuolisia kuin olemassa olevat tiokianaatit.
Orgaaniset tiokosianaatit on tarkoitettu enemmän kuin mikään rakenteellisina lohkoina lääketieteessä käytettyjen rikkiyhdisteiden synteesille.
Toisaalta epäorgaanisia tiokianaatteja, joilla on värillisiä, käytetään tekstiiliteollisuuteen tai venereiden lisäaineena. Myös koska se on hyvä SCN -ionin avunantajat-, Niitä vaaditaan hyönteismyrkkyjen ja sienitautien torjuntaan.
Tiocianaateista suosituimpia ovat NASCN ja KSCN, joita molemmat pyydetään hyvin lääkkeissä, rakenteissa, elektronisissa ja maatalousteollisuudessa.
Viitteet
- Morrison, r. T. ja Boyd, R, N. (1987). Orgaaninen kemia. 5. painos. Toimituksellinen Addison-Wesley Inter-American.
- Carey f. (2008). Orgaaninen kemia. (Kuudes painos). MC Graw Hill.
- Graham Solomons t.W -., Craig B. Freedle. (2011). Orgaaninen kemia. (10. painos.-A. Wiley Plus.
- Shiver & Atkins. (2008). Epäorgaaninen kemia. (Neljäs painos). MC Graw Hill.
- Wikipedia. (2020). Tiosyanaatti. Haettu: vuonna.Wikipedia.org
- Kansallinen bioteknologiatietojen keskus. (2020). Tiosyanaatti. Pubchem -tietokanta., CID = 9322. Toipunut: Pubchem.NCBI.Nlm.NIH.Hallitus
- Elsevier B.V. (2020). Tiosyanaatti. Tiede. Haettu: ScienEdirect.com
- Nouryon. (2020). Tiosyanaatti. Haettu: rikkivihjeet.Nouryon.com
- Riedel, k., Hagundan, h.W -. Ja Scherer, G. (2013). Tiosyanaatti plasmassa ja sylkeissä [BiomonitoRing Methods, 2013]. Työterveyden ja turvallisuuden MAK -kokoelmassa (toim. Ja). Doi: 10.1002/3527600418.BI5712SALE0013
- « Journalistiset tekstit ominaisuudet, rakenne, tyypit, esimerkit
- Erikoistuneet tekstit ominaisuudet, rakenne, tyypit, esimerkit »

