Hiiliatomi
- 3076
- 643
- Ronald Reilly
Selitämme, mikä on hiiliatomi, sen elektroninen rakenne, ominaisuudet ja kiertoradan hybridisaatio.
 Hiiliatomijärjestelmä
Hiiliatomijärjestelmä Mikä on hiiliatomi?
Hiili on jaksollisen taulukon elementti 6 ja on yksi tärkeimmistä olemassa olevista elementeistä. Sen merkitys syntyy erittäin rikkaasta ja monimuotoisesta kemiasta, joka tekee tämän elementin muodostavan Elämän perusta planeetalla, kuten tiedämme.
Kyse on noin a ei-metalli kuulua Ryhmä 14 jaksollisesta taulukosta (entinen ryhmä 4A) ja toinen jakso. Luonnollisessa muodossaan se liittyy hiilen (sekä mineraalien että vihannesten) ja noen kanssa, jossa se on pääasiassa grafiitin tai muun alotroopin muodossa.
Hän Hiiliatomi Se on yksi pienimmistä jaksollisesta taulukosta. Se on tetravalenttia atomi, ts. Se voi muodostua Enintään neljä linkkiä muiden atomien kanssa yhtä suuret tai erilaiset kuin samat.
Hiili on erittäin tärkeä ihmisille. Se on yksi kehomme pääkomponenteista, muodostaen yli 19% sen massasta. Lisäksi siinä on myös useita teknisiä sovelluksia, jotka on johdettu sen atomiominaisuuksista.
Hiiliatomin ominaisuudet
- Hiiliatomi on ei -metalli: Hiili on ei -metallinen elementti, joka voidaan yhdistää moniin muihin jaksollisen taulukon elementteihin. Hiiliatomit voivat hankkia tai antaa elektroneja muille atomeille, tullaan anioneiksi tai kationeiksi.
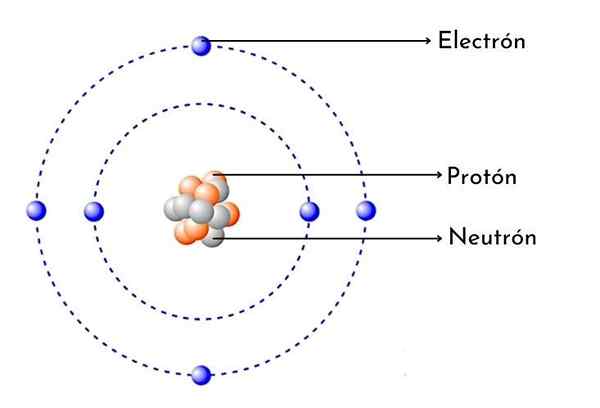
- Sen ytimessä on 6 protonia: Hiilen atomi lukumäärä on 6, mikä tarkoittaa, että sen ytimessä on 6 protonia. Se tarkoittaa myös, että neutraalissa hiiliatomisessa on 6 elektronia ytimen ympärillä.
Voi palvella sinua: magneettinen erotus- Se kuuluu jaksollisen taulukon lohkoon P: Elektroninen hiilen kokoonpano sen perustilassa on 1s2 2s2 2 p2. Kuten voidaan nähdä, viimeiset Valencia -elektronit sijaitsevat P -orbitaaleissa, joten hiili kuuluu jaksollisen taulukon lohkoon P.
- Hiiliatomin valenssit ovat +2, +4 ja -4: Hiilen valenssikerroksesta puuttuu vain 4 elektronia täytettäväksi kokonaan ja siten hankkia jalokaasun elektroninen konfiguraatio. Tästä syystä hiili voi muodostaa karbidianionin, c4-, jossa on 4 elektronia enemmän kuin neutraali hiili. Toisaalta hiiliatomi voi myös menettää kaksi 2P -elektronia, jolloin siitä tulee hiilikationia (C2+) tai kaikki 4 elektronia Valenciassa, tulossa hiilikationiksi (C4+-A.
- Voit muodostaa useita alotrooppeja: Alkeishiili löytyy kahdesta yleisestä luonnollisesta muodosta, jotka ovat grafiittia ja timantteja, joilla on radikaalisti vastakkaiset ominaisuudet. Lisäksi voit muodostaa erilaisia kavereita, hiili- ja grafeeninanoputkia.
Hiiliatomin kolme isotoopia
Kaikissa hiiliatomeissa on kuusi protonia ytimessä, mutta kaikilla ei ole samaa määrää neutroneja, mikä aiheuttaa kolme isotoopia:
- Hiili-12 (12C): Se on vakain ja runsas (noin 98,9%). Sen ytimessä on 6 neutronia.
- Hiili-13 (13C): Siinä on 7 neutronia.
- Hiili-14 (14C): Se on radioaktiivista käyttöä vanhojen esineiden päivämäärille.
Hiiliatomin elektroninen rakenne
Kuten jokainen hiiliatomi, sen ytimessä on kuusi positiivista protonia, silloin sillä on myös 6 elektronia Negatiivisen kuorman kääntyessä.
Voi palvella sinua: Alikvotti (kemia)Näiden elektronien jakautumisen tapa tai hiiliatomin elektroninen kokoonpano on:
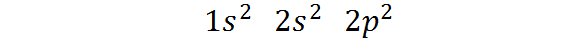
Tämä elektroninen kokoonpano osoittaa sen Hiilellä on 2 elektronia 1s kiertoradalla, Kaksi elektronia Orbital 2: ssa, ja Kaksi elektronia jakautuneena kolmen kiertoradan kesken 2p.
Toisaalta hiilen valenssikerros on kerros L, joka vastaa tasoa n = 2, koska se on korkein tason kerros, joka sisältää elektroneja. Kuten voimme nähdä, hiilellä on yhteensä 4 elektronia tasolla 2, Joten sanomme niin Siinä on 4 Valencia -elektronia.
Tästä syystä hiili sijaitsee, jossa sitä aiemmin kutsuttiin jaksollisen taulukon ryhmäksi 4a.
Atomillinen kiertoradan hybridisaatio hiiliatomisessa
Atomit reagoivat ja linkittävät toisiinsa valenssielektroniensa ja heidän miehittämiensa kiertorajojen kautta. Jälkimmäisillä ei kuitenkaan aina ole riittävää suuntausta tarvittavien linkkien muodostamiseksi.
Valencian linkkiteorian mukaan atomit sekoittavat atomiorbitaalinsa muodostaen uusia hybridi -kiertoratoja, joilla on asianmukainen ohjaus. Tätä prosessia kutsutaan hybridisaatio.
Hiiliatomien yhdistävien atomien lukumäärästä riippuen se sekoittaa tai hybridisoi eri määrän puhtaita atomisiorbitaaleja. Tämä aiheuttaa kolme erilaista hybridisaatiota, Mitä ne ovat:
SP
Tapahtuu, kun hiili on kytketty vain Kaksi atomia. Tässä tapauksessa kiertoradan, jolla on yksi kolmesta P -kiertoradalla, on sekoitettu, mikä johtaa kahteen SP -kiertoradalle, jotka osoittavat vastakkaisiin suuntiin (180º toisistaan).
Voi palvella sinua: Mercury BarometriPi -sidosten muodostamiseen käytetään kahta p -kiertorataa, jotka jätetään ilman sekoitusta. Hiiliatomi voi muodostua Kolminkertainen linkki (joka sisältää kaksi Pi -sidosta) yhdellä atomilla tai voi muodostaa Kaksi kaksinkertaista linkkiä, yksi jokaisella atomilla (ja linkillä pi) kanssa).
SP2
Kun hiili haluaa liittyä Kolme atomia, Tarvitset kolme hybridi -kiertorataa, joten sekoita kolme puhdasta kiertorataa: kiertoradan S ja kaksi kiertorataa P. Tämä tuottaa kolme SP -hybridi -orbitaalia2 Se merkitsee tasapainon kolmion kulmia.
Orbitaali P, jota ei käytetty.
SP3
Kun hiili aikoo linkittää Neljä atomia, Sekoita valenssikerroksen 4 puhdasta kiertorataa 4 hybridi -kiertoradan SP: n tuottamiseksi3. Nämä viittaavat tavallisen tetraedron kärkeen.
Koska PI -sidosten muodostamiseksi ei ole kiertorataa, hiili, jolla on SP -hybridisaatio3 Voit muodostaa vain neljä yksinkertaista linkkiä eikä useita linkkejä.
Viitteet
- Britannica, Encyclopaedian toimittajat. Hiili - tosiasiat, käytöt ja ominaisuudet. Otettu https: // www.Britannica.com/tiede/hiilikemiallinen elementti
- Globaali seurantalaboratorio. (S. F.-A. Hiilisyklin kasvihuonekaasut. Otettu https: // gml.NOAA.Gov/ccg/isotoopit/kemia.HTML

