Döbereiner -triadit
- 2366
- 191
- Juan Breitenberg V
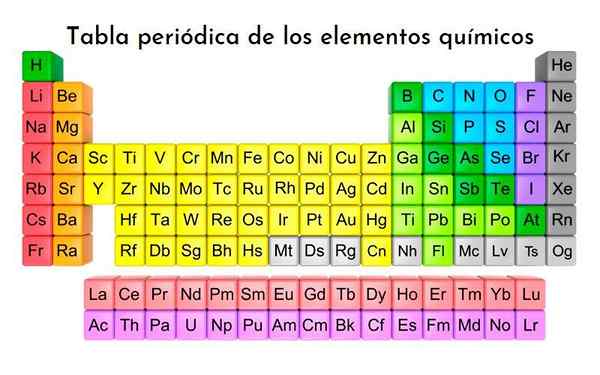
 Elementtien jaksollinen taulukko, kaikki tähän mennessä löydetyt kemialliset elementit luokitellaan. Lisenssillä
Elementtien jaksollinen taulukko, kaikki tähän mennessä löydetyt kemialliset elementit luokitellaan. Lisenssillä Mitkä ovat Döbereinerin triadit?
Se Döbereiner -triadit Ne ovat ensimmäinen koe, jossa ryhmiteltiin kolme kemiallista elementtiä, joilla on samanlaiset ominaisuudet, yhdistämällä ne atomipainoihinsa. Ovat osa 118 kemiallista elementtiä, jotka ovat esitettyjen reaktioiden monimuotoisuus ja niiden yhdisteet niiden merkittävin ulkonäkö.
Ajatuksena elementtien luokittelusta on käsitellä niiden kemiallisia ominaisuuksia asianmukaisesti kehittämättä joukkoja ja teorioita kullekin niille.
Sen jaksollinen luokittelu on antanut erittäin hyödyllisen systemaattisen kehyksen korreloidakseen niitä muutaman hyvin yksinkertaisen ja loogisen mallin mukaan.
Elementit on järjestetty systemaattisesti riveihin ja sarakkeisiin, joissa on lisääntyviä atomilukuja, ja uusien löytöjen tila on varattu.
Vuonna 1815 tiedettiin vain noin 30 elementtiä. Vaikka näistä ja niiden yhdisteistä oli saatavana paljon tietoa, ei ollut mitään ilmentää.
Tilauksen löytäminen oli kuitenkin vaikeaa, mutta se oli vaikeaa.
Tutustu Döbereinerin kolmioihin
Tutkija Johann Wolfgang Döberereiner (1780-1849) teki tärkeitä havaintoja numeerisesta säännöllisyydestä elementtien atomipainoissa. Hän huomasi ensimmäisenä useiden kolmen elementin ryhmien olemassaolon, jota hän kutsui kolmiksi, mikä osoitti kemiallisia yhtäläisyyksiä.
Nämä elementit paljastivat tärkeän numeerisen suhteen, koska kun ne on määrätty vastaavan tai atomipainon mukaan, keskuselementin paino osoittautui kahden jäljellä olevan elementin likimääräiseksi keskiarvoksi kolmessa.
Voi palvella sinua: Natriumfosfaatti: rakenne, ominaisuudet, synteesi, käyttääVuonna 1817 Döberereiner havaitsi, että jos tietyt elementit yhdistettiin binaarisissa yhdisteissä happea, näiden yhdisteiden ekvivalenttien painojen välillä voitaisiin havaita numeerinen suhde.
Siten, kun tarkasteltiin kalsium-, strontium- ja bariumoksideja, strontiumioksidin vastaava paino oli suunnilleen kalsiumoksidin ja bariumoksidin keskiarvo. Sanotaan.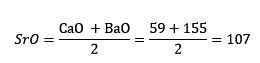
Vaikka Döbereiner työskenteli pesojen kanssa, jotka oli johdettu vain pienistä tiukkoista kokeellisista menetelmistä, mutta voimassa voimassa, niiden arvot ovat tiiviisti hyviä.
Döbereinerin havainnolla ei ollut juurikaan vaikutusta kemikaalimaailmaan, mutta siitä tuli sitten erittäin vaikutusvaltainen. Tällä hetkellä sitä pidetään yhtenä jaksollisen järjestelmän kehityksen pioneereista.
Kaksitoista vuotta myöhemmin, vuonna 1829, Döbereiner lisäsi kolme uutta kolmiota, jotka on esitetty alla:
Halogeeniryhmä
Kloorilla, bromilla ja jodilla on samanlaiset kemialliset ominaisuudet ja ne muodostavat kolmion. Nämä elementit ovat hyvin reaktiivisia metalleja. Jos ne on lueteltu suhteellisen massan lisäämisjärjestyksessä, he ovat vähentävän reaktiivisuuden järjestyksessä. Bromolla on väliatomia massa kloorin ja jodin välillä.

Keskimääräisen bromin atomimassa.
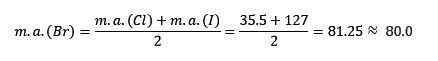
Saatu keskiarvo on lähellä bromin atomimassaa (BR).
Kemiallisten ominaisuuksien yhtäläisyydet:
1. Ne ovat kaikki ei -metallia.
2. Ne kaikki reagoivat veden kanssa happojen muodostamiseksi (esimerkiksi: HCL, HBR, HF).
Se voi palvella sinua: Biodiesel: Historia, ominaisuudet, tyypit, edut, haitat3. Jokaisella on yhden valencia (esimerkiksi: HCL, HBR, HF).
4. Ne kaikki reagoivat alkalimetallien kanssa neutraalien suolojen muodostamiseksi (esimerkiksi NaCl, NaBab, NAI)
Emäksinen metalliryhmä
Litiumilla, natriumilla ja kaliumilla on samanlaiset kemialliset ominaisuudet ja ne muodostavat kolmion. Nämä elementit ovat pehmeitä ja kevyitä, mutta erittäin reaktiivisia metalleja.
Jos ne on lueteltu suhteellisen atomimassan lisäämisjärjestyksessä, ne ovat myös lisääntyvän reaktiivisuuden järjestyksessä. Natriumilla on väliatomia massa litiumin ja kaliumin välillä.

Keskielementin atomismassa natrium (NA) on yhtä suuri kuin litiumiatomien massa (Li) ja kalium (k) keskiarvo.
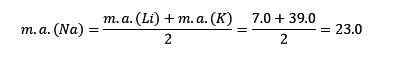
Kemiallisten ominaisuuksien yhtäläisyydet:
1. Ne ovat kaikki metalleja.
2. Kaikki reagoivat veden kanssa muodostaen emäksisiä liuoksia ja vetykaasua.
3. Jokaisella on Valencia de One (esimerkiksi: LICL, NaCl, KCL).
4. Sen karbonaatit ovat resistenttejä lämpöhajoamiselle.
Ryhmä laskimia tai amfumoja
Rikki, seleenillä ja telurolla on samanlaiset kemialliset ominaisuudet ja ne muodostavat kolmion. Seleenissä on väliatomia massa rikin ja Teluron välillä.

Keskimääräisen seleenielementin (SE) atomimassa on yhtä suuri kuin rikin (S) ja Teluron (TE) keskimääräiset atomimassat (TE).
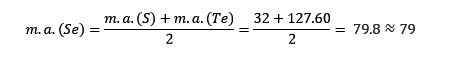
Saatu keskiarvo on jälleen lähellä seleenin atomitaikinaa (SE).
Kemiallisten ominaisuuksien yhtäläisyydet:
1. Yhdistelmät näiden elementtien hydrogeenien kanssa johtavat myrkyllisiin kaasuihin.
2. Jokaisessa näistä elementeistä on 6 valenssielektronia.
3. Metalliominaisuudet lisääntyvät, kun atomiluku kasvaa.
Döberereiner varoitti myös, että olemisen pätevyyden oli paljastettava kemialliset suhteet elementtien ja numeeristen suhteiden välillä.
Se voi palvella sinua: kaliumkloraatti (kclo3)Toisaalta hän kieltäytyi ryhmittelemästä fluoria yhdessä kloorin, bromin kanssa.
Hän oli myös haluttomia pohtimaan triadien ulkonäköä erilaisten elementtien, kuten typen, hiilen ja hapen välillä.
Döbereinerin työ keskittyi kolmion elementtien välisiin suhteisiin, mutta ei antanut aavistustakaan niiden välisestä suhteesta.
Riittää sanoen, että Döbereinerin tutkimuksessa todettiin käsitteen triadista voimakkaana käsitteenä, että useat muut kemikaalit ottavat pian huomioon.
Itse asiassa Döbereiner -triadit edustivat ensimmäistä vaihetta elementtien ryhmittelemiseksi jaksollisen taulukon pystysuoriin sarakkeisiin ja siten perustamaan järjestelmän, joka selittää kemialliset ominaisuudet ja paljastaa elementtien fysikaaliset suhteet.
Kolmioiden laajennus
Muut kemikaalit laajensivat Döbereinerin kolmioita, jotka sisältävät enemmän kuin alkuperäiset kolme elementtiä. Esimerkiksi fluoridia lisättiin klooria sisältävän kolmion, bromin ja jodin yläosaan.
Muita "kolmioita" tapahtui, kuten sellainen, joka sisälsi happea, rikkiä, seleeniä ja Telurioa. Mutta ei ollut järjestelmää korreloimaan niitä kuin kokonaisuus.
Yksi tärkeimmistä haitoista oli, että monet suhteelliset atomimassat olivat vielä väärässä ajankohtana.
Viitteet
- Johann Wolfgang Döbereiner. Toipunut Britannicasta.com.
- Mikä on jaksollisen taulukon ryhmä 16? Kuinka näitä elementtejä käytetään? Quorasta toipunut.com.

