Perusoksidit

- 2447
- 681
- Louis Moen
Selitämme, mitkä ovat perusoksidit, kuinka niiden ominaisuudet, nimikkeistö ja annamme useita esimerkkejä,
 Monilla perusoksideilla on silmiinpistäviä, ominaisia metalliväreihin
Monilla perusoksideilla on silmiinpistäviä, ominaisia metalliväreihin Mitkä ovat perusoksidit?
Se perusoksidit Ne ovat epäorgaanisia yhdisteitä, jotka muodostavat hapen ja metallin välinen liitto. Niitä kutsutaan perusoksideiksi, koska ne tuottavat emäksisiä tai emäksisiä liuoksia liukeneessa veteen. Myös siksi, että ne reagoivat happojen kanssa suolan ja veden muodostamiseksi happo-emäs neutralointireaktion kautta.
Perusoksidit ovat hyvin yleisiä. Itse asiassa suurin osa luonnon metalleista löytyy oksidimaakista, joten niitä kutsuttiin aiemmin maaksi.
Perusoksidit ovat erittäin tärkeitä teollisuudelle. Monet teollisuudessa käytetyt värilliset pigmentit ovat oksideja. Muita oksideja käytetään pohjana maalauksille, erityisesti titaani-, lyijy- ja sinkkioksideille.
Emäksiset oksidioksidit
Ne ovat binaarisia yhdisteitä
Nämä yhdisteet muodostavat vain kaksi elementtiä: happi ja metalli. Siksi ne ovat binaarisia yhdisteitä.
Sen empiirinen kaava on m2JOMPIKUMPIX tai MoX/2
Oksidien hapen valenssi on aina -2, joten oksidien empiiriset kaavat yksinkertaistetaan, kun metalli Valencia on vääntömomentti. Sama ei kuitenkaan tapahdu, kun se on outoa.
Esimerkiksi natriumoksidin empiirinen kaava on NA2Tai koska natriumissa on Valencia +1 (pariton). Sen sijaan kalsiumoksidin empiirinen kaava on CaO, koska kalsiumilla on Valencia +2.
Ne ovat epäorgaanisia yhdisteitä, melkein aina ionisia
Useimmat emäksiset oksidit ovat kiteisiä ionisia yhdisteitä. Tähän sisältyy kaikkien alkalimetallien, kaikkien alkaliinien (paitsi beryllium) oksidit ja siirtymämetallien ensimmäinen sarja.
Voi palvella sinua: kemiallinen sidosHeillä on erittäin korkea fuusio- ja kiehumispisteet
Ioninen sidos pitää kaikki ionit, jotka muodostavat perusoksidit voimakkaasti yhtenäisesti. Tämä vaikeuttaa niiden sulamista ja vielä vaikeampaa höyrystää. Tästä syystä heillä on erittäin korkea fuusio- ja kiehumispisteet.
Ne ovat kiinteitä huoneenlämpötilassa
Koska kaikki perusoksidit ovat samanlaisia fuusiopisteitä, kaikki perusoksidit ovat kiinteitä huoneenlämpötilassa.
Ne ovat emäksisiä yhdisteitä
Syy siihen, miksi niitä kutsutaan emäksisiä oksideja, on juuri sen happo-emäsominaisuuksien ominaisuuksien takia. Oksidit, joilla on suurempi ioninen luonne, tuottavat emäksisiä liuoksia liuottaessasi veteen ja reagoivat myös happojen kanssa, neutraloimalla ne.
On kuitenkin huomattava, että kaikki metallioksidit eivät ole emäksiä. Jotkut ovat neutraaleja, muut hapot ja muut ammattikorit.
Useimmat ovat vähän liukoisia tai liukenemattomia veteen
Kaikki emäksiset oksidit ovat liukenemattomia veteen, alkali- ja bariummetallien oksidien lukuun ottamatta. Ne ovat kuitenkin liukenevia happoliuoksiin.
Kuinka perusoksidit ovat?
Perusoksidit voidaan muodostaa spontaanisti, kun metallit altistuvat ilman happea. Itse asiassa metallien pinnalle muodostuneet korroosiokerrokset koostuvat eri emäksisistä oksideista.
Mukana oleva metalli, yleensä se on emäksinen, emäksinen metalli tai siirtymämetalli.
Voit kirjoittaa kolme yleistä reaktiota oksidien muodostumiseen riippuen siitä, onko metalli Valencia tasainen vai pariton:
Metalleille, joilla on pariton valenssi:
Kun metallilla on pariton valenssi, oksidin muodostumisen yleinen reaktio on:

Esimerkiksi natriumoksidin muodostumiseksi, jossa natriumilla on Valencia +1, reaktio on:
Se voi palvella sinua: fosfori: historia, ominaisuudet, rakenne, hankkiminen, käyttö
Toinen esimerkki on ferrioksidin muodostuminen, jossa raudassa on hapettumista tai Valencia +3. Tässä tapauksessa reaktio on:

Metalleille, joilla on Valencia +2:
Kun metallilla on Valencia +2, oksidin muodostumisen yleinen reaktio on:

Esimerkiksi kalsiumoksidien muodostumisen tapauksessa, jossa kalsiumilla on Valencia +2, reaktio on:

Metalleille muiden parien kanssa:
Kun metallilla on jopa valensseja +2: n lisäksi, oksidin muodostumisen yleinen reaktio on:
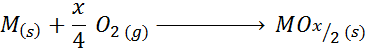
Esimerkki tästä tapauksesta on titaanioksidin muodostumisreaktio (IV):

Perusoksidi -nimikkeistö
Perusoksidille on kolme nimikkeistöjärjestelmää, jotka ovat: perinteinen nimikkeistö, varastot ja systemaattinen.
Kahden ensimmäisen nimikkeistöjärjestelmän mukaisesti oksidin nimeämiseksi on tarpeen tuntea metalli Valencia, kun taas viimeiset.
Perinteinen nimikkeistö
Perinteisen nimikkeistön mukaan perusoksidit on nimetty sanalla jompikumpiXido jota seuraa kationimi. Tämä sukunimi on rakennettu asettamalla metallin nimen juuri sekä metalli Valencia osoittama etuliitteet ja jälkiliitteet:
Oksidi + Etuliite-raí-sufijo
Seuraavassa taulukossa esitetään tiivistelmä etuliitteiden ja jälkiliitteiden määrittämistä koskevat säännöt:
Mahdollisten valenssien lukumäärä | Valencia | Etuliite | Jälkiliite |
1 yksittäinen Valencia | |||
Vain | --- | ___ICO | |
2 Valencias | |||
Vanhukset | --- | ___ICO | |
Vähäinen | --- | ___karhu | |
3 valenssia | |||
Vanhukset | --- | ___ICO | |
Väli- | --- | ___karhu | |
Vähäinen | Hikka___ | ___karhu | |
4 valenssia | |||
Vanhukset | Per___ | ___ICO | |
Keskiarvo | --- | ___ICO | |
Vähäinen välituote | --- | ___ICO | |
Vähäinen | Hikka___ | ___ICO |
Esimerkki:
Hän Usko2JOMPIKUMPI3 Se on rautaoksidi, jolla on Valencia +3. Raudassa on vain kaksi valenssia, jotka ovat +2 ja +3, joten tässä oksidissa raudassa on vanhin kahdesta valenssista. Tästä syystä jälkiliite lisätään ___ICO rautametallin nimen juuressa Holho-.
Se voi palvella sinua: Ei elektrolyyttejä: ominaisuudet ja esimerkitSiksi perinteinen nimi Usko2JOMPIKUMPI3 On: Rautaoksidi.
Nimikkeistö
Tässä järjestelmässä nimi on rakennettu aloittaen sanoilla oksidi -, jota seuraa metallinimi. Lopuksi hänen valencia sijoitetaan roomalaiseen lukumäärään suluihin:
Metalli + nimioksidi (Valencia)
Jos metallilla on vain yksi valenssi, se jätetään pois.
Esimerkki:
Cr2JOMPIKUMPI3 Kromilla on Valencia +3, joten nimivarasto on Kromioksidi (III).
Järjestelmällinen nimikkeistö
Tämä on ainoa kolmesta nimikkeistä, jotka eivät määritä metallia Valencia. Sivuteemaiset nimet osoittavat, kuinka monta happi- ja metalliatomia sisältävät yhdisteen numeerisia etuliitteitä käyttämällä.
Nimi on rakennettu sanalla oksidi edeltävä hän etuliite, joka osoittaa hapen lukumäärän, Sitten artikkeli - jonka jälkeen Metallin nimi sen etuliitteellä.
Etuliite-oksidi + + prefit-metalista
Jotkut etuliitteet ovat:
Määrä | Etuliite |
1 | Pulla |
2 | Antaa |
3 | Tri |
4 | Tetra |
5 | Penta .. |
Esimerkki:
Systemaattisessa nimikkeistössä CR2JOMPIKUMPI3 Sitä kutsutaan dikromatrioksidiksi, koska siinä on kolme happea ja kaksi kromia.
Esimerkkejä perusoksideista
- Natriumoksidi - NA2JOMPIKUMPI
- Rautaoksidi - usko2JOMPIKUMPI3
- Rauta monoksidi - ruma
- Cromic Oxide - CR2JOMPIKUMPI3
- Divanadio Pentaoksidi - V2JOMPIKUMPI5
- Kaliumoksidi - k2JOMPIKUMPI
- Bariumoksidi - Bao

