Lyijyasetaatirakenne, ominaisuudet, hankkiminen, käyttö

- 3867
- 182
- Eddie Hackett
Hän Lyijyasetaatti o Lyijyasetaatti (II) on yhdiste, jonka muodostuu lyijy -ioni (PB2+) ja kaksi asetaatti -ionia (CH3Kujertaa--A. Sen kemiallinen kaava on (CHO3Kujertaa)2PB tai myös PB (valitse3Kujertaa)2.
Se tunnetaan myös "lyijäsokerina" makean maun saamisesta. Se on kuitenkin erittäin myrkyllinen aine. Se on hyvin liukoinen kiteinen kiinteä kiinteä kiinteä. Voit helposti reagoida rikkivetyllä (H2S) Ruskean lyijy sulfidin (PBS) tuottaminen, jota käytetään tämän myrkyllisen kaasun havaitsemisessa teollisuusprosesseissa.
 Kiinteä lyijy (II) asetaatti. Dormoothemist At English Wikipedia/CC by (https: // creativecommons.Org/lisenssit/by/3.0). Lähde: Wikimedia Commons.
Kiinteä lyijy (II) asetaatti. Dormoothemist At English Wikipedia/CC by (https: // creativecommons.Org/lisenssit/by/3.0). Lähde: Wikimedia Commons. Muinaisina aikoina se saatiin suhteellisen helposti, joten sillä oli käyttötarkoituksia, jotka ovat tällä hetkellä täysin kiellettyjä tämän yhdisteen toksisuuden vuoksi.
Lyijyasetaattijauhetta ei tule dispergoitua ympäristöön, koska se muodostaa räjähtäviä seoksia hapen kanssa. Lisäksi se on karsinogeeninen yhdiste eläimille ja ihmisille.
Se imeytyy orgaanisiin kudoksiin helpommin kuin muut lyijyyhdisteet. Sillä on taipumus biologisesti elävissä olennoissa, joten sitä ei pidä hylätä ympäristöön.
[TOC]
Rakenne
Lyijyasetaatissa (II) on alla olevassa kuvassa esitetty rakenne:
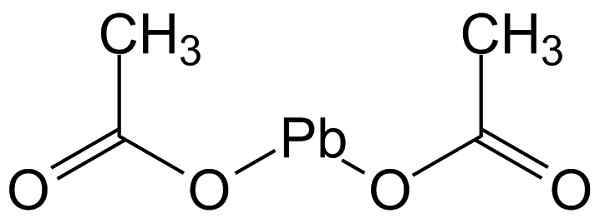 Lyijyasetaatin molekyylirakenne (II). Michał Sobkowski/cc by-Sa (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons.
Lyijyasetaatin molekyylirakenne (II). Michał Sobkowski/cc by-Sa (https: // creativecommons.Org/lisenssit/by-SA/3.0). Lähde: Wikimedia Commons. Nimikkeistö
- Lyijyasetaatti (II)
- Lyijydiaketti
- Johtaa etanoaattia
- Plumboso -asetaatti
- Johtava sokeri
- Saturn -suola
Ominaisuudet
Fyysinen tila
Kiteinen yksiväritön tai valkoinen.
Molekyylipaino
325 g/mol
Sulamispiste
280 ºC
Kiehumispiste
Älä kiehu. Hän hajoaa, kun häntä lämmitetään.
Tiheys
3,25 g/cm3
Liukoisuus
Hyvin liukoinen veteen: 44,3 g/100 ml 20 ° C: ssa. Liukenematon alkoholiin.
PHE
Vesipitoisen liuoksen ja 5%: n pH: n pH on 5,5-6,5.
Kemialliset ominaisuudet
Kun PB (Ococh3-A2 Se liukenee veteen, osa ionisoidaan seuraavasti:
PB (Ococh3-A2 → PB2+ + 2 ch3Kujertaa-
Osaa molekyyleistä ei kuitenkaan ole ionisoitu ja pysyy muodossa:
CH3COO-PB-Ococh3.
Kun PB -ioni2+ Syötä liuos osittain hydrolysoinnit vedessä, joka tuottaa PB -lajia4(VAI NIIN)44+.
Vesipitoinen PB (II) asetaatiliuokset liuottavat lyijyoksidin (PBO).
Se voi palvella sinua: butenoReagoi rikkivetyllä (H2S) Lyijy sulfidin (PBS) ruskean lyijyn muodostamiseksi.
PB (Ococh3-A2 + H2S → PBS + 2 CH3Haittaa
Jos lisätään vesipitoinen ammoniakkiliuos (NH3;.
Muut ominaisuudet
Säteilee hajua kuin etikan. Sillä on makea maku. Sen yleisin kaupallinen muoto on PB -trihydraatti (CH3Kujertaa)2 •3H2JOMPIKUMPI.
 Lyijyasetaatti. Leiem/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons.
Lyijyasetaatti. Leiem/CC BY-SA (https: // creativecommons.Org/lisenssit/by-SA/4.0). Lähde: Wikimedia Commons. Saada
Se voidaan valmistaa liuottamalla oksidi tai lyijykarbonaatti (II) konsentroituneeseen etikkahapeen. Pieniä ohuita metallisia lyijalevyjä voidaan käyttää myös.
Pbo + 2 ch3Cooh → (ch3Kujertaa)2PB + H2JOMPIKUMPI
Muinaiset käytöt
Lääketieteellisesti
Sitä käytettiin laimennetussa liuoksessa sen levittämiseksi hauteena ja pestiin myrkkyvihan aiheuttamissa tulehduksissa ja voitettaessa supistavana. Myös ripulin hoitamiseksi.
Eläinlääketieteellisissä hoidoissa
Sitä käytettiin supistavana ja rauhoittavana voideina pinnallisten tulehdusten ja mustelmien hoidossa.
Kosmetiikassa
Se valmistettiin muinaisina Rooman aikoina. Jotkut naiset sovelsivat sitä kasvoihinsa näyttämään vaalealta, mikä ei ollut vain muoti, vaan myös sosiaalisen aseman asia.
Valkoinen ihonväri osoitti, että nainen ei kuulu työväenluokkaan, vaan Rooman yhteiskunnan korkeimpaan tasoon. Ja tämä tapahtui huolimatta siitä, että tuolloin lääkärit, kuten Plinio El Viejo, tiesivät joitain sen haitallisia vaikutuksia.
Juomien makeutusaineena
Makean maun vuoksi sitä käytettiin antiikissa sokerin korvikkeena, etenkin viinissä ja makeuttamaan ja säästämään hedelmiä.
Useissa sovelluksissa
Joitakin näistä käyttötarkoituksista sovelletaan edelleen, mutta kuultu kirjallisuus ei ole siitä selvää:
- Kromipigmenteissä, liimavärien komponenttina, kuivissa orgaanisissa saippuissa maalauksille, lakkoille ja musteille, kuten veden hylkivälle, estävien maalien vastaisilla maalauksilla.
- Syanidien kultaa hankkimisprosessissa metallien peittämiseksi lyijyllä.
- Puuvillavärien parissa, komponentti kylpyammeten kiinnityspaperia auringonvalolla.
- Hoitoa ja ulkokalusteita ja siten estämään muotilta ja sateen heikkenemisiltä suojaavien aineiden poistamisen.
Nykyiset käyttötarkoitukset
H -havainnassa2S
Tietyissä teollisuusprosesseissa sitä käytetään myrkyllisen H: n havaitsemiseen2S kaasumaisissa virtauksissa koekäyttöroolin kautta, jossa se toimii indikaattorina. Tunnistusraja on 5 ppm (osa miljoonasta).
 Lyijyasetaatti (II) mahdollistaa H: n havaitsemisen2Teollisuuskaasuissa, jotta tätä myrkyllistä kaasua ei vapauteta ilmakehään. Kirjoittaja: Leestilltaolcom. Lähde: Pixabay.
Lyijyasetaatti (II) mahdollistaa H: n havaitsemisen2Teollisuuskaasuissa, jotta tätä myrkyllistä kaasua ei vapauteta ilmakehään. Kirjoittaja: Leestilltaolcom. Lähde: Pixabay. Viimeaikaisissa testeissä nanofibras on sisällytetty yhdessä polymeerin kanssa, joka johtaa uuteen havaitsemismateriaaliin, joka mahdollistaa 400 ppb: n (osaa miljardia) esiintymisen H: n kanssa2S jopa 90%: n kosteus.
Tämän nanomateriaalin korkea potentiaali kolorimetrisenä anturilla tekee siitä soveltuvan H: n havaitsemiseen2S halitoosista kärsivien ihmisten hengityksessä, joiden alue on alle 1 ppm.
 Uudet nanokuidut, jotka sisältävät PB: tä (CH3Kujertaa)2 Ne voivat havaita hyvin pieniä määriä h2S hengossa. Kirjoittaja: Natalia Ovcharenko. Lähde: Pixabay.
Uudet nanokuidut, jotka sisältävät PB: tä (CH3Kujertaa)2 Ne voivat havaita hyvin pieniä määriä h2S hengossa. Kirjoittaja: Natalia Ovcharenko. Lähde: Pixabay. Muiden yhdisteiden saamiseksi
Sen avulla voidaan valmistaa muita lyijyyhdisteitä, kuten karbonaatti ja kromaatti, korkean molekyylipainon lyijysuolat ja antioksidantti rasvahapot kumille.
Ulkoiseen käyttöön
Joidenkin kuultujen lähteiden mukaan tätä yhdistettä käytetään edelleen hiusväreissä, joiden käyttötarkoitukset varoittavat, että sitä ei pidä käyttää muualla kehon osissa, jotka eroavat päänahasta.
Se on myös osa ulkoista käyttöä kipulääketuotteita ja ihonsuojaimia.
Molemmissa tapauksissa ei kuitenkaan ole tarpeeksi näyttöä näiden tuotteiden turvallisuusasteen määrittämiseksi, joten Kanadan ja Yhdysvaltain osavaltion kaltaisissa maissa sen käyttö kaikentyyppisissä kosmetiikassa tai soveltamisessa on kielletty iholla.
Riskejä
Turvallisuus
Se ei ole polttoainetta, mutta se on dispergoitu ympäristössä hienojen hiukkasten muodossa voi tuottaa räjähtäviä seoksia ilman kanssa.
Sitä tulisi varastoida kaukana hapettavista yhdisteistä, vahvoista hapoista ja kemiallisesti aktiivisista metalleista ja viemärien johtavista viemäreistä tai pääsystä viemäriin, jotka johtavat viemäriin.
Terveydelle
Se voi ärsyttää silmiä, hengitysteitä ja ruuansulatusta aiheuttaen päänsärkyä, pahoinvointia, oksentelua, koliikkia, lihasheikkoutta, kouristuksia, kouristuksia, halvauksia, huimausta, tietoisuuden menetystä, koomaa ja jopa kuolemaa.
Se voi palvella sinua: hyposulfurousihappoLyijyasetaatti imeytyy noin 1,5 kertaa nopeammin kuin muut lyijyyhdisteet.
 Lyijyasetaatti vaikuttaa negatiivisesti lasten aivoihin. Kirjoittaja: Pete Lyforth. Lähde: Pixabay.
Lyijyasetaatti vaikuttaa negatiivisesti lasten aivoihin. Kirjoittaja: Pete Lyforth. Lähde: Pixabay. Erittäin alhaiset veripitoisuudet lapsilla voi aiheuttaa yliherkkyyttä tai neuro -myötävammaisuutta, koska se tuottaa vaikutuksia hermostoon. Se voi myös tuottaa anemiaa ja vaurioita munuaisille.
Eläinten tapauksessa on riittävästi todistettu, että se on myrkyllinen lisääntymiselle, syöpää aiheuttaville ja teratogeenisille. Arvioidaan, että ihmiset vaikuttavat samalla tavalla.
Ympäristölle
Sitä pidetään ympäristössä vaarallisena aineena, koska se on myrkyllinen epäpuhtaus. Se on hyvin haitallista vesieliöille. Lintuihin, nisäkkäisiin, maaperän pilaantumiseen ja veden laatuun olisi kiinnitettävä erityistä huomiota.
Tämän yhdisteen bioakumulointi kasveissa ja eläimissä voi tapahtua. Kansainväliset ekologiset instituutiot eivät salli ympäristöön pääsyä, koska se on pysyvä.
Historiallinen myrkytyskotelo
Yksi tutkituista tapahtumista on ollut Yhdysvaltain Andrew Jacksonin (1767-1845) presidentin tapahtumia, joista suoritettiin hoidon "johtava sokeri", joka tuolloin oli perinteinen lääke monimuotoisilla tarkoituksilla.
Vuonna 1999 tehtiin toimenpiteitä kahdelle presidentin elämästä saatulle hiusnäytteelle ja havaittiin, että lyijytasot olivat erittäin korkeat molemmissa näytteissä, mikä on yhteensopiva kärsimän plumbismin oireiden kanssa.
 Andrew Jackson oli päihtynyt lyijypohjaisilla lääkkeillä. Kirjoittaja: Gordon Johnson. Lähde: Pixabay.
Andrew Jackson oli päihtynyt lyijypohjaisilla lääkkeillä. Kirjoittaja: Gordon Johnson. Lähde: Pixabay. Sekä heidän kirjeidensä että elämäkerransa kuvaavat, että hän esitteli muun muassa oireita, kuten pahoinvointia, vatsakramppeja ja halvaantumaa reumaa. Mutta jonkin ajan kuluttua Jackson hylkäsi lyijyasetaatin hoidon, joten hänen terveytensä parani.
Siksi arvioidaan, että hänen kuolemansa ei todennäköisesti johdu lyijymyrkytyksestä.
Viitteet
- TAI.S. Lääketieteen kansalliskirjasto. (2019). Lyijy (ii) asetaatti. PubChemistä toipunut.NCBI.Nlm.NIH.Hallitus.
- Lyijy, d.R -. (Toimittaja) (2003). CRC: n kemian ja fysiikan käsikirja. 85th CRC -lehdistö.
- Puuvilla, f. Albert ja Wilkinson, Geoffrey. (1980). Edistynyt epäorgaaninen kemia. Neljäs painos. John Wiley & Sons.
- Ghazi, a.M. ja Millette, J.R -. (1964). Johtaa. Lyijyasetaatti. Oikeuslääketieteellisessä ympäristössä. ScienEdirect.com.
- Mushak, P. (2011). Johtava ja kansanterveys. Kadehtaissa hiven metallit ja OHER -epäpuhtaudet. ScienEdirect.com.
- Cha, j.-H. et al. (2018). Miljoonan rikkivetyjen kolorimetrinen anturi: Lyijy-särkyneet nanokuidut kohti halitoosidiagnoosia. Anaali Chem 2018 7. elokuuta; 90 (15): 8769-8775. NCBI toipunut.Nlm.NIH.Hallitus.
- Wikimedia -säätiö (2020). Lyijy (ii) asetaatti. Haettu jstk.Wikipedia.org.
- Stewart, s. (2015). "Hohtaminen ja tappava valkoinen". Kohtuullinen ihonväri. Toksikologian ja ympäristöterveyden historiassa. ScienEdirect.com.
- Deppisch, L.M. et al. (1999). Andrew Jacksonin altistuminen elohopealle ja lyijylle: Myrkytetty presidentti? JAMA 1999 11. elokuuta; 282 (6): 569-71. NCBI toipunut.Nlm.NIH.Hallitus.
- « Lyijynitraattirakenne, ominaisuudet, hankkiminen, käyttö
- Lyijyjodidirakenne, ominaisuudet, hankkiminen, käyttö »

